ВВЕДЕНИЕ
Инфекции нижних мочевыводящих путей (ИНМП) относятся к числу наиболее распространенных заболеваний человека, характеризуются склонностью к рецидивированию и существенно ухудшают качество жизни больных [1, 2]. Подавляющее число, до 95%, среди всех пациентов с рецидивирующими ИНМП составляют женщины [2]. После первого эпизода ИНМП у трети из них, даже несмотря на адекватное лечение, в течение 6 месяцев развивается рецидив заболевания [3]. Рецидивирующая ИНМП является наиболее частой причиной обращений женщин за урологической помощью [4]. Возбудители ИНМП представлены главным образом микроорганизмами семейства Enterobacteriaceae, причем доля E. coli достигает 80% среди всех уропатогенов [5]. Основой фармакологического лечения ИНМП является антибактериальная терапия. Однако ее эффективность, особенно в отношении предотвращения рецидива заболевания, часто недостаточна. Это обстоятельство наряду с негативным влиянием антибиотиков на микробиоту желудочно-кишечного тракта и других органов, а также селекция антибиотикорезистентных уропатогенов определили поиск дополнительных стратегий лечения ИНМП [3, 6].
В последнее десятилетие особенно активно обсуждаются возможности альтернативных неантибактериальных методов лечения и профилактики ИНМП – поведенческой, иммуно- и фитотерапии, применения пре- и пробиотиков, D-маннозы [3, 6-11]. Указанные субстанции используются либо по отдельности, либо в составе комбинированных продуктов. К последним относится биологически активная добавка (БАД) «Уронекст®», в состав которой входят D-манноза, экстракт клюквы и витамин D3. Проведенные исследования показали высокую эффективность назначения БАД «Уронекст®» пациентам с ИНМП в разных клинических ситуациях: рецидивирующем бактериально-вирусном цистите [12], при сочетании ИНМП и бактериального вагиноза [13], для профилактики посткоитального цистита [14]. Известно, что адгезия бактерий к слизистой оболочке мочевыводящих путей является первым этапом взаимодействия микро- и макроорганизма и определяет возможность колонизации, инвазии и формирования биопленки.
Предотвращение адгезии уропатогенов является одним из возможных способов лечения и профилактики ИНМП [7, 10]. Ранее наша исследовательская группа изучала механизм лечебного эффекта «Уронекста®» и выявила наличие значимого антиадгезивного эффекта, выражающегося в снижении индекса адгезии (ИА) к эпителиоцитам в 3,1 – 4,8 раза в зависимости от вида уропатогена, а также прямого антибактериального действия данного продукта [15]. Однако многие аспекты лечебного действия «Уронекста®» остались неясными, что и послужило основанием для продолжения научной работы.
Целью настоящего исследования явилась количественная оценка антиадгезивного и антибактериального эффектов БАД «Уронекст®» в отношении уропатогенов, выделенных у пациентов с рецидивирующими ИНМП.
МАТЕРИАЛЫ И МЕТОДЫ
Были исследованы 124 штамма уропатогенов, выделенных из средней порции мочи женщин с рецидивирующими ИНМП. Критериями включения в настоящее исследование были женский пол, возраст 18 лет и старше, давность заболевания не менее трех лет и наличие обострения цистита к началу исследования. Последнее диагностировали на основании жалоб, клинической картины, а также результатов общего анализа мочи (более 10 лейкоцитов в 1 мкл мочи). Критериями невключения были наличие осложненной ИНМП, острого или активной фазы хронического пиелонефрита, полиурии, тяжелых сопутствующих соматических заболеваний, а также прием любых лекарственных препаратов с антибактериальной активностью в течение 4 недель до взятия материала для микробиологического анализа.
Исследование состояло из двух этапов. На первом из них проводили идентификацию уропатогенных микроорганизмов и определяли их чувствительность к исследуемому продукту. Изоляты микроорганизмов, чувствительные к «Уронексту®», являлись материалом для второго этапа исследования. Для оценки активности «Уронекста®» в отношении выделенных уропатогенов in vitro исследовали минимальную ингибирующую концентрацию (МИК) данного продукта, его влияние на ИА уропатогенов в течение 24 часов, а также степень и продолжительность антимикробной активности.
Идентификацию полученных изолятов осуществляли с помощью масс-спектрометрического исследования на приборе Microflex NM LT MALDI-TOF (Bruker Daltonik GmbH, Германия). Анализ спектров и идентификацию микроорганизмов выполняли с использованием программного обеспечения MALDI Biotyper 3.0 (Bruker Daltonik GmbH, Германия). С целью определения антибактериальной активности на чашки Петри с мясопептонным агаром наносили культуры бактерий в концентрации 0,5 MF (McFarland Standard). После подсыхания инокулюма вносили по 1 капле исследуемого продукта «Уронекст®» в трех вариантах: цельного, разведенного в 10 и в 100 раз. После подсыхания капель чашки помещали в термостат при 37ºС. Через 24 часа инкубирования выполняли подсчет числа колоний. Исследование МИК производили методом серийных разведений в стерильных 96-луночных плоскодонных полистироловых планшетах с крышкой в соответствии с регламентирующими документами [16]. Результаты рассчитывали в соответствии с изменением оптической плотности среды. Рост микроорганизмов сопровождается изменением рН среды и, соответственно, изменением окраски индикатора. При этом МИК соответствовала наибольшему разведению исследуемого продукта, тормозящему рост исследуемой культуры микроорганизма.
Длительность антибактериального действия «Уронекста®» оценивали путем определения количества жизнеспособных уропатогенных бактерий после их взаимодействия с исследуемым продуктом. Для этого готовили контрольный и опытный образцы. Контрольный образец представлял из себя суспензию бактерий в мясопептонном бульоне в концентрации 1·10² КОЕ/мл, а опытный образец – смесь из бактерий в такой же стартовой концентрации с добавлением «Уронекста®» в дозе, соответвующей МИК, определенной ранее для каждого из выделенных уропатогенов. Высев на чашки Петри с мясопептонным агаром производили сразу после приготовления образцов, а далее – через каждый час. Чашки с посевами помещали в термостат при 37°С на 24 часа. После этого производили подсчет колоний бактерий (КОЕ/мл) на каждой чашке опытных и контрольных образцов.
Для количественной оценки антиадгезивного действия «Уронекста®» оценивали ИА выделенных уропатогенов на клетках буккального эпителия в присутствии исследуемого продукта в терапевтической концентрации в течение 24 часов по оригинальной методике А.С. Благонравовой и соавт. [17]. Забор клеток буккального эпителия проводили в день исследования у одного и того же донора путем соскоба с внутренней поверхности слизистой оболочки щеки стерильной ложечкой объемом 3 мл или шпателем после предварительного трехкратного полоскания ротовой полости физиологическим раствором. Полученные путем соскоба клетки помещали в забуференный физиологический раствор при рН 7,2–7,4, отмывали от индигенной микрофлоры центрифугированием при скорости 35 g в течение 10 минут и доводили до необходимой концентрации 3×106 кл/мл путем расчета в камере Горяева. Затем отмытые клетки разделяли по 0,5 мл в пробирки и готовили мазки с окраской по Граму. Просматривали 50 эпителиальных клеток, о состоянии естественной адгезии судили по числу S. salivarius в пересчете на 1 эпителиоцит. Для изучения искусственной адгезии на буккальном эпителии использовали штаммы уропатогенных микроорганизмов. Для этого из суточной бактериальной культуры, выросшей на плотной питательной среде, готовили смыв забуференным физиологическим раствором, отмывали центрифугированием при 35 g в течение 10 минут, затем доводили в физиологическом растворе по стандарту мутности до концентрации 3×108 КОЕ/мл. В одной стерильной центрифужной пробирке соединяли равные объемы компонентов эксперимента: 0,5 мл бактериальной культуры и 0,5 мл буккального эпителия (контроль). В другой центрифужной пробирке соединяли 0,5 мл бактериальной культуры, 0,5 мл буккального эпителия и 0,5 мл продукта «Уронекст®» в минимальной ингибирующей концентрации для каждого микроорганизма. Пробирки со всеми компонентами интенсивно встряхивали и помещали в термостат при температуре 37°С на 30 мин. По истечении времени инкубации культуры отмывали от неприкрепившихся микроорганизмов, готовили мазки, фиксировали этиловым спиртом и окрашивали по Граму. ИА рассчитывали по формуле: ИА = Б50 / 50Э, где Б50 – количество бактерий, прикрепившихся к 50 эпителиоцитам, 50Э – 50 изученных эпителиоцитов. Одной из задач исследования была оценка продолжительности антиадгезивного эффекта продукта «Уронекст®». Для этого пробирки со всеми компонентами помещали в термостат при температуре 37°С на разные промежутки времени: 30 минут, 1 час, 2 часа, 4 часа, 6 часов, 8 часов и 24 часа. Подготовка культур и подсчет ИА проводились по описанной выше методике.
Систематизацию, обработку и статистический анализ материалов исследования проводили с использованием пакета прикладных статистических программ Statistica 10 En (StatSoft, Inc.). Независимые выборки сравнивались критерием Стьюдента для нормальных распределений и критерием Манна-Уитни в иных слчаях. Различия считали достоверными при уровне значимости р≤0,05.
РЕЗУЛЬТАТЫ
Среди выделенных 124 штаммов уропатогенных микроорганизмов 95 (76,6%), были грамотрицательными, а 29 (23,4%) – грамположительными. К первым относились Escherichiacoli (n=61), Klebsiella spp. (n=21), Enterobacter spp. (n=6) и Аcinetobacterspp.(n=7), ко вторым – Staphylococcus spp. (n=9), Enteroccocus spp. (n=16), Streptococcus spp. (n=3) и Corynebacteriumspp.(n=1).
На первом этапе исследования была проведена оценка антимикробного эффекта продукта «Уронекст®» в отношении выделенных уропатогенов, результаты которой представлены в таблице 1. Выявлено прямое антибактериальное действие «Уронекста®» в отношении 53,7% штаммов грамотрицательных и 51,7% штаммов грамположительных микроорганизмов. Так, чувствительность к «Уронексту®» отмечена у 51,8% штаммов E. coli, 57,1% штаммов Klebsiella spp., 43,8% штаммов Enteroccocus spp.
Таблица 1. Антибактериальная активность БАД «Уронекст®» в отношении выделенных уропатогенов
Table 1. Antibacterial activity of the Uronext® dietary supplement against isolated uropathogens
| Микроорганизм Microorganism |
Чувствительность к Уронексту®, n (%)/ Sensitivity to Uronext®, n (%) |
||
|---|---|---|---|
| Да/Yes | Нет/No | ||
| Грамотрицательные бактерии (n=95) Gram-negative bacteria (n=95) | E. coli (n=61) | 31 (51,8%) | 30(48,2%) |
| Klebsiellaspp. (n=21) | 12 (57,1%) | 9 (42,9 %) | |
| Enterobacterspp. (n=6) | 3 (50%) | 3 (50%) | |
| Аcinetobacterspp. (n=7) | 5 (71,4%) | 2 (28,6%) | |
| Всего | 51 (53,7%) | 44 (46,3%) | |
| Грамположительные бактерии (n=29) Gram-positive bacteria (n=29) | Staphylococcusspp. (n=9) | 5 (55,6%) | 4 (44,4%) |
| Enteroccocusspp. (n=16) | 7 (43,8%) | 9 (56,2%) | |
| Streptococcusspp. (n=3) | 2 (66,7%) | 1 (33,3%) | |
| Corynebacteriumspp. (n=1) | 1 (100%) | - | |
| Всего/Total | 15 (51,7%) | 14 (48,3%) | |
Изоляты микроорганизмов, чувствительные к «Уронексту®», явились биологическим материалом для определения МИК изучаемого продукта в отношении выделенных уропатогенов (табл. 2). Полученные данные свидетельствуют о наибольшей активности «Уронекста®» в отношении представителей семейства Enterobacteriaceae, при этом его МИК для грамположительных микроорганизмов оказалась в 8 раз выше по сравнению с грамотрицательными. В отношении Acinetobacter spp., являющихся одним из наиболее значимых уропатогенов с множественной лекарственной резистентностью, «Уронекст®» также продемонстрировал антибактериальный эффект с МИК 25 мг/мл.
Таблица 2. Значения минимальной ингибирующей концентрации БАД «Уронекст®» в отношении основных уропатогенов
Table 2. Values of the minimum inhibitory concentration of the dietary supplement «Uronext®» in relation to the main uropathogens
| Микроорганизм Microorganism |
МИК Уронекста®, мг/мл (медиана)/ MIC of Uronext®, mg/ml (median) |
|
|---|---|---|
| Да/Yes | ||
| Грамотрицательные бактерии (n=51) Gram-negative bacteria (n=51) | E. coli (n=31) | 25 |
| Klebsiellaspp. (n=12) | 50 | |
| Enterobacterspp. (n=3) | 50 | |
| Аcinetobacterspp. (n=5) | 25 | |
| Грамположительные бактерии (n=12) Gram-positive bacteria (n=12) | Staphylococcusspp. (n=3) | 100 |
| Enteroccocusspp. (n=7) | 200 | |
| Streptococcusspp. (n=2) | 50 | |
Значительный практический интерес представляет количественная оценка способности микроорганизмов к адгезии – первому и ключевому этапу инфекционного процесса. В настоящей работе мы изучили выраженность и продолжительность антиадгезивного эффекта «Уронекста®» для разных уропатогенов. С этой целью по методике, описанной в предудыщем разделе, производили подсчет количества микробных клеток, адгезированных на одном буккальном эпителиоците, и рассчитывали ИА. Данный способ относится к прямым методам оценки бактериальной адгезии. Результаты исследования представлены в таблице 3. Через 30 минут после добавления «Уронекста®» в культуру бактерий ИА снижался в 2-3,3 раза у разных микроорганизмов по сравнению с контролем.
Таблица 3. Сравнительная оценка выраженности и продолжительности антиадгезивного эффекта БАД «Уронекст®»
в отношении уропатогенных микроорганизмов (значения индекса адгезии, M±m)
Table 3. Comparative assessment of the severity and duration of the anti-adhesive effect of the Uronext® dietary supplement against uropathogenic microorganisms (adhesion index values, M±m)
| Вид микроорганизмов/ группа Type of microorganisms/ group |
Esherichiacoli (n=31) |
Klebsiellapneumoniae (n=12) |
Enterobacteraerogenes (n=3) |
Аcinetobacterbaumannii (n=5) |
Staphylococcusepidermidis (n=3) |
Enteroccocusfaecalis (n=7) |
Streptococcusagalactiae (n=2) |
|---|---|---|---|---|---|---|---|
| 30 мин после начала исследования / 30 minutes after the start of the study | |||||||
| К | 25±5 | 20±5 | 22±5 | 20±4 | 32±6 | 30±6 | 26±6 |
| У | 8±3* | 6±2** | 7±3 | 6±4** | 15±5 | 14±4** | 13±4 |
| 1 час после начала исследования / 1 hour after the start of the study | |||||||
| К | 29±5 | 35±5 | 33±5 | 32±5 | 53±6 | 50±6 | 48±6 |
| У | 7±3* | 4±2* | 4±2** | 3±2* | 10±4* | 10±3* | 10±3 |
| 2 часа после начала исследования / 2 hours after the start of the study | |||||||
| К | 37±6* | 41±6 | 45±6 | 44±6 | 62±7 | 65±7 | 55±7 |
| У | 6±3 | 3±2* | 3±2* | 3±2* | 13±4* | 12±4* | 11±4 |
| 4 часа после начала исследования / 4 hours after the start of the study | |||||||
| К | 48±7 | 64±7 | 62±7 | 63±7 | 71±7 | 77±7 | 67±7 |
| У | 6±3* | 3±2* | 4±2* | 4±2* | 15±4* | 15±4* | 14±4 |
| 6 часов после начала исследования / 6 hours after the start of the study | |||||||
| К | 66±8 | 81±9 | 78±8 | 80±8 | 88±8 | 89±9 | 78±9 |
| У | 8±3* | 7±3* | 9±3* | 8±3* | 29±5* | 26±5* | 28±5 |
| 8 часов после начала исследования / 8 hours after the start of the study | |||||||
| К | 95±10 | 95±10 | 86±9 | 88±9 | 94±9 | 101±11 | 94±10 |
| У | 11±4* | 14±4* | 18±4* | 22±5* | 42±6** | 48±6* | 44±6 |
| 24 часа после начала исследования / 24 hours after the start of the study | |||||||
| К | 125±15 | 111±13 | 97±11 | 97±10 | 128±12 | 134±14 | 112±13 |
| У | 45±9* | 26±5* | 33±6** | 38±7* | 75±8** | 77±8* | 67±8 |
Примечание: К – контроль; У – при добавлении «Уронекста»; * p<0,01 по сравнению с контролем; **p<0,05 – по сравнению с контролем
Note: K – control; U – when adding «Uronext®»; * p<0,01 compared to control; **p<0,05 – compared to control
Минимальное значение ИА зарегистрировано через 2 часа после добавления исследуемого продукта и составляло в зависимости от вида микроорганизмов от 3 до 13, тогда как в контрольной группе – от 37 до 65. Значения ИА в основной группе были значимо меньше по сравнению с контролем на протяжении всего 24-часового времени наблюдения. При этом наименьшие значения ИА отмечались в течение первых 4 часов после добавления исследуемого продукта. Снижение значений ИА при добавлении «Уронекста®» для грамотрицательных микроорганизмов было более выражено, чем для грамположительных. Так, через 4 часа от начала эксперимента значения ИА для грамотрицательных бактерий варьировали в диапазоне от 3 до 6 (в контроле – от 48 до 64), тогда как для грамположительных – от 14 до 15 (в контроле – от 67 до 77). Начиная с 6 часов от начала исследования отмечена тенденция к повышению значений ИА, более выраженная для грамположительных микроорганизмов. Через 24 часа наблюдения значения ИА для всех грамотрицательных микроорганизмов оставались достоверно меньшими, чем в контрольной группе. На заключительном этапе настоящего исследования мы оценивали выраженность антимикробного эффекта «Уронекста®» в динамике в отношении выделенных уропатогенных микроорганизмов. Результаты исследования представлены на рис. 1-7.
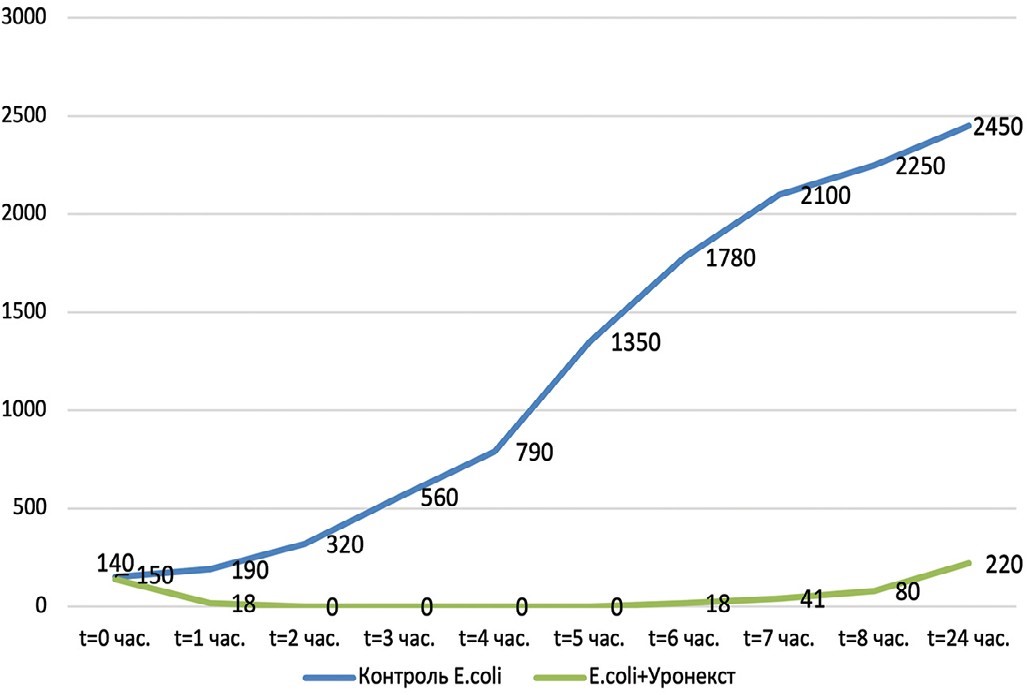
Рис. 1. Выраженность антибактериального эффекта «Уронекста®» в отношении Escherichia coli (МИК 25 мг/мл). По оси ординат – количество живых бактерий (КОЕ/мл), по оси абсцисс – время от начала эксперимента
Fig. 1. The severity of the antibacterial effect of «Uronext®» against Escherichia coli (MIC 25 mg/ml). The ordinate axis is the number of live bacteria (CFU/ml), the abscissa axis is the time from the start of the experiment
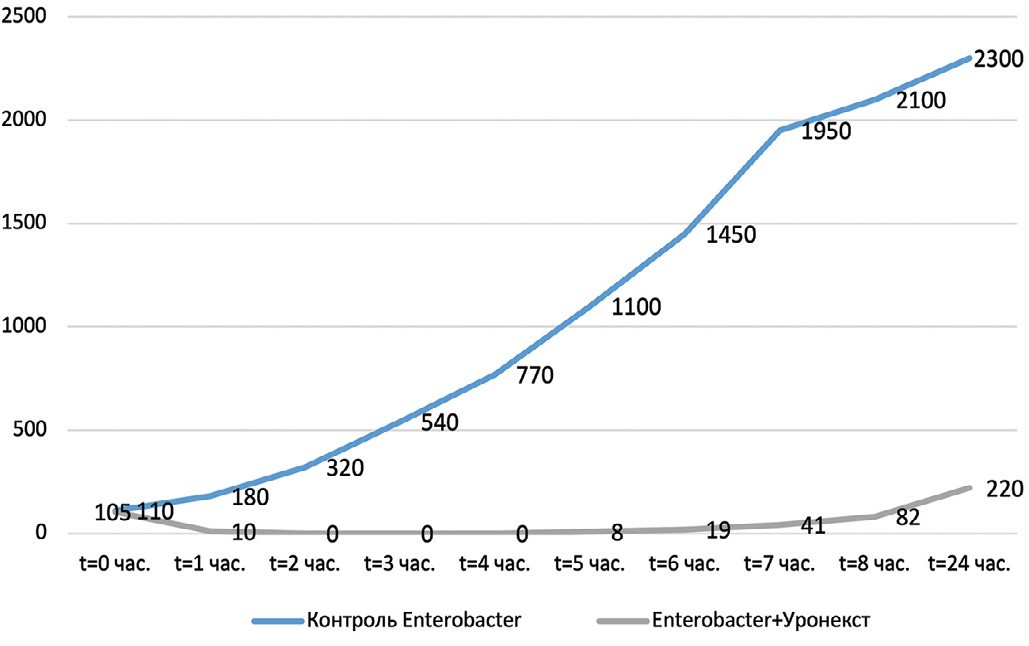
Рис. 2. Выраженность антибактериального эффекта «Уронекста®» в отношении Klebsiella pneumoniae (МИК 50 мг/мл). По оси ординат – количество живых бактерий (КОЕ/мл), по оси абсцисс – время от начала эксперимента
Fig. 2. The severity of the antibacterial effect of «Uronext®» against Klebsiella pneumoniae (MIC 50 mg/ml). The ordinate axis is the number of live bacteria (CFU/ml), the abscissa axis is the time from the start of the experiment
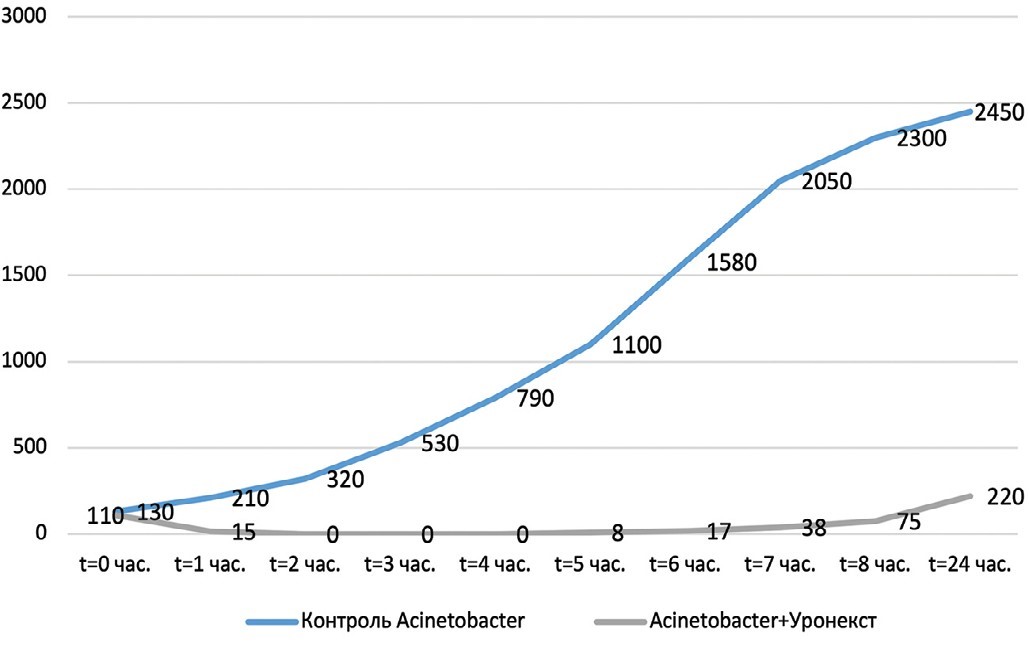
Рис. 3. Выраженность антибактериального эффекта «Уронекста®» в отношении Enterobacter aerogenes (МИК 50 мг/мл). По оси ординат – количество живых бактерий (КОЕ/мл), по оси абсцисс – время от начала эксперимента.
Fig. 3. The severity of the antibacterial effect of «Uronext®» against Enterobacteraerogenes (MIC 50 mg/ml). The ordinate axis is the number of live bacteria (CFU/ml), the abscissa axis is the time from the start of the experiment
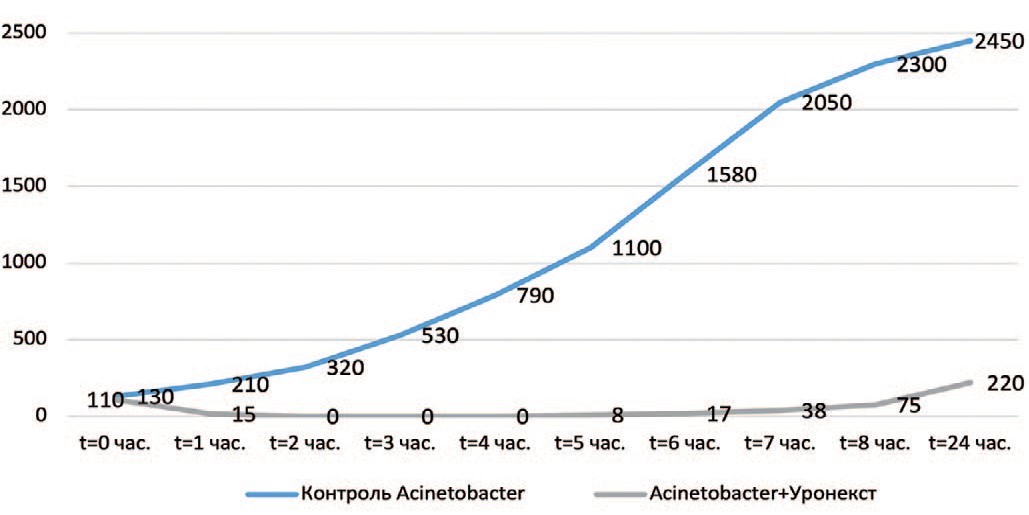
Рис. 4. Выраженность антибактериального эффекта «Уронекста®» в отношении Аcinetobacter baumannii (МИК 25 мг/мл). По оси ординат – количество живых бактерий (КОЕ/мл), по оси абсцисс – время от начала эксперимента
Fig. 4. The severity of the antibacterial effect of «Uronext®» against Acinetobacterbaumannii (MIC 25 mg/ml). The ordinate axis is the number of live bacteria (CFU/ml), the abscissa axis is the time from the start of the experiment
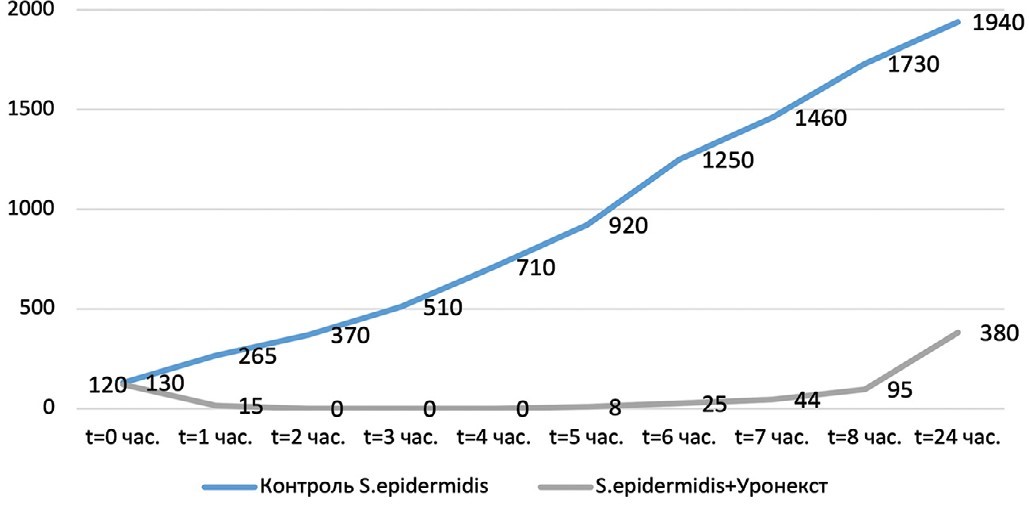
Рис. 5. Выраженность антибактериального эффекта «Уронекста®» в отношении Staphylococcus epidermidis (МИК 100 мг/мл). По оси ординат – количество живых бактерий (КОЕ/мл), по оси абсцисс – время от начала эксперимента
Fig. 5. The severity of the antibacterial effect of «Uronext®» against Staphylococcusepidermidis (MIC 100 mg/ml). The ordinate axis is the number of live bacteria (CFU/ml), the abscissa axis is the time from the start of the experiment
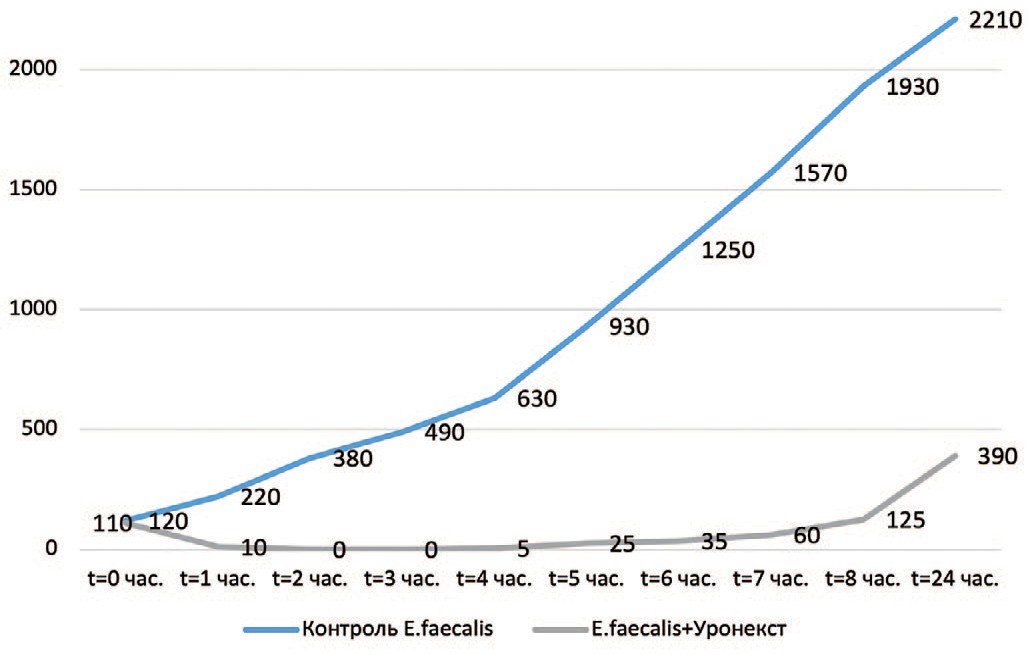
Рис. 6. Выраженность антибактериального эффекта «Уронекста®» в отношении Enterococcus faecalis (МИК 200 мг/мл). По оси ординат – количество живых бактерий (КОЕ/мл), по оси абсцисс – время от начала эксперимента
Fig. 6. The severity of the antibacterial effect of «Uronext®» against Enterococcusfaecalis (MIC 200 mg/ml). The ordinate axis is the number of live bacteria (CFU/ml), the abscissa axis is the time from the start of the experiment
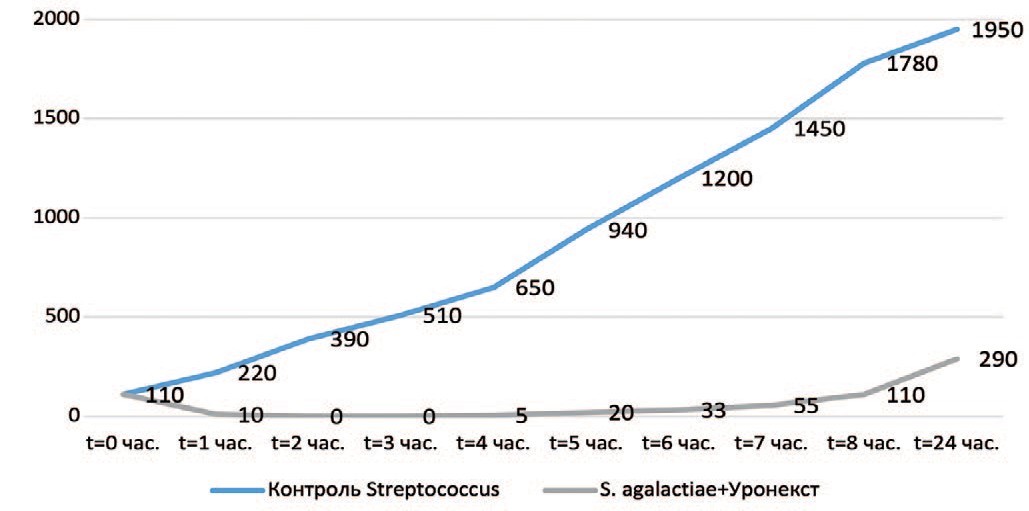
Рис. 7. Выраженность антибактериального эффекта «Уронекста®» в отношении Streptococcus agalactiae (МИК 50 мг/мл). По оси ординат – количество живых бактерий (КОЕ/мл), по оси абсцисс – время от начала эксперимента
Fig. 7. The severity of the antibacterial effect of «Uronext®» against Streptococcusagalactiae (MIC 50 mg/ml). The ordinate axis is the number of live bacteria (CFU/ml), the abscissa axis is the time from the start of the experiment
Установлено, что в отношении всех изучаемых микроорганизмов (Escherichia coli, Klebsiella pneumoniae, Enterobacter aerogenes, Аcinetobacter baumannii, Staphylococcus epidermidis, Enterococcus faecalis, Streptococcus agalactiae) антибактериальная активность «Уронекста®» in vitro развивалась уже через 1 час, достигала максимума через 2 часа и сохранялась на этом уровне на протяжении 5 часов исследования. Через 6 часов наблюдения отмечена тенденция к снижению антибактериальной активности в виде повышения количества жизнеспособных колоний уропатогенов. При этом даже через 24 часа в образцах после внесения «Уронекста®» число КОЕ исследуемых уропатогенов было существенно ниже по сравнению с контролем. Указанная тенденция была характерна для всех исследуемых микроорганизмов.
ОБСУЖДЕНИЕ
Результаты бактериологического исследования показали, что продукт «Уронекст®» обладает антимикробной активностью в отношении более половины (53,2%) выделенных уропатогенных микроорганизмов. Установлено, что in vitro «Уронекст®» проявляет антибактериальное действие как в отношении грамотрицательных, так и грамположительных микроорганизмов. Важно подчеркнуть, что значения его МИК были различны в зависимости от вида микроорганизмов. При этом в отношении грамотрицательных бактерий МИК оказались в 8 раз ниже, чем для грамположительных. Эти наблюдения подтверждают результаты, полученные нами ранее [15]. Количественная оценка антиадгезивного эффекта показала, что in vitro «Уронекст®» снижает адгезивный потенциал уропатогенов в 2-3,3 раза в зависимости от вида микроорганизмов. Максимальное снижение ИА было зарегистрировано через 2 часа от начала исследования и сохранялось на достигнутом уровне в течение 4 часов. Эта тенденция была характерна как для грамотрицательных, так и для грамположительных микроорганизмов. Начиная с 6 часов от начала эксперимента ИА начинал повышаться, причем более выражено для грамположительных уропатогенов. Длительность антибактериального эффекта БАД «Уронекст®» коррелировала с длительностью антиадгезивного эффекта. Через 6 часов наблюдения зарегистрировано уменьшение антибактериальной активности продукта, что выражалось в повышении количества жизнеспособных колоний уропатогенов, однако даже через 24 часа от начала эксперимента количество микробных клеток в опытных образцах было существенно ниже, чем в контроле.
Полученные данные свидетельствуют о наличии связи между значениями ИА и выраженностью антибактериального действия продукта «Уронекст®». Полагаем, что антибактериальная активность обусловлена однонаправленным действием субстанций, входящих в его состав – D-маннозы, экстракта клюквы и витамина D3. Именно D-манноза и экстракт клюквы обеспечивают антиадгезивный эффект «Уронекста®».
Известно, что инфекционный процесс протекает по стандартному сценарию:
- адгезия микроорганизмов к эпителию макроорганизма;
- инвазия микроорганизмов во внутренние среды макроорганизма;
- пролиферация микроорганизмов во внутренней среде макроорганизма [18].
Структуры уропатогенных бактерий, обеспечивающие их фиксацию к эпителиоцитам, обозначаются термином адгезины. Они неоднородны у различных видов бактерий по своим морфологическим, биохимическим, антигенным и функциональным свойствам. У грамотрицательных бактерий в адгезии участвуют различные фимбрии (пили), белки и липополисахариды наружной мембраны, а у грамположительных – белки клеточной стенки, тейхоевые и липотейхоевые кислоты [19]. Фимбриальные адгезины обеспечивают более эффективную адгезию, чем нефимбриальные [20]. Специфическая адгезия на поверхности слизистых мочевыводящих путей является наиболее важным механизмом, с помощью которого бактерии колонизируют и/или инфицируют макроорганизм. Развитие воспалительной реакции происходит при прочной фиксации бактерий к уротелиальным клеткам и последующем размножении микроорганизмов. После специфической адгезии нормальный ток жидкости, слизи или мочи не смывает бактерии с поверхности слизистой. Размножение бактерий в этом случае достигает критической массы, что сопровождается инвазией микроорганизмов во внутреннюю среду организма хозяина.
У представителей семейства Enterobacteriaceae адгезия является ключевым звеном в патогенезе ИНМП, причем в ней участвуют как фимбриальные, так и нефимбриальные адгезины [19]. Установлено, что более 60% уропатогенных штамов E. coli имеют от 5 до 15 типов фимбрий [3]. Наиболее распространенными из них являются тип 1, тип 3, тип 9, S, P, F1C и Auf [21]. Пили 1 типа обнаруживают у 80% уропатогенных штаммов E. coli и 90% уропатогеных штаммов Kl. pneumoniae [22]. Различные типы пили различаются по характеру серологической реакции гемагглютинации и специфичности рецепторов: пили 1 типа обеспечивают маннозочувствительную гемагглютинацию, а Р-пили – маннозорезистентную гемагглютинацию [23]. Пили 1 типа представляют собой многочисленные спиралевидные выросты на поверхности бактериальной клетки (100-500 пилей на клетку), имеют длину до 2 мкм и ширину до 10 нм [3]. По молекулярной структуре эти органеллы состоят из нескольких различных субъединиц, включая повторяющиеся единицы белка FimA, FimF, FimG и белка адгезии FimH [24]. Основными рецептором для FimH являются расположенные на поверхности зонтичных клеток уротелия маннозосодержащий гликопротеин уроплакин 1а, гликопротеин Тамма –Хорсфалла, β1- и α3-интегрины [3, 24]. Контакт FimH с высокоманнозилированным уроплактином 1а обеспечивает стабильную бактериальную адгезию. Кроме того, FimH также отвечает за образование биопленок, пролиферацию, инвазию и образование внутриклеточных бактериальных сообществ [3]. Благодаря множественности функций лиганда FimH пили 1типа являются ключевым фактором вирулентности уропатогеннов штаммов семейства Enterobacteriaceae [3, 6]. Исходя из вышеизложенного, адгезин FimH оказался наиболее подходящей мишенью для блокирования адгезии. Высокие концентрации D-маннозы в моче приводят к насыщению адгезина FimH, что не позволяет бактериям связываться с рецепторами уротелия и прикрепляться к стенке мочевого пузыря [25]. Эксперментально доказано, что полифенольные соединения (проантоцианидины, флавонолы и их гликозиды), содержащиеся в экстракте клюквы, способны ингибировать прикрепление P-пили E. coli к гликопротеиновым рецепторам уротелия [26]. Основным недостатком антиадгезивной терапии является тот факт, что большинство микроорганизмов имеют несколько механизмов адгезии. В продукте «Уронекст®» содержится экстракт клюквы, блокирующий адгезию P-пили, и D-манноза, которая нарушает адгезию пили 1 типа. Одновременное воздействие на несколько механизмов адгезии микроорганизмов позволяет добиться более выраженного и стойкого антиадгезивного эффекта.
ЗАКЛЮЧЕНИЕ
Проведенное исследование позволило установить и количественно оценить выраженность антиадгезивного и антибактериального эффектов продукта «Уронекст®» в отношении уропатогенных микрорганизмов, выделенных из мочи пациентов с рецидивирующими ИНМП. Полученные данные свидетельствуют о наличии связи между значениями ИА и выраженностью антибактериального действия «Уронекста®». Назначение БАД «Уронекст®» больным с рецидивирующими ИНМП представляется патогенетически оправданным.
ЛИТЕРАТУРА
- Перепанова Т.С., Козлов Р.С., Руднов В.А., Синякова Л.А., Палагин И.С. Антимикробная терапия и профилактика инфекций почек, мочевыводящих путей и мужских половых органов. Федеральные клинические рекомендации М., 2022;126 с. [Perepanova T.S., Kozlov R.S., Rudnov V.A., Sinyakova L.A., Palagin I.S. Antimicrobial therapy and prevention of infections of the kidneys, urinary tract and male genital organs. Federal clinical guidelines M., 2022; 126 p. (In Russian)].
- Goedken AM, Foster KY, Ernst EJ. Urinary Tract Infection Frequency and Prescription Prophylaxis in Females and Males with Recurrent Urinary Tract Infection. Pathogens 2023;12(2):170. https://doi.org/10.3390/pathogens1202017.
- Sarshar M, Behzadi P, Ambrosi C, Zagaglia C, Palamara AT, Scribano D. FimH and Anti-Adhesive Therapeutics: A Disarming Strategy Against Uropathogens. Antibiotics (Basel) 2020;9(7):397. https://doi.org/10.3390/antibiotics9070397.
- Слесаревская М.Н., Игнашов Ю.А., Кузьмин И.В., Аль-Шукри С.Х. Стойкая дизурия у женщин: этиологическая диагностика и лечение. Урологические ведомости 2021;11(3):195-204. [Slesarevskaya M.N., Ignashov Y.A., Kuzmin I.V., Al-Shukri S.K. Persistent dysuria in women: etiological diagnostics and treatment. Urologicheskiye vedomosti= Urology reports 2021; 11(3):195-204 (In Russian)]. https://doi.org/10.17816/uroved81948
- Палагин И.С., Сухорукова М.В., Дехнич А.В., Эйдельштейн М.В., Перепанова Т.С., Козлов Р.С., исследовательская группа «ДАРМИС-2018». Антибиотикорезистентность возбудителей внебольничных инфекций мочевых путей в России: результаты многоцентрового исследования «ДАРМИС-2018». Клиническая микробиология и антимикробная химиотерапия 2019;21(2):134–46. [Palagin I.S., Sukhorukova M.V., Dekhnich A.V., Edelstein M.V., Perepanova T.S., Kozlov R.S., «DARMIS-2018» Study Group. Antimicrobial resistance of pathogens causing community-acquired urinary tract infections in Russia:results of the multicenter study «DARMIS-2018». Klinicheskaja mikrobiologija i antimikrobnaja himioterapija = Clinical Microbiology and Antimicrobial Chemotherapy 2019; 21(2):134–46 (In Russian)]. https://doi.org/10.36488/cmac.2019.2.134-146.
- Terlizzi ME, Gribaudo G, Maffei ME. UroPathogenic Escherichia coli (UPEC) Infections: Virulence Factors, Bladder Responses, Antibiotic, and Non-antibiotic Antimicrobial Strategies. Front Microbiol 2017;8:1566. https://doi.org/10.3389/fmicb.2017.01566.
- Loubet P, Ranfaing J, Dinh A, Dunyach-Remy C, Bernard L, Bruyère F, et al. Alternative Therapeutic Options to Antibiotics for the Treatment of Urinary Tract Infections. Front Microbiol 2020;11:1509. https://doi.org/10.3389/fmicb.2020.01509.
- Шорманов И.С., Соловьев А.С., Чирков И.А., Щедров Д.Н., Красняк С.С., Шадеркин И.А. Возможности препаратов на основе D-маннозы и растительных компонентов в лечении и профилактике рецидивирующих инфекций нижних мочевых путей у женщин. Урологические ведомости 2022;12(1):13-20 [Shormanov I.S., Solovyov A.S., Chirkov I.A., Shchedrov D.N., Krasnyak S.S., Shaderkin I.A. Opportunities of drugs based on D-mannose and herbal components in the treatment and prevention of recurrent lower urinary tract infections in women. Urologicheskiye vedomosti = Urology reports 2022;12(1):13-20 (In Russian)]. https://doi.org/10.17816/uroved84084.
- Кульчавеня Е.В., Неймарк А.И., Цуканов А.Ю., Плугин П.С., Неймарк А.Б., Раздорская М.В. Комбинированная терапия больных рецидивирующим циститом с применением комплекса природных антимикробных пептидов и цитокинов: первые результаты. Урология 2022;(6):47–55 [Kulchavenya E.V., Neymark A.I., Tcukanov A.Yu., Plugin P.S., Neymark A.B., Razdorskaya M.V. Combined therapy of patients with recurrent cystitis using a complex of natural antimicrobial peptides and cytokines: first results. Urologiya = Urologiia 2022;(6):47–55. (In Russian)]. https://doi.org/10.18565/urology.2022.6.47-55.
- Кузьмин И.В., Слесаревская М.Н., Аль-Шукри С.Х. Антиадгезивная стратегия неантибактериальной профилатики рецидивирующей инфекции нижних мочевыводящих путей. Урология 2021;(3):5–12 [Kuzmin I.V., Slesarevskaya M.N., Al-Shukri S.H. Antiadhesive strategy for non-antibacterial prophylaxis of recurrent lower urinary tract infections. Urologiya = Urologiia 2021;(3):5–12. (In Russian)]. https://doi.org/10.18565/urology.2021.3:5–12.
- Слесаревская М.Н., Кузьмин И.В., Аль-Шукри С.Х. Инфекция нижних мочевыводящих путей: новые возможности фитотерапии. Урология 2022;(2):103–12. [Slesarevskaya M.N., Kuz'min I.V., Al-Shukri S.H. Infection of the lower urinary tract: new possibilities of herbal medicine. Urologiya = Urologiia 2022;(2):103–12. (In Russian)]. https://doi.org/10.18565/urology.2022.2.103-112.
- Ибишев Х.С., Гаджиева З.К., Мамедов В.К. Эффективность биологически активной добавки Уронекст при хроническом рецидивирующем бактериально-вирусном цистите с множественной устойчивостью к антибактериальным препаратам. Урология 2022;(2):90–4. [Ibishev Kh.S., Gadzhieva Z.K., Mamedov V.K. Efficacy of Uronext in chronic recurrent bacterial-viral cystitis with multiple resistance to antibacterial drugs. Urologiya = Urologiia 2022;(2):90–4. (In Russian)]. https://doi.org/10.18565/urology.2022.2.90-94.
- Тевлин К.П., Ханалиев Б.В., Тевлин Д.К. Свойства и безопасность комбинированной биологически активной добавки Уронекст в комплексном лечении острого (обострение хронического) цистита у женщин с бактериальным вагинозом. Consilium Medicum 2021;23(7):571–8. [Tevlin KP, Khanaliev BV, Tevlin DK. Properties and safety of combined dietary supplement Uronext in complex treatment of acute (recrudescence of chronic) cystitis in women with bacterial vaginosis. Consilium Medicum 2021;23(7):571–8. (In Russian)]. https://doi.org/10.26442/20751753.2021.7.201061.
- Неймарк А.И., Неймарк Б.А., Ноздрачев Н.А., Ковалева Ю.С., Раздорская М.В., Мельник М.А. Возможности профилактики посткоитального цистита. Урология 2022;(3):33–41 [Neymark A.I., Neymark B.A., Nozdrachev N.A., Kovaleva Yu.S., Razdorskaya M.V., Mel'nik M.A. Possibilities for the prevention of postcoital cystitis. Urologiya = Urologiia 2022;(3):33–41. (In Russian)]. https://doi.org/10.18565/urology.2022.3.33-41.
- Слесаревская М.Н., Кузьмин И.В., Краева Л.А., Смирнова Е.В. Эффективность комбинированной биологически активной добавки Уронекст у женщин с рецидивирующими циститами: клинико-микробиологическое исследование. Экспериментальная и клиническая урология 2022;15(2)120-8. [Slesarevskaya M.N., Kuzmin I.V., Kraeva L.A., Smirnova E.V. The effectiveness of the combined dietary supplement Uronext in women with recurrent cystitis: a clinical and microbiological study. Eksperimentalnaya i klinicheskaya urologiya = Experimental and Clinical Urology 2022;15(2):120-8. (In Russ- ian)]. https://doi.org/10.29188/2222-8543-2022-15-2-120-128.
- Определение чувствительности микроорганизмов к антимикробным препаратам. Версия 2021-01. Рекомендации Межрегиональной ассоциации по клинической микробиологии и антимикробной химиотерапии МАКМАХ;222 c. [Электронный ресурс]. [Determination of the sensitivity of icroorganisms to antimicrobial drugs. Version 2021-01. Recommendations of the Interregional аssociation for clinical microbiology and antimicrobial chemotherapy AKMAKH;222 p. [Electronic resource]. (In Russian)]. URL: https://www.antibiotic.ru/files/321/clrec-dsma2021.pdf (accessed 18.12.2023).
- Благонравова А.С., Афонин А.Н., Воробьева О.Н., Широкова И.Ю. Сравнительный анализ адгезивности микроорганизмов, выделенных от больных и с объектов внешней среды лечебно-профилактических учреждений. Медицинский альманах 2011;5(18):215-8. [Blagonravova A.S., Afonin A.N., Vorobeva O.N., Shirokova I.Yu. Comparative analysis of the adhesiveness of microorganisms isolated from patients and from objects of the external environment of medical institutions. Meditsinskiy almanah = Medical Almanac 2011;5(18):215-8. (In Russian)].
- Сидоренко С.В. Инфекционный процесс как «диалог» между хозяином и паразитом. Клиническая микробиология и антимикробная химиотерапия 2001;3(4):301-15. [Sidorenko S.V. Infectious process as a «dialog» between host and parasite. Klinicheskaja mikrobiologija i antimikrobnaja himioterapija = Clinical Microbiology and Antimicrobial Chemotherapy 2001;3(4):301-15 (In Russian)].
- Govindarajan DK, Kandaswamy K. Virulence factors of uropathogens and their role in host pathogen interactions. Cell Surf 2022;8:100075. https://doi.org/10.1016/j.tcsw.2022.100075.
- Андрюков Б.Г., Ромашко Р.В., Ефимов Т.А., Ляпун И.Н., Бынина М.П., Матосова Е.В. Механизмы адгезивно-коадгезивного взаимодействия бактерий при формировании биопленки. Молекулярная генетика, микробиология и вирусология 2020;38(4):155–161 [Andryukov B.G., Romashko R.V., Efimov T.A., Lyapun I.N., Bynina M.P., Matosova E.V. Mechanisms of adhesive-coadhesive interaction of bac- teria in the formation of a biofilm. Molekulyarnaya Genetika, Mikrobiologiya i Virusologiya = Molecular Genetics, Microbiology and Virology 2020;38(4):155–61. (In Russian)]. https://doi.org/10.17116/molgen202038041155.
- Wurpel DJ, Beatson SA, Totsika M, Petty NK, Schembri MA. Chaperone-usher fimbriae of Escherichia coli. PLoS One 2013;8(1):e52835. https://doi.org/10.1371/journal.pne.0052835.
- Hartmann M, Papavlassopoulos H, Chandrasekaran V, Grabosch C, Beiroth F, Lindhorst TK, Röhl C. Inhibition of bacterial adhesion to live human cells: activity and cytotoxicity of synthetic mannosides. FEBS Lett 2012;586(10):1459-65. https://doi.org/10.1016/j.febslet.2012.03.059.
- Blumenstock E, Jann K. Adhesion of piliated Escherichia coli strains to phagocytes: differences between bacteria with mannose-sensitive pili andthose with mannose-resistant pili. Infect Immun 1982;35(1):264-26932.
- Hatton NE, Baumann CG, Fascione MA. Developments in Mannose-Based Treatments for Uropathogenic Escherichia coli-Induced Urinary Tract Infections. Chembiochem 2021;22(4):613-29. https://doi.org/10.1002/cbic.202000406.
- Кузьмин И.В., Слесаревская М.Н., Аль-Шукри С.Х. D-манноза в профилактике и лечении инфекций нижних мочевыводящих путей: патогенетические основы и клинические результаты. Урология 2020;(4):131–8. [Kuzmin I.V., Slesarevskaya M.N., Al-Shukri S.H. D-mannose for prevention and treatment of lower urinary tract infection: pathogenetic basics and clinical results. Urologiya = Urologiia 2020;(4):131–8. (In Russian)]. https://doi.org/10.18565/urology.2020.4.131-138.
- de Llano DG, Esteban-Fernández A, Sánchez-Patán F, Martínlvarez PJ, Moreno-Arribas MV, Bartolomé B. Anti-Adhesive Activity of Cranberry Phenolic Compounds and Their Microbial-Derived Metabolites against Uropathogenic Escherichia coli in Bladder Epithelial Cell Cultures. Int J Mol Sci 2015;16(6):12119-30. https://doi.org/10.3390/ijms160612119.







