ВВЕДЕНИЕ
Рак предстательной железы (РПЖ) является одним из наиболее распространенных злокачественных новообразований у мужчин [1]. В Российской Федерации в структуре онкозаболеваемости мужского населения доля РПЖ составляет 14,4%, уступая только злокачественным опухолям трахеи, бронхов и легкого [2]. Основным хирургическим методом лечения больных локализованным РПЖ является радикальная простатэктомия (РПЭ) [3-5]. Совершенствование оперативной техники и широкое внедрение лапароскопических и робот-ассистированных технологий позволили существенно улучшить функциональные и онкологические результаты оперативного вмешательства. Однако, несмотря на это, частота послеоперационных осложнений – недержания мочи (НМ) и эректильной дисфункции, остается весьма значительной. Развитие НМ после РПЭ обусловлено дисфункцией уретрального сфинктера и/или мочевого пузыря [6]. Первая клинически проявляется стрессовым НМ, а вторая – симптомами гиперактивного мочевого пузыря и ургентным НМ. В подавляющем большинстве случаев НМ после РПЭ связано с повреждением уретрального сфинктера и является стрессовым или смешанным. Изолированное ургентное НМ после РПЭ возникает крайне редко, не более чем в 3% случаев [7], а для его лечения рекомендуют антихолинергические препараты [7, 8]. Неспособность удержать мочу существенно ухудшает качество жизни больных [9-11]. Учитывая, что радикальное хирургическое лечение РПЖ обычно проводят пациентам с ожидаемой продолжительностью жизни более 10 лет, НМ представляет собой не только медицинскую, но и значимую социальную проблему.
Непосредственно после удаления уретрального катетера НМ отмечают практически все пациенты, перенесшие РПЭ [12]. В течение года после операции у большинства больных наблюдается восстановление или существенное улучшение способности удерживать мочу, однако у значительного числа пациентов, по разным данным от 7 до 30%, и после этого срока НМ остается значимой проблемой [13, 14]. Первой линией лечения стрессового НМ после РПЭ являются мероприятия, направленные на восстановление функции мышц тазового дна [3, 15]. К ним относят тренировку мышц тазового дна (ТМТД) с или без применения метода биологической обратной связи (БОС), электро- и магнитную стимуляцию тазовой мускулатуры [16-19]. Упражнения для мышц тазового дна являются наиболее простыми и безопасными лечебными методиками и могут выполняться в домашних условиях. При этом эффективность ТМТД оказывается не всегда высокой. Это связано как с неспособностью ряда больных правильно выполнять эти упражнения, так и с зачастую непонятной постановкой задач пациенту медперсоналом. Для повышения эффективности ТМТД в последние годы значительное внимание придается методу БОС [12]. При его использовании пациент с помощью электронных приборов получает информацию о сокращении тазовой мускулатуры. Таким образом, посредством БОС больной в процессе тренировки может самостоятельно контролировать правильность выполнения упражнений, а врач получает возможность оценивать работу различных мышечных групп пациента [20].
В научной литературе нет единого мнения относительно эффективности ТМТД при лечении НМ после РПЭ [16]. Причинами этого являются отсутствие стандартизированной методики проведения упражнений – времени начала выполнения ТМТД после операции, продолжительность курса лечения, частоты тренировок, а также методов оценки эффективности лечения [15]. Также отсутствует консенсус относительно значимости метода БОС при лечении НМ после РПЭ. В этой связи проведение исследований в данном направлении представляются весьма актуальными.
Цель исследования – оценка эффективности ТМТД с использованием метода БОС у больных с НМ после РПЭ.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование были включены 47 мужчин в возрасте от 55 до 72 лет (средний возраст 68,9 лет), которым выполняли лапароскопическую РПЭ по поводу локализованного РПЖ. К моменту включения в исследование (в среднем – через 3,4±1,1 месяца после РПЭ) наблюдаемые больные предъявляли жалобы на НМ в отсутствие позывов на мочеиспускание, что было расценено как стрессовое НМ. У всех пациентов отсутствовали данные за наличие рецидива РПЖ.
Все больные были разделены на две группы, представители которых были сопоставимы по возрасту и степени выраженности НМ. Пациентам 1-й группы (n=24) рекомендовали проводить ТМТД в домашних условиях 3 раза в сутки по 15 мин в течение 6 месяцев. Больные 2-й группы (n=23) также в течение 6-х месяцев проводили ТМТД в домашних условиях, но в течение первого месяца дополнительно выполняли упражнения для тазовых мышц на стационарном аппаратнопрограммном комплексе БОС «Уропроктокор» (НПЦ «Ин Витро», Россия) 1 раз в неделю в течение 40 мин. БОС осуществляли с помощью ректального электромиографического датчика, а также электромиографических электродов для регистрации сократительной активности абдоминальных мышц. Фиксация сокращений брюшной мускулатуры необходима для минимизации ее активности во время ТМТД и облегчения формирования навыка изолированного сокращения тазовых мышц.
Аппаратно-программный комплекс «Уропроктокор» позволяет устанавливать различные режимы тренировок в зависимости от количества, силы, характера и продолжительности сокращений и коэффициента усиления электромиографического сигнала. Во время первого сеанса БОС устанавливали низкий порог сокращения и высокий коэффициент усиления. Затем значения минимальной пороговой силы сокращений увеличивали, а коэффициент усиления снижали. Параметры тренировки подбирали индивидуально в соответствии с результатом первой тестовой тренировки, где оценивали способность пациента сокращать тазовые мышцы, силу сокращений и возможность длительного сокращения. После завершения каждого упражнения в программе аппаратно-программного комплекса высчитывали долю правильно выполненных упражнений. Под контролем врача пациенты выполняли 4 вида упражнений. При выполнении первого упражнения пациент чередовал максимальное сокращение мышц тазового дна с их расслаблением. Это необходимо для идентификации пациентом нужных мышц и определения максимальной силы сокращения. Второе и третье упражнения заключались в постепенном увеличении силы сокращения и таком же плавном расслаблении тазовой мускулатуры. Эти упражнения позволяют обучить больных контролировать силу и длительность сокращения мышц тазового дна. Четвертое упражнение представляло собой длительное сокращение m. levator ani в течение определенного периода времени, обычно начиная с 1 минуты, с последующим его увеличением.
Оценку эффективности лечения проводили по результатам анализа дневников мочеиспускания, которые пациенты заполняли в течение 3-х суток до и после окончания терапии, подсчета количества использованных прокладок в сутки, 1-часового и 24-часового прокладочных тестов (pad-тестов) с измерением объема теряемой мочи и 5-балльной Шкалы субъективной оценки пациентами эффективности лечения. С целью определения функционального состояния уретрального сфинктера пациентам проводили урофлоуметрический тест на прерывание струи мочи. Исследование силы мышц тазового дна выполняли с помощью пальцевой перинеометрии и оценивали в баллах по модифицированной Оксфордской шкале. Согласно последней 0 баллов соответствовало отсутствию ощутимых сокращений; 1 балл – очень слабым мерцающим сокращениям; 2 балла – слабым, но ощутимым сокращениям без визуально заметного движения промежности кпереди; 3 балла – умеренным сокращениям с ощутимым движением мышцы под пальцем и визуально заметным движением промежности кпереди; 4 балла – сокращением, концентрически ощутимым пальцем; 5 баллов – сильным сокращениям с втягиванием пальца. Пальцевую перинеометрию по модифицированной Оксфордской шкале проводил один и тот же врач в течение всего исследования, в которое включали пациентов с силой сокращений от 1 до 5 баллов.
Качество жизни больных оценивали с помощью опросника оценки влияния недержания мочи на качество жизни ICIQ – SF (International Conférence on Incontinence Questionnaire Short Form).
Статистический анализ результатов исследования проводили при помощи компьютерной программы STATISTICA 10,0 с использованием общеупотребительных методов медицинской статистики. Достоверными считали различия при p<0,05.
РЕЗУЛЬТАТЫ
К моменту включения в настоящее исследование у всех пациентов отмечались клинические проявления стрессового НМ. Выраженность НМ у представителей 1-й и 2-й групп была одинаковой (табл. 1). Так, количество используемых прокладок в сутки у пациентов 1-й группы составляло 4,9±1,0, а у пациентов 2-й группы – 4,7±1,1, объем теряемой мочи по данным 1- и 24-часовых pad-тестов составлял соответственно 45,8±18,8 г и 468,3±176,0 г для больных 1-й группы и 47,1±17,9 г и 437,7±143,4 г для больных 2-й группы (p>0,1 для всех пар показателей 1-й и 2 групп). Проведенные тесты показали существенное снижение функциональной способности замыкательного аппарата уретрального сфинктера. Из 47 пациентов только 10 (21,3%) оказались способны прервать струю мочи во время урофлоуметрического теста – 6 пациентов из 1-й и 4 – из 2-й группы. Отмечено значительное снижение силы мышц тазового дна по результатам оценки по шкале Оксфорда. Оценка силы мышц тазового дна у больных 1-й группы составила в среднем 1,8±0,9 баллов, у пациентов 2-й группы – 1,7±1,0 (p>0,1). Анализ результатов анкетирования больных с использованием опросника ICIQ – SF показал выраженное негативное влияние НМ на качество жизни пациентов. Cредние суммы баллов по анкете качества жизни составили 19,4±2,0 и 19,5±1,8 у пациентов 1-й и 2-й групп соответственно (p>0,1). Анализ анкетирования показал значительное влияние НМ на качество жизни пациентов. Средняя сумма баллов по опроснику ICIQ-SF до терапии в 1-й и 2-й группе равнялась 19,5±1,5 (p>0,1).
При контрольном обследовании через 1 месяц от начала исследования отмечено снижение выраженности НМ у больных как 1-й, так и 2-й групп (табл. 1). У пациентов обеих групп достоверно снизились количество используемых прокладок в сутки и объем теряемой мочи по данным 1- и 24-часовых прокладочных тестов. Отмечено также значимое увеличение силы тазовых мышц по шкале Оксфорда. Качество жизни больных, оцениваемое по опроснику ICIQ-SF, достоверно улучшилось только у пациентов 2-й группы (t=2,6; p<0,05). При сравнении исследуемых показателей у пациентов 1-й и 2-й групп через 1 месяц после начала лечения выявлено достоверно меньшее использование прокладок больными 2-й группы (t=2,8; p=0,01). О существенном снижении выраженности НМ сообщили 14 (58,3%) из 24 больных 1-й группы и 19 (82,6%) из 23 пациентов 2-й группы (рис. 1). Через 1 месяц после начала исследования 17 (73,9%) пациентов 2-й группы оказались способны прервать поток мочи, тогда как в 1-й группе таких пациентов было только 11 (45,8%). Больные, которые наряду с ТМТД в домашних условиях проводили тренировки с использованием БОС, более высоко оценили эффективность проводимого лечения. Об этом свидетельствовали результаты субъективной оценки пациентами эффективности лечения по 5- балльной шкале. Значение данного показателя в 1-й группе составило 2,8±1,1 балла, а во 2-й группе – 3,6±0,9 балла (t=2,5; p<0,05).
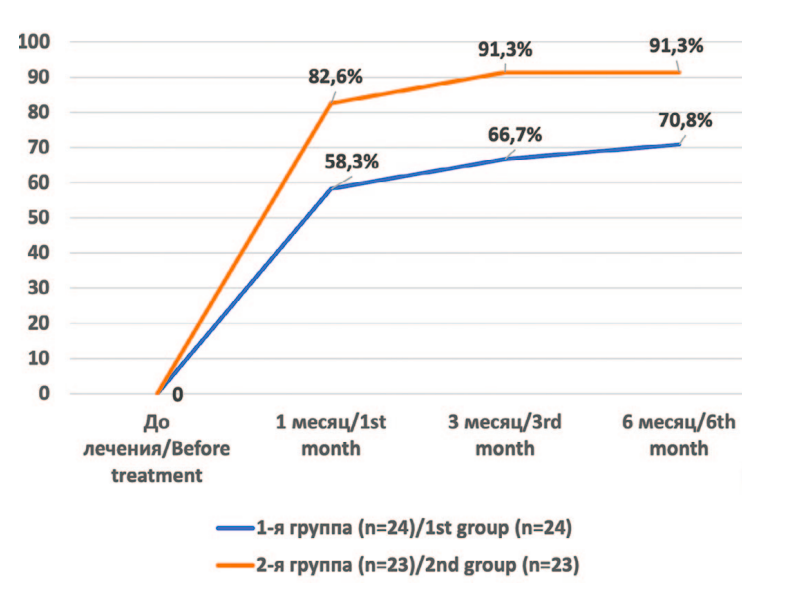
Рис. 1. Доля больных 1-й и 2-й групп, указавших на снижение выраженности
НМ в процессе лечения
Fig. 1. Percentage of patients in groups 1 and 2 who indicated a decrease in the
severity of UI during treatment
Таблица 1. Динамика клинических показателей у больных с НМ после РПЭ (M±σ)
Table 1. Dynamics of clinical parameters in patients with UI after LRP (M±σ)
|
Показатели |
1-я группа (n=24) 1st group (n=24) |
2-я группа (n=23) 2nd group (n=23) |
||
|---|---|---|---|---|
|
До лечения |
Через 1 месяц после начала лечения |
До лечения |
Через 1 месяц после начала лечения |
|
|
Среднее количество прокладок в сутки, шт. |
4,9±1,0 |
3,6±0,9 |
4,7±1,1 |
2,9±0,9 |
|
Объем теряемой мочи (1-часовой pad-test), г |
45,8±18,8 |
3,6±0,9 |
47,1±17,9 |
26,1±11,7 |
|
Объем теряемой мочи (24-часовой pad-test), г |
468,3±176,0 |
311,1±137,3 |
437,7±143,4 |
284,7±136,5 |
|
Сила мышц тазового дна по шкале Оксфорда, баллы |
1,8±0,9 |
2,7±1,1 |
1,7±1,0 |
2,9±1,1 |
|
Сумма баллов по анкете качества жизни ICIQ-SF, баллы |
19,4±2,0 |
18,1±2,2 |
19,5±1,8 |
16,4±2,1 |
Примечание: *по сравнению с показателем до лечения; **по сравнению с показателем в 1-й группе
Note: *in comparison with the parameter before treatment; **compared with the parameter in the 1st group
У больных 2-й группы на каждом еженедельном сеансе БОС с помощью программно-аппаратного комплекса оценивали правильность выполнения всех 4-х упражнений для тазовых мышц (табл. 2). Отмечено, что наиболее сложным для больных оказалось выполнять упражнение 2, заключающееся в постепенном увеличении силы сокращения тазовых мышц. Во время 1-го сеанса БОС-терапии доля правильно выполненных упражнений данного типа составила только 67,3%. К окончанию БОС-терапии, во время 4-го сеанса, отмечено существенное повышение доли правильно выполняемых упражнений. Данное наблюдение указывает на приобретение пациентами навыка изолированного сокращения мышц тазового дна и способности контролировать сокращения тазовой мускулатуры, что является важным фактором восстановления перинеального рефлекса. К окончанию 1-го месяца лечения навык изолированного сокращения мышц тазового дна приобрели 17 (73,9%) пациентов 2-й группы. Именно у этих больных эффективность лечения НМ оказалась наиболее высокой. Остальным 6 пациентам 2-й группы продолжили проведение БОС-терапии в режиме 1 сеанс каждые 2 недели.
К 3-му месяцу наблюдения у 16 (66,7%) пациентов 1-й группы отмечено улучшение, у 8 (33,3%) пациентов – изменений выраженности НМ не было. Из 23 пациентов 2-ой группы у 5 (21,7%) с навыком изолированных сокращений наблюдалось восстановление удержания мочи, у 16 (69,6%) – улучшение, включая тех, кто продолжил тренировки с помощью БОС и у 2 (8,7%) пациентов изменений не отмечено (рис. 1). При контрольном обследовании через 6 месяцев от начала исследования из 24 пациентов, которые выполняли ТМТД самостоятельно в домашних условиях, у 17 (70,8%) пациентов наступило улучшение, а у 7 (29,2%) пациентов – изменений не было. Из 23 пациентов 2-й группы, которым наряду с ТМТД назначала БОС-терапию, у 9 (39,1%) НМ исчезло полностью, у 12 (52,2%) отмечено значимое улучшение и только у 2 (8,7%) пациентов снижения выраженности НМ не наблюдали.
Пациенты хорошо переносили лечение НМ. Ни у одного больного 1-й и 2-й групп не отмечено побочных эффектов терапии. Также ни в одном случае лечение не прерывалось и досрочно не прекращалось.
ОБСУЖДЕНИЕ
Известно, что в механизме удержания мочи у мужчин принимают участие два сфинктера — проксимальный (препростатический) и дистальный [21]. Проксимальный сфинктер состоит из гладкомышечных волокон, которые охватывают простатический отдел уретры от шейки мочевого пузыря до семенного бугорка. Дистальный сфинктер (рабдосфинктер) представлен поперечнополосатыми мышечными волокнами, относящимися к лобково-копчиковой мышце. Во время РПЭ препростатический сфинктер удаляется, поэтому основная роль в удержании мочи принадлежит дистальному уретральному сфинктеру. В его состав входят поперечно-полосатые мышечные волокна двух типов. Волокна I типа («медленные» или тонические) обеспечивают тонус сфинктера в фазе наполнения микционного цикла и расслабляются только в момент инициации мочеиспускания. Ко II типу относятся так называемые «быстрые» мышечные волокна, которые осуществляют сильные кратковременные сокращения в ответ на резкое повышение внутрибрюшного давления, что обеспечивает резкое увеличение внутриуретрального давления и удержание мочи [22]. Выполнение РПЭ сопровождается нарушением замыкательного механизма наружного сфинктера, что может приводить к НМ. Установлено, что вероятность развития НМ после РПЭ зависит не только от техники оперативного вмешательства, но и от ряда других факторов: возраста больного, общесоматического статуса, исходного нарушения функции нижних мочевыводящих путей и тазового дна. Несмотря на то, что в патогенезе НМ после РПЭ преобладает уретральная составляющая, определенный вклад в его развитие вносит и нарушение функции мочевого пузыря, наблюдаемое, по разным оценкам, у 8–38,9% больных, перенесших РПЭ [6, 23].
Таблица 2. Результаты выполнения упражнений для тазовых мышц пациентами 2-й группы (доля правильно выполненных упражнений, в %)
Table 2. The results of performing exercises for the pelvic muscles by patients of the 2nd group (the proportion of correctly
performed exercises, in%)
|
1-й сеанс (1-я неделя лечения |
4-й сеанс (4-я неделя лечения |
|
|---|---|---|
|
Упражнение 1 |
76,9 % |
87,0 % |
|
Упражнение 2 |
67,3 % |
75,6 % |
|
Упражнение 3 |
81,2 % |
86,3 % |
|
Упражнение 4 |
95,0 % |
98,6 % |
Укрепление тазовых мышц в настоящее время рассматривается как патогенетически обоснованный метод лечения НМ после РПЭ [17]. Повреждения мышечных волокон тазового дна при оперативных вмешательствах связано с их денервацией с последующей атрофией денервированных мышечных волокон. При ТМТД жизнеспособные нервные волокна способны стимулировать реиннервацию и в этом случае часть быстросократимых волокон трансформируются в медленносократимые (I типа), что способствует восстановлению функции наружного уретрального сфинктера и тазового дна в целом [22]. Предложено множество методик ТМТД, при этом большинство из них включает упражнения для укрепления разных мышечных волокон: длительные статические сокращения m.levator ani (волокна I типа) и быстрые сильные сокращения этой мышцы (волокна II типа). Помимо указанных типов сокращений ряд методик включает в себя так называемые «интенсивные» сокращения путем плавного постепенного усиления тонуса m.levator ani в течении определенного времени до максимально возможного уровня с последующим таким же постепенным ее расслаблением [24]. В последние годы большинство авторов рекомендуют начинать ТМТД в раннем послеоперационном периоде непосредственно после удаления уретрального катетера в стационаре и затем продолжать после выписки в домашних условиях [15]. Однако многие больные (от 40 до 60%) не в состоянии самостоятельно корректно осуществлять тренировку тазовых мышц [22]. Вместо того, чтобы изолированно сокращать m. levator ani, эти пациенты сокращают другие мышечные группы, чаще всего прямую мышцу живота, что приводит к повышению внутрибрюшного давления. В таких случаях ТМТД не только не оказывает лечебного эффекта, но и может усилить НМ вследствие повышенной нагрузки на тазовое дно. Для решения данной проблемы было предложено использовать метод БОС. Основной задачей данного метода при лечении больных с НМ является обучение пациентов правильному выполнению упражнений, приобретение ими навыка изолированного сокращения тазовых мышц и восстановление перинеального рефлекса – увеличения внутриуретрального давления в ответ на повышение внутрибрюшного за счет быстрого сокращения тазовой мускулатуры [20]. К настоящему времени во многих исследованиях показано, что комбинация ТМТД и БОСтерапии является методом выбора для пациентов с НМ после РПЭ [13, 25]. Наиболее часто БОС проводят с помощью электромиографических ректальных датчиков, однако в ряде исследований с этой целью успешно использовали манометрические и ультразвуковые ректальные датчики [26]. Применение БОС существенно повышает эффективность ТМТД. Об этом свидетельствуют результаты исследований как зарубежных, так и отечественных специалистов [12, 13, 25-28].
A. Sciarra и соавт. представили результаты систематического обзора и метаанализа 26 публикаций, свидетельствующие о большей эффективности ТМТД в сочетании с БОС или электростимуляцией тазовых мышц по сравнению с выполнением ТМТД в монорежиме, особенно в период первых 3 месяцев после операции (р<0,01), в то время как в период 6 и 12 месяцев после операции различие в результатах лечения было менее явным [12]. Представленные данные указывают на целесообразность раннего начала комбинированного консервативного лечения НМ после РПЭ.
Полученные нами результаты также свидетельствует об эффективности БОС-терапии у пациентов с НМ после РПЭ. Уже к концу первого месяца лечения у пациентов, которым было проведено 4 еженедельных сеансов БОС, отмечены лучшие клинические результаты по сравнению с пациентами, выполнявшими ТМТД только в домашних условиях. Проведение БОСтерапии способствовало более быстрому восстановлению удержания мочи и улучшению качества жизни больных. Формирование навыка правильного выполнения упражнений для тазовых мышц увеличивало эффективность тренировок, что сопровождалось повышением силы сокращений тазовых мышц. Несмотря на высокую эффективность БОС-терапии, ее широкое использование на сегодняшний день еще ограничено. Это связано как с недостаточным количеством аппаратов БОС, так и с отсутствием единых стандартов выполнения ТМТД с помощью БОС. Последнее обстоятельство затрудняет сравнение результатов клинических исследований между собой. В этой связи весьма актуальной представляется разработка общих протоколов тренировок с определением их периодичности, временных характеристик сокращения и расслабления мышц, числа повторений в день и т.д.
ЗАКЛЮЧЕНИЕ
Проведенное исследование показало высокую эффективность ТМТД в сочетании с методом БОС при лечении НМ после РПЭ. Данная методика при работе с квалифицированным специалистом помогает пациентам приобрести навык правильного выполнения упражнений для тазовых мышц, что способствует более быстрому восстановлению функции сфинктерного аппарата уретры, исчезновению или уменьшению выраженности НМ и улучшению качества жизни больных. Применение БОС-терапии при НМ после РПЭ является патогенетически оправданным методом лечения данной категории пациентов. Представляется целесообразным более широкое внедрение данного метода в практическую медицину, а также использование данного метода в обучении пациентов правильным упражнениям для тазовых мышц перед выполнением РПЭ.
ЛИТЕРАТУРА
1. Pernar CH, Ebot EM, Wilson KM, Mucci LA. The Epidemiology of prostate cancer. Cold Spring Harb Perspect Med 2018;8(12):a030361. https://doi.org/10.1101/ cshperspect.a030361.
2. Злокачественные новообразования в России в 2017 году (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой; М.: МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России 2018;250 с. [Malignant neoplasms in Russia in 2017 (morbidity and mortality). Edited by A.D. Kaprin, V.V. Starinskij, G.V. Petrova; Moscow.: P.A. GercenMNIOI – filial FGBU «NMIC radiologii» Minzdrava Rossii 2018;250 p. (In Russian)].
3. Министерство здравоохранения Российской федерации. Клинические рекомендации «Рак предстательной железы» 2021. [Ministry of Health of the Russian Federation. Clinical recommendations «Prostate cancer» 2021. (In Russian)]. URL: https://cr.minzdrav.gov.ru/schema/12_3#doc_a1.
4. Mottet N, Bellmunt J, Bolla M, Briers E, Cumberbatch MG, De Santis M, et al. EAU-ESTRO-SIOG Guidelines on prostate cancer. Part 1: Screening, diagnosis, and local treatment with curative intent. Eur Urol 2017;71(4):618–629. https://doi.org/10.1016/j.eururo.2016.08.003.
5. Петров С.Б., Велиев Е.И. Хирургическое лечение локализованных форм рака предстательной железы. Практическая онкология 2001;(2):50–52. [Petrov S.B., Veliev E.I. Surgical treatment of localized forms of prostate cancer. Prakticheskaya onkologiya = Practical Oncology 2001;(2):50–52. (In Russian)].
6. Majoros A, Bach D, Keszthelyi A, Hamvas A, Romics I. Urinary incontinence and voiding dysfunction after radical retropubic prostatectomy (prospective urodynamic study). Neurourol Urodyn 2006;25(1):2-
7. https://doi.org/10.1002/ nau.20190. 7. Pastore AL, Palleschi G, Illiano E, Zucchi A, Carbone A, Costantini E. The role of detrusor overactivity in urinary incontinence after radical prostatectomy: a systematic review. Minerva Urol Nefrol 2017;69(3):234-241. https://doi.org/10.23736/S0393-2249.16.02790-9.
8. Кузьмин И.В., Кузьмина С.В. Антихолинергическая терапия гиперактивного мочевого пузыря: практические аспекты. РМЖ. Медицинское обозрение 2021;5(5):273–279. [Kuzmin I.V., Kuzmina S.V. Anticholinergic therapy of an overactive bladder: clinical practice aspects. RMJ. Medicinskoe Оbozrenie = RMJ. Russian Medical Inquiry 2021;5(5):273–279. (In Russian)]. https://doi.org/10.32364/2587-6821-2021-5-5-273-279.
9. Sarikaya S, Yildiz FG, Senocak C, Bozkurt OF, Karatas OF. Urinary incontinence as a cause of depression and sexual dysfunction: Questionnairebased study. Rev Int Androl 2020;18(2):50-54. https://doi.org/10.1016/ j.androl.2018.08.003.
10. Вагайцева М.В., Караваева Т.А., Васильева А.В., Чулкова В.А., Носов А.К. Психологические механизмы формирования отношения к заболеванию у больных раком предстательной железы после радикальной простатэктомии. Урологические ведомости 2018;8(3):53-66. [Vagaytseva M.V., Karavaeva T.A., Vasileva A.V., Chulkova V.A., Nosov A.K. Psychological mechanisms in the formation of attitude toward the disease among patients with prostate cancer after radical prostatectomy. Urologicheskie Vedomosti = Urology Reports 2018;8(3):53-66. (In Russian)]. https://doi.org/10.17816/uroved8353-66.
11. Аль-Шукри С.Х., Кузьмин И.В. Качество жизни больных с гиперактивностью мочевого пузыря. Урологические ведомости 2011;1(1):21–26. [AlShukri SH, Kuzmin IV. Quality of life in patients with overactive bladder. Urologicheskie Vedomosti = Urology Reports 2011;1(1):21-26. (In Russian)].
12. Sciarra A, Viscuso P, Arditi A, Mariotti G, De Berardinis E, Di Pierro GB, et al. A biofeedback-guided programme or pelvic floor muscle electric stimulation can improve early recovery of urinary continence after radical prostatectomy: A meta-analysis and systematic review. Int J Clin Pract 2021;75(10):e14208. https://doi.org/10.1111/ijcp.14208.
13. Демидко Ю.Л., Глыбочко П.В., Винаров А.З., Рапопорт Л.М., Чалый М.Е., Ахвледиани Н.Д. и др. Лечение недержания мочи после радикальной простатэктомии с применением тренировки мышц таза под контролем биологической обратной связи. Урология 2015;(1):41-43. [Demidko Yu.L., Glybochko P.V., Vinarov A.Z., Rapoport L.M., Chaly M.E., Akhvlediani N.D., et al. Treatment of urinary incontinence after radical prostatectomy using training of pelvic muscles under the control of biofeedback. Urologiia = Urologya 2015;(1):41-43. (In Russian)].
14. Chang JI, Lam V, Patel MI. Preoperative pelvic floor muscle exercise and postprostatectomy incontinence: a systematic review and meta-analysis. Eur Urol 2016;69(3):460-7. https://doi.org/10.1016/j.eururo.2015.11.004.
15. Ma ZZ, Zhang HB, Niu ME, Ding YH, Zhou Y, Yang Q, et al. Construction of pelvic floor muscle rehabilitation training program for patients undergoing laparoscopic radical prostatectomy. Transl Cancer Res 2022;11(2):392-402. https://doi.org/10.21037/tcr-21-2738.
16. Anderson CA, Omar MI, Campbell SE, Hunter KF, Cody JD, Glazener CM. Conservative management for postprostatectomy urinary incontinence. Cochrane Database Syst Rev 2015;1(1):CD001843. https://doi.org/10.1002/14651858.CD001843.pub5.
17. Лебединец А.А., Школьник М.И. Патофизиологическое обоснование эффективности консервативной немедикаментозной терапии недержания мочи после радикальной простатэктомии. Вопросы онкологии 2013;59(4):435-443. [Lebedinec A.A., SHkol'nik M.I. Pathophysiological substantiation of the effectiveness of conservative non-drug therapy of urinary incontinence after radical prostatectomy. Voprosy onkologii = Issues of Oncology 2013;59(4):435-443. (In Russian)]. https://doi.org/10.37469/0507- 3758-2013-59-4-435-443.
18. Аль-Шукри С.Х., Ананий И.А., Амдий Р.Э., Кузьмин И.В. Электростимуляция мышц тазового дна в лечении больных с недержанием мочи после радикальной простатэктомии. Урологические ведомости 2016;6(4):10-13. [Al-Shukri S.K., Ananiy I.A., Amdiy R.E., Kuzmin I.V. Electrical stimulation of the pelvic floor in the treatment of patients with urinary incontinence after radical prostatectomy. Urologicheskie Vedomosti = Urology Reports 2016;6(4):10-13. (In Russian)]. https://doi.org/10.17816/ uroved6410-13.
19. Амдий Р.Э., Аль-Шукри С.Х., Кузьмин И.В., Макеев В.А., Созданов П.В. Экстракорпоральная магнитная стимуляция в урологии. Урологические ведомости 2021;11(4):345-353. [Amdiy R.E., Al-Shukri S.K., Kuzmin I.V., Makeev V.A., Sozdanov P.V. Extracorporeal magnetic stimulation in urology. Urologicheskie Vedomosti = Urology Reports 2021;11(4):345-353. (In Russian)]. https://doi.org/10.17816/uroved84474.
20. Кротова Н.О., Кузьмин И. В., Улитко Т. В. Метод биологической обратной связи в лечении и реабилитации женщин с недержанием мочи. Вестник восстановительной медицины 2020;6(100):57–65. [Krotova N.O., Kuzmin I.V., Ulitko T.V. Biofeedback in Treatment and Rehabilitation of Urinаry Incontinence in Women. Vestnik Vosstanovitel'noj Mediciny = Bulletin of Rehabilitation Medicine 2020;6(100):57–65. (In Russian)]. https://doi.org/10.38025/2078-1962-2020-100-6-57-65.
21. Perucchini D, DeLancey JOL. Functional anatomy of the pelvic floor and lower urinary tract. In: Baessler K, Burgio KL, Norton PA, Schüssler B, Moore KH, Stanton SL. (eds) Pelvic Floor Re-education. Springer, London 2008;3-21. https://doi.org/10.1007/978-1-84628-505-9_1.
22. Bourcier A.P., Juras J.C. Kinesitherapie pelvi-perineale. Urodynamique et Readaptation en Urogynecologie 1986; Paris, Vigot.
23. Голубцова Е.Н., Томилов А.А., Велиев Е.И. Современное состояние проблемы недержания мочи после радикальной простатэктомии. Consilium Medicum 2017;19(7):8–14. [Golubcova E.N., Tomilov A.A., Veliev E.I. The current state of the problem of urinary incontinence after radical prostatectomy. Consilium Medicum 2017;19(7):8–14. (In Russian)]. https://doi.org/10.26442/2075-1753_19.
24. Кротова Н.О., Улитко Т.В., Кузьмин И.В., Аль-Шукри С.Х. Метод биологической обратной связи в лечении пациентов с недержанием мочи после радикальной простатэктомии. Урологические ведомости 2021;11(1):69-78. [Krotova N.O., Ulitko T.V., Kuzmin I.V., Al-Shukri S.K. Biofeedback in the treatment of patients with urine incontinence after radical prostatectomy. Urologicheskie Vedomosti = Urology Reports 2021;11(1):69-78. (In Russian)]. https://doi.org/10.17816/uroved63508.
25. Kim YU, Lee DG, Ko YH. Pelvic floor muscle exercise with biofeedback helps regain urinary continence after robot-assisted radical prostatectomy. Yeungnam Univ J Med 2021;38(1):39-46. https://doi.org/10.12701/ yujm.2020.00276.
26. Matsunaga A, Yoshida M, Shinoda Y, Sato Y, Kamei J, Niimi A, et al. Effectiveness of ultrasound-guided pelvic floor muscle training in improving prolonged urinary incontinence after robot-assisted radical prostatectomy. Drug Discov Ther 2022;16(1):37-42. https://doi.org/10.5582/ddt.2022.01004.
27. Винаров А.З., Рапопорт Л.М., Крупинов Г.Е., Демидко Ю.Л., Цариченко Д.Г., Безруков Е.А. и др. Результаты тренировки мышц тазового дна под контролем биологической обратной связи пациентов с недержанием мочи после лапароскопической и робот-ассистированной радикальной простатэктомии. Онкоурология 2018;14(2):102-108. [Vinarov A.Z., Rapoport L.M., Krupinov G.E., Demidko YU.L., Carichenko D.G., Bezrukov E.A., et al. Results of pelvic floor muscle training under the control of biofeedback of patients with urinary incontinence after laparoscopic and robot-assisted radical prostatectomy. Onkourologiya = Cancer Urology 2018;14(2):102-108. (In Russian)]. https://doi.org/10.17650/1726-9776-2018-14-2-102-108.
28. Аляев Ю.Г., Рапопорт Л.М., Безруков Е.А., Цариченко Д.Г., Демидко Л.С., Винаров А.З. и др. Результаты тренировки мышц тазового дна под контролем биологической обратной связи при недержании мочи после радикальной простатэктомии. Андрология и генитальная хирургия 2011;12(4):61-65. [Alyaev YU.G., Rapoport L.M., Bezrukov E.A., Carichenko D.G., Demidko L.S., Vinarov A.Z., et al. Results of pelvic floor muscle training under the control of biofeedback for urinary incontinence after radical prostatectomy. Andrologiya i genital'naya hirurgiya = Andrology and Genital Surgery 2011;12(4):61-65 (In Russian)].







