ВВЕДЕНИЕ
Сегодня ультразвуковое исследование (УЗИ) за счет целого ряда преимуществ перед другими диагностическими методами (небольшая стоимость, отсутствие ионизирующего излучения, возможность выполнения без ограничения по возрасту, полу, массе тела, наличия металлических предметов и др.) широко внедрено в клиническую практику. Однако точность данных, получаемых в ходе УЗИ, вариабельна и зависит от опыта специалиста, выполняющего исследование, и качества УЗ-аппарата [1]. При обнаружении камней мочевых путей диапазон диагностической точности варьирует от 33% до 95%, а при камнях менее 5 мм он не выше 32% [2].
Одним из способов повышения точности УЗИ в обнаружении камней органов мочевыделительной системы является артефакт мерцания (twinkling artefact), представляющий собой скопления быстро меняющихся окрашенных различными цветами пикселей (желтые, голубые, зеленые и др.), появляющихся в зоне твердых структур, чаще всего камнях, кальцинатах, инородных телах [3].
Природа артефакта мерцания (АМ) на сегодняшний день изучена не полностью. На сегодняшний день основной причиной возникновения данного явления считается взаимодействие ультразвука с микропузырьками на поверхности камня, а также упругие колебания твердого включения небольших размеров относительно датчика, проявляющихся хаотичным расширением допплеровского спектра [4].
Долгое время АМ считался именно артефактом, т.е. ложным отображением анатомической структуры или искажением на изображении, получаемом с помощью различных методов лучевой диагностики [5]. Однако, начиная с 2001 года, согласно запросу в базу данных PubMed, интерес к изучению данного явления стал прогрессивно увеличиваться.
Несмотря на то, что в обнаружении мочевых камней АМ известен на протяжении почти 30 лет, врачи ультразвуковой диагностики, а также урологи редко используют его в своей практике [6, 7]. Одной из причин является значительное различие данных о диагностической точности АМ в выявлении камней мочевых путей – она варьирует от 50% до 97% в различных исследованиях [8]. Это может быть связано с методическими особенностями проведения научных исследований, а также с техническими особенностями конкретного УЗИ-аппарата. Практический опыт последних десятилетий показал, что АМ хорошо проявлялся на цифровых ультразвуковых аппаратах первых поколений, в дальнейшем, по не совсем понятной причине, стал обнаруживаться значительно реже. Одной из версий этого, является разработка и оснащение ультразвуковых аппаратов программными средствами подавления различных артефактов, в число которых попали и допплеровские артефакты. Однако использование ультразвуковых аппаратов, разработанных в последнее десятилетние, показало возможность получения очень выраженного АМ на них. Таким образом, парк ультразвуковых аппаратов в настоящее время состоит из приборов, в которых легко получить АМ и аппаратов, на которых нет смысла ждать появления цветового мерцания в области мочевых камней. Это определяет необходимость разработки методики тестирования УЗИ-аппарата на предмет определения возможности использовать АМ на нем. Кроме того, известно, что для получения значимого АМ необходимы определенные настройки УЗ-сканера, некоторые из которых индивидуальны для конкретного аппарата, что определяет целесообразность наличия устройства для настройки сканера без привлечения пациентов или добровольцев.
Цель: разработка специального устройства для тестирования и настройки ультразвукового сканера на получение значимого АМ для его дальнейшего использования в обнаружении мочевых камней.
МАТЕРИАЛЫ И МЕТОДЫ
В 2023 году сотрудниками НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России и Московского государственного технического университета им. Н.Э. Баумана проведена серия экспериментов, и разработано устройство (фантом), позволяющее исследовать АМ в лабораторных условиях. Для тестирования устройства в процессе разработки использовались УЗИаппараты: Philips Affinity 70 и ALOKA Ultrosound F75. Для испытания рабочих свойств устройства проведена оценка возможности получения АМ на ряде ультразвуковых сканеров: BK Specto 5000, Simens, Samsung RS65, Samsung Rs 85, Mindrey Kesona, Hitachi Arienta 750.
В качестве исследуемого материала использовались фрагменты мочевых камней различного химического состава, состоящие на 70% и более процентов из мочевой кислоты, кальций-оксалата, кальций-фосфата, струвита, а также искусственно приготовленного дигидрата сульфата кальция (гипс). Диаметр фрагментов камней составил <5 мм, а в качестве контактной среды использовались ультразвуковой гель, дегазированная минеральная и водопроводная вода.
РЕЗУЛЬТАТЫ
В ходе предварительной работы выявили, что АМ мочевого камня можно получить в пластиковом контейнере объемом 200 мл, шириной 10 см, высотой 5 см, в который погружена силиконовая подложка, применяющаяся для отработки лапароскопического интракорпорального шва. В углубление подложки помещали фрагмент мочевого камня (кальций – фосфат), а в качестве контактной среды использовали дегазированную воду. Для исследования использовали аппарат Philips Affinity 70 с линейным УЗ-датчиком 5-15 мГЦ (рис. 1).
Как видно из рисунка 1Б, на вершине силиконовой подложки визуализируется АМ, соответствующий мочевому камню (рис. 1А). При включении импульсно-волнового режима отмечали колебания высокой амплитуды и хрустящий звук в динамиках ультразвукового аппарата, что подтверждало наличие в зоне интереса структуры высокой плотности (рис. 1В). При смещении ультразвукового датчика вне зоны локализации камня АМ, колебания высокой амплитуды и хрустящий звук пропадали.
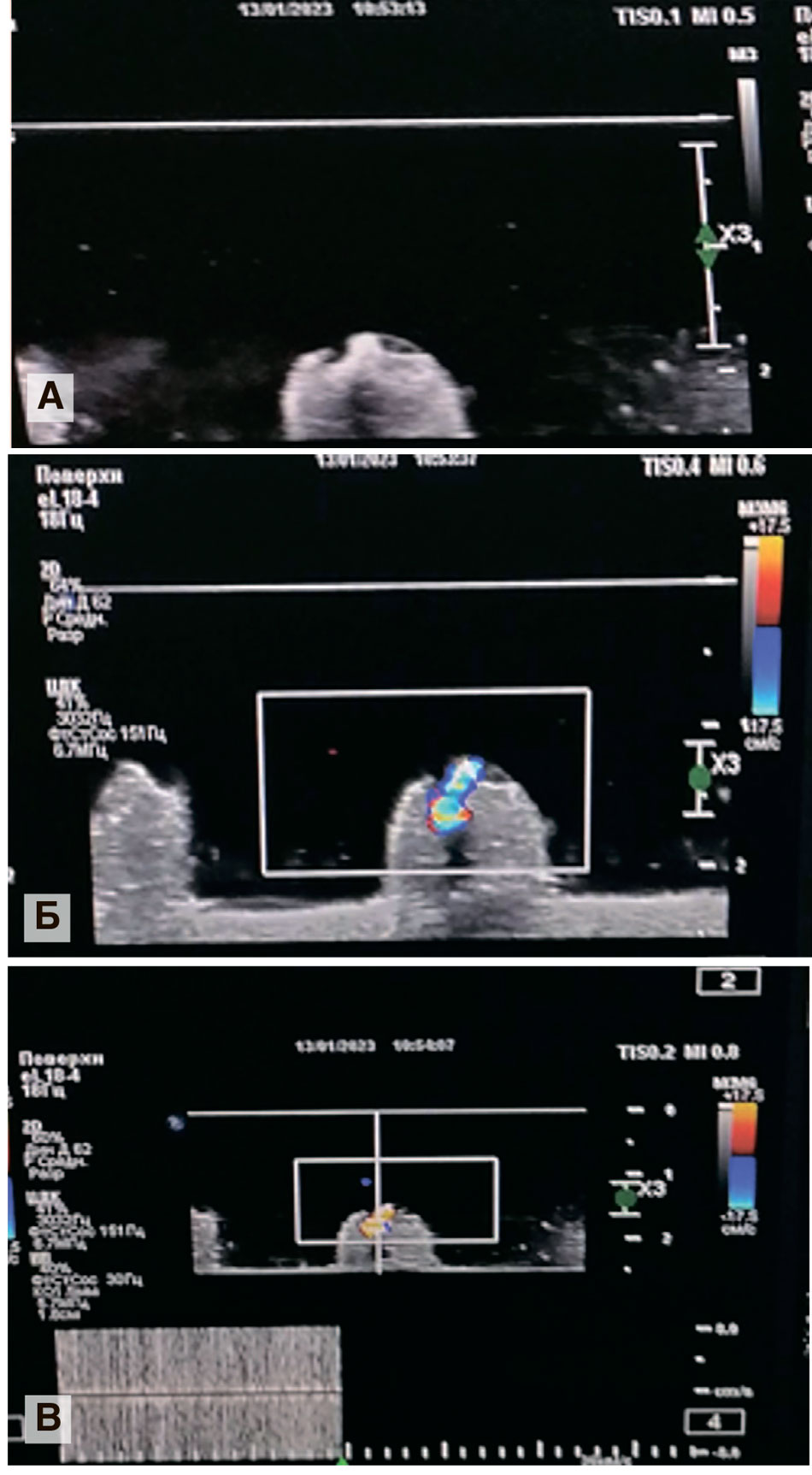
Рис. 1. Артефакт мерцания мочевого камня 5 мм (кальций-оксалат моногидрат 100%) в дегазированной воде, полученный на УЗ-аппарате Philips Affinity 70, линейным датчиком 5-15 мГц: А) серо-шкальный режим, Б) режим ЦДК, В) импульсно-волновой режим
Fig. 1. 5 mm urinary calculus twinkling artifact (calcium oxalate monohydrate 100%) in degassed water, obtained on a Philips Affinity 70 ultrasonic device with a 5-15 MHz linear sensor: A) gray-scale mode, Б) CDK mode, В) pulse-wave mode
Подобные исследования проведены с камнями различного химического состава, при этом нам удалось зарегистрировать АМ в области всех камней, в том числе и искусственно приготовленном из дигидрата сульфата кальция (гипса) (рис. 2).
Однако такой подход требовал постоянной фокусировки ультразвуковой волны на мочевом конкременте, что отвлекало и затрудняло подбор оптимальных настроек режима допплеровского картирования для лучшей визуализации АМ, появилось понимание в необходимости наличия в устройстве системы фиксации датчика.
При разработке подложки было испытано несколько вариантов силикона на основе платины и олова, определяли необходимую высоту подложки, а также способ фиксации камня. Для определения материала подложки и фиксации конкремента на ней было изготовлено несколько прототипов, которые помещали в контейнер с дегазированной минеральной водой. Установлено, что оптимальным материалом для подложки является силикон на основе платины, что позволило фиксировать конкременты, не заливая их силиконом, а помещая в углубление диаметром 5 мм и глубиной 3 мм.
При разработке фиксирующего компонента устройства определяли вид зажима и механизм фиксации. Были исследованы следующие виды зажимов: винтовой, разъемный и пружинный. Апробация установила, что зажим должен быть выполнен из пластика, быть разъемным, с фиксатором, а механизм, приводящий в действие, может быть в виде зубчатого соединения, приводящегося в движение посредством червячной передачи.
В итоге было разработано устройство, представляющее собой пластиковый контейнер 4*10*5 см, с толщиной боковых стенок 0,2 см (рис. 3 А-В). Внутрь устройства помещена подложка, сделанная из силикона на основе платины, размером 10*5*2 см (рис. 3Г). По центральной линии подложки на расстоянии 2 см друг от друга располагаются 3 углубления для фиксации конкремента диаметром <5 мм. Для предотвращения миграции ультразвукового датчика во время исследования предусмотрена система фиксации в виде 2-х зажимов, расположенных в верхней части контейнера, соединенных друг с другом посредством зубчатого соединения. Изменение диаметра фиксации производится поворотом винтового колеса: уменьшение – по часовой стрелке, увеличение – против часовой стрелки. Для предотвращения повреждения ультразвукового датчика на последний одевали латексный презерватив для ультразвуковой диагностики, предварительно заполненный небольшим количеством геля для УЗИ.
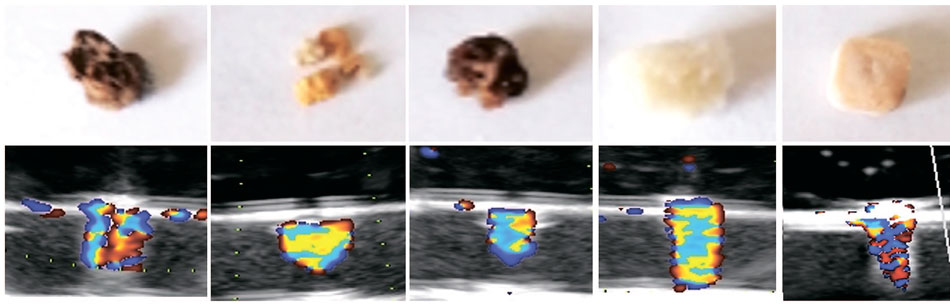
Fig. 2. An artifact of the twinkling of stones of various chemical compositions: A) calcium oxalate, B) uric acid, C) calcium phosphate, D) struvite, E) calcium sulfate dihydrate was obtained on a ultrasonic device – Philips Affinity 70 device with a 2-7.5 MHz convexic sensor

Рис. 3. Устройство для лабораторной оценки артефакта мерцания (фантом): А – вид спереди, Б – вид сбоку, В – вид сверху, Г – силиконовая подложка с размещенными 3-мя камнями различного химического состава
Fig. 3. Device for laboratory evaluation of the flicker artifact (phantom): A – front view, Б – side view, В – top view, Г – silicone substrate with 3 stones of different chemical composition placed
В рамках апробации разработанного фантома первым этапом определили возможность визуализации АМ в различных контактных средах. Учитывая результаты предварительных исследований, в ходе которых мы выявили, что АМ определяется во всех исследуемых фрагментах камней, дальнейшее исследование проводили только с использованием дигидратасульфата кальция (гипс) размером 5 мм, помещенного в центральную лунку силиконовой подложки. После этого контейнер заполняли различными контактными средами, устанавливали конвексный датчик 3,5 мГц в зажиме и в режиме серошкального сканирования визуализировали камень (гиперэхогенное включение с акустической тенью). После этого фиксировали датчик и включали допплеровский режим картирования.
Изначально при заводских настройках ультразвуковых аппаратов мы отметили сильное свечение, затрудняющее визуализацию АМ (рис. 4А, В). После внесения изменений в настройки, согласно рекомендациям по использованию мерцающего артефакта для выявления твердых включений в ультразвуковой диагностике [4], добились свечения АМ только в зоне исследуемого конкремента.
Мы выяснили, что для адекватной визуализации АМ в фантоме достаточно использовать следующие настройки:
- увеличение мощности передатчика до максимальной (power 100%),
- увеличение частоты повторения импульсов (PRF) до максимальных значений,
- уменьшение размера цветового окна (color box) до 5 см (ширина) * 2 см (высота),
- установление цветового окна в зону локализации мочевого конкремента,
- установление фокуса (focus) в область локализации конкремента.
Следующим этапом исследования было изучение АМ в различных контактных средах: водопроводная вода и гель для УЗИ (рис. 5).
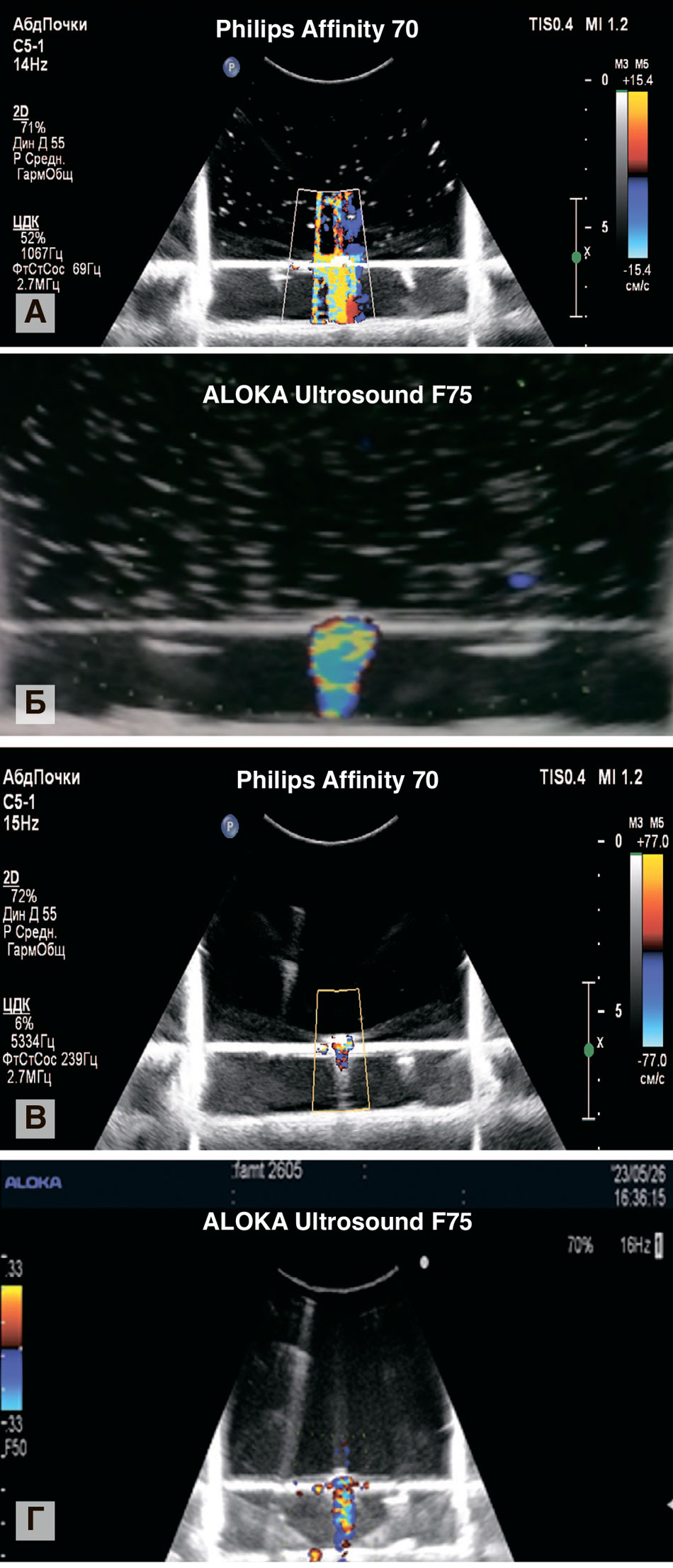
Рис. 4. Артефакт мерцания дигидрата сульфата кальция, полученный на УЗ-аппаратах Philips Affinity 70 (А, В), ALOKA Ultrosound F75 (Б, Г): А, Б – до настроек режима допплеровского картирования, В, Г – после настроек
Fig. 4. Calcium sulfate dihydrate twinkling artifact obtained on Philips Affinity 70 (A, В), ALOKA Ultrosound F75 (Б, Г,) ultrasound devices: A, Б – before the Doppler mapping mode settings, В, Г – after the settings
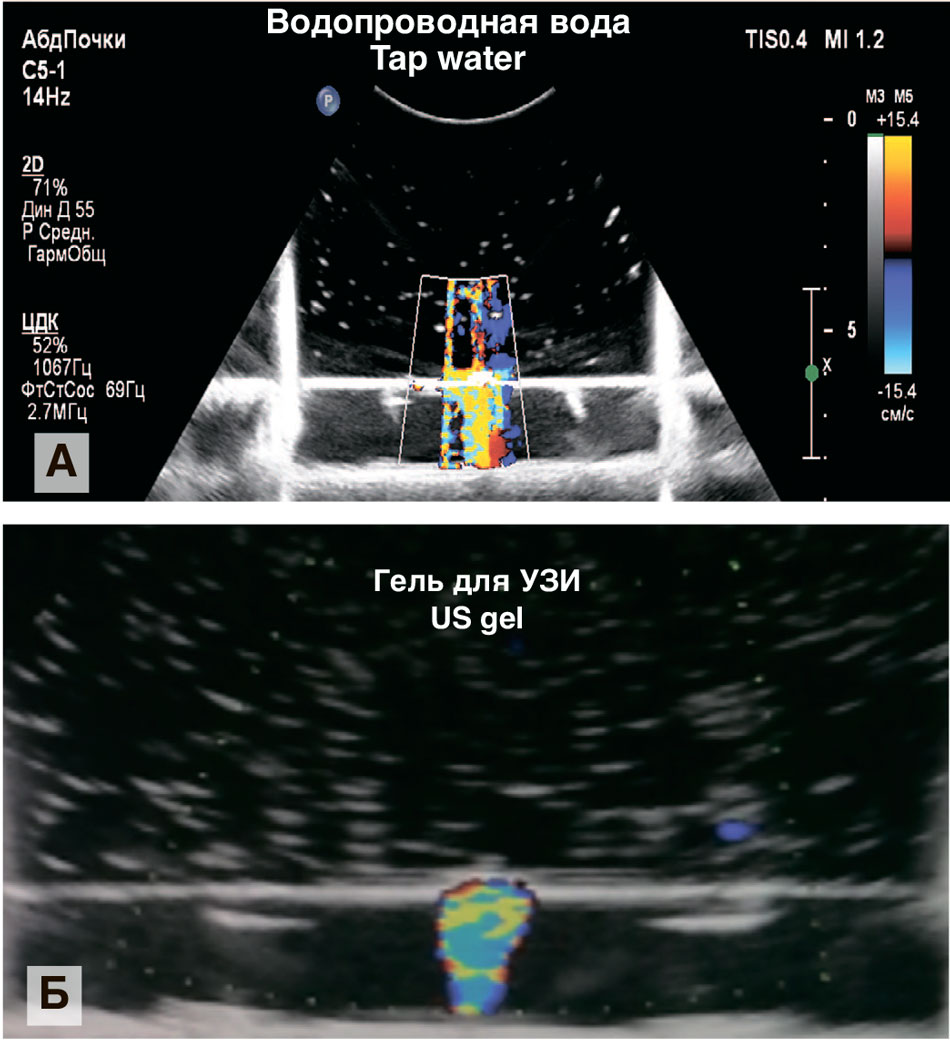
Рис. 5. Артефакт мерцания дигидрата сульфата кальция на УЗ-аппарате в различных контактных средах: водопроводная вода, гель для УЗИ (после настройки режима допплеровского картирования)
Fig. 5. Artifact of twinkling of calcium sulfate dihydrate on an ultrasonic device in various contact media: tap water, ultrasonic gel (after setting the Doppler mapping mode)
Как видно из рисунка 5, АМ удалось определить во всех контактных средах, но наиболее точный, соответствующий контурам конкремента был получен при использовании геля для УЗИ. Данное вещество, состоящее из очищенной воды, глицерина, пропиленгликоля, карбомера, гидроксида калия, консервантов и этилендиаминтетрауксусной кислоты (ЭДТА), улучшает изображение структуры камня за счет уменьшения реверберации, артефактов и наиболее схоже по своим морфометрическим свойствам с тканями человека. Использование же водопроводной воды и дегазированной воды отображали АМ практически одинаково, однако наличие пузырьков воздуха вызывало проявление АМ в них.
ОБСУЖДЕНИЕ
Проведенная экспериментальная работа по визуализации АМ в лабораторных условиях показала, что получение АМ при помощи устройства, разработанного нами, возможно. Мы оказались не новаторами в данном направлении, и подобные работы проводились ранее.
B.G. Wood с соавт. для визуализации АМ использовали контейнер с водой, в который помещали камень, подвешенный на марлевом гамаке, а на расстоянии 5 см от камня устанавливали конвексный УЗ-датчик. На наш взгляд, такая конструкция сложнее, чем предложенный нами вариант, поскольку марлевый гамак, являясь тканевой структурой, отображающей АМ, затрудняет дифференциацию АМ от камня и от марли. Использование силиконовой подложки на основе платины с углублением по центру позволяет решить эту проблему.
Мы выявили, что визуализация АМ зависит от изменений настроек допплеровского режима. Однако в работах M. Hirsh и соавт. и R. Bacha и соавт. показано, что АМ не зависит от них, в частности, от PRF (частоты повторения импульсов) [9, 10]. Мы с этим утверждением не согласны, так как изменение данной настройки позволяет убрать лишние шумы и тем самым улучшить визуализацию АМ. При этом, на разных аппаратах изменение частоты повторения импульсов оказалось различным. Так, на аппарате Philips Affinity 70 PRF для визуализации АМ необходимо увеличивать PRF до 70 см/с, а на ALOKA Logic 9 наоборот уменьшить до 20-30 см/с. Кроме того, мы отметили, что изменение расположения фокуса отображается на АМ: смещение выше локализации камня ухудшает визуализацию, а ниже, наоборот, усиливает её, но при этом появляются дополнительные артефакты.
Выбор контактной среды для проведения исследования имеет важное значение. Мы использовали 2 варианта: воду и гель для УЗИ. Нам удалось получить АМ во всех контактных средах, при этом визуализация АМ в водопроводной воде и дегазированной воде значительно не отличалась, за исключением пузырьков воздуха, которые под действием ультразвуковой волны хаотично перемещались в контейнере с водопроводной водой. Использование таких контактных сред очень простое, полностью перекрывает поступление воздуха и позволяет определять в лабораторных условиях АМ камней различного химического состава путем легкого погружения их в лунку при помощи пинцета. Использование же геля для УЗИ предоставляет более четкое изображение АМ именно в зоне конкремента. Это становится возможным благодаря большей плотности, вследствие чего сила проникающих волн за счет преломления, рассеяния и поглощения уменьшается и фокусируется исключительно на камне [11].] Однако использование геля усложняет изучение АМ камней различного химического состава, так как для этого необходимо полностью выбирать гель из контейнера, а затем вновь его наполнять. Погружение же камня в наполненный гелем контейнер фантома приводит к попаданию воздуха, что усложняет визуализацию АМ. Одним из решений может стать разработка закрытого фантома, чтобы не заменять гель. Данная работа проводится, ее результаты будут представлены в следующих публикациях.
ЗАКЛЮЧЕНИЕ
Проведенная экспериментальная работа по визуализации АМ в лабораторных условиях показала, что получение АМ in-vitro при помощи разработанного нами устройства возможно. Данное устройство значительно упрощает настройку режима допплеровского картирования ультразвукового аппарата для лучшей визуализации АМ и позволяет легко оценить возможность использования АМ на конкретном УЗ-сканере.
ЛИТЕРАТУРА
- Лютая Е.Д. Лучевая диагностика в зеркале доказательной медицины. Вестник Волгоградского государственного медицинского университета 2006;(4):3-9. [Lutaya E. D. Radiology in the mirror of evidence based medicine. Vestnik Volgogradskogo gosudarstvennogo meditsinskogo universiteta = Journal of Volgograd State Medical University 2006;(4):3-9. (In Russian)].
- Salmaslıoglu A, Bulakçı M, Bakır B, Yılmaz R, Akpınar YE, Tefik T, et al. The usefulness of agent emission imaging – high mechanical index ultrasound mode in the diagnosis of urolithiasis: A prospective preliminary study. Diagn Interv Radiol 2018;24(3):169-74. https://www.doi.org/10.5152/dir.2018.18005.
- Ozan E, Atac GK, Gundogdu S. Twinlking artifact on color Dopplerultrasound: an advantage or a pitfall? J Med Ultrasonics 2016;43(3):361-71. https://doi.org/10.1007/s10396-016-0715-z.
- Леонов Д.В., Кульберг Н.С., Громов А.И. Использование мерцающего артефакта для выявления твердых включений в ультразвуковой диагностике. Методические рекомендации №;11. Серия «Лучшие практики лучевой и инструментальной диагностики». ГБУЗ «НПКЦ ДиТ ДЗМ» 2021:32. [Leonov D.V., Kulberg N.S., Gromov A.I. Using a flickering artifact to detect solid inclusions in ultrasound diagnostics. Guidelines No. 11. Series «Best Practices in Radiation and Instrumental Diagnostics». State Budgetary Healthcare Institution «Research and Clinical Center for Diagnostics and Toxicology of the Moscow Health Department» 2021:32. (In Russian)].
- Васильев Ю.А., Семенов Д.С., Панина О.Ю., Ахмад Е.С., Васильева Ю.Н., Блохин И.А. и соавт. Артефакты от металлоконструкций в магнитно-резонансной томографии. Методические рекомендации №3. ГБУЗ «НПКЦ ДиТ ДЗМ» 2022:40. [Vasiliev Yu.A., Semenov D.S., Panina O.Yu., Akhmad E.S., Vasilyeva Yu.N., Blokhin I.A. et al. Artifacts from metal structures in magnetic resonance imaging. Methodical recommendations No. 3. State Budgetary Healthcare Institution «Research and Clinical Center for Diagnostics and Tractology of the Moscow Health Department» 2022:40. (In Russian)].
- Rahmouni A, Bargoin R, Herment A, Bargoin N, Vasile N. Color doppler twinkling artifact in hyperechoic regions. Radiology 1996;199(1):269-71. https://doi.org/10.1148/radiology.199.1.8633158.
- Васильев А.Ю., Громов А.И. Цветовое допплеровское картирование с использованием энергетического допплера в оценке патологии предстательной железы. Военно-медицинский журнал 1997;318(4):33-7. [Vasiliev A.Yu., Gromov A.I. Color Doppler mapping using power Doppler in assessing prostate pathology. Voyenno-meditsinskiy zhurnal = Military Medical Journal 1997;318(4):33-7. (In Russian)].
- Nabheerong P, Kengkla K, Saokaew S, Naravejsakul K Diagnostic accuracy of Doppler twinkling artifact for identifying urolithiasis: a systematic review and meta-analysis. J Ultrasound 2023;26(2):321-31. https://doi.org/10.1007/s40477-022-00759-z.
- Hirsch M, Palavecino T, León B. Color Doppler twinkling artifact: A misunderstood and useful sign. Revista Chilena de Radiología 2011;17(2):82-4.
- Bacha R, Manzoor I, Gilani SA, Khan AI. Clinical Significance of Twinkling Artifact in the Diagnosis of Urinary Stones. Ultrasound Med Biol 2019;45(12):3199-206. https://doi.org/10.1016/j.ultrasmedbio.2019.08.015.
- Lawrence JP. Physics and instrumentation of ultrasound. Crit Care Med 2007;35(8 Suppl): S314-22. https://doi.org/10.1097/01.ccm.0000270241.33075.60.







