ВВЕДЕНИЕ
В современной андрологии одной из значимых проблем является бесплодие [1]. В последние десятилетия была существенно переосмыслена роль мужского фактора в структуре бесплодного брака, поскольку неуклонно увеличивается количество мужчин с нарушенной фертильностью, о чем свидетельствуют неблагоприятные демографические показатели России и многих стран мира [2, 3]. Бесплодие характеризуется полиэтиологичностью и среди основных причин этого состояния рассматривают инфекционно-воспалительные заболевания, травмы, опухоли урогенитального тракта и аномалии развития мужской репродуктивной системы, эндокринопатии, генетические синдромы, иммунные факторы и варикоцеле [1, 3–7]. Отмечено, что истоки мужской инфертильности почти всегда лежат в детском возрасте, ярким примером чего является варикоцеле – одно из самых распространенных заболеваний мужчин, приводящих к бесплодию и наиболее часто диагностируемое в подростковом возрасте [8–11]. При варикоцеле бесплодие обусловлено гипертермией и ишемией яичка, развивающихся в результате изменения гемодинамики в извитых и расширенных венах семенного канатика, что приводит к регургитации теплой брюшной крови в вены мошонки и формированию теплового стресса [12, 13]. К тепловому стрессу очень чувствительны клетки сперматогенеза и клетки Сертоли и их повреждение приводит к нарушению сперматогенеза [14–16]. При этой патологии отмечается угнетение функции клеток Лейдига и происходит уменьшение синтеза тестостерона, а в условиях андрогенного дефицита ухудшается качество спермы [8, 13, 17]. Кроме того, в современной репродуктивной медицине все больше внимания уделяется нарушениям отцовского генома, основной причиной которого считают окислительный стресс, выступающий ведущим патофизиологическим механизмом патоспермии при варикоцеле [18]. Избыточность активных форм кислорода, свободных радикалов в эякуляте при оксислительном стрессе могут провоцировать повреждение сперматозоидов на субклеточном уровне, приводя не только к фрагментации ДНК, но и повреждению акросомы, митохондрий, усилению апоптоза [12, 16, 19–21].
Спермограмма, несомненно, является обязательным методом диагностики мужского бесплодия, прогноза фертильности и представляет собой результат исследования физических, количественных, морфологических, кинетических показателей эякулята. Электронно-микроскопическое исследование сперматозоидов (ЭМИС) относится к дополнительным, вспомогательным методам диагностики, позволяющим выявить изменения на субклеточном уровне, нередко сопровождающиеся нормозооспермией, особенно в случаях варикоцеле [6, 18, 22, 23].
Цель исследования: оценить ультраструктуру сперматозоидов у подростков, выявить изменения сперматозоидов, характерные для варикоцеле.
МАТЕРИАЛЫ И МЕТОДЫ
В исследовании приняли участие 130 подростков в возрасте 17 лет, из них у 100 человек диагностировано левостороннее варикоцеле, а 30 подростков без варикоцеле составили группу сравнения. Обследуемые соответствовали следующим критериям включения: наличие варикоцеле для основной группы, отсутствие инфекционно-воспалительных и других заболеваний органов мошонки, наличие опыта мастурбации для подростков обеих групп. Пациенты и их законные представители дали информированное согласие на участие в исследовании.
Эякулят для исследования был получен методом мастурбации после 3-5 дневного воздержания при соблюдении всех условий сбора спермы у подростков [24]. Анализ полученных образцов был выполнен в лаборатории электронной микроскопии ГАУЗ СО «КДЦ».
Для электронно-микроскопического исследования сперматозоидов (ЭМИС) эякулят фиксировали в 2,5% растворе глютаральдегида. Затем образец центрифугировали и полученный осадок помещали для последующей дофиксации в 1% раствор 4-х тетраоксида осмия. Затем образец проводили в спиртах возрастающей концентрации и полимеризовали в аралдитовой смоле при температуре 600С. Ультратонкие срезы получали на ультратоме Leica EM UC6 (Leica Mikrosysteme GmbH, Австрия), контрастировали цитратом свинца и исследовали в электронном микроскопе Morgagni 268 (FEI Company, Чехия-Голландия) при ускоряющем напряжении 70 киловольт. Строение сперматозоидов оценивали на продольных и поперечных срезах по следующим параметрам: форма ядра и состояние хроматина (степень компактизации, наличие вакуолей и очагов деструкции), наличие акросомы, ее локализация, размер и состояние, структура центриолей и аксонемы (количественные и качественные характеристики дуплетов, денеиновых ручек), структура и локализация митохондрий, плотных фибрилл, волокон фиброзного слоя, наличие цитоплазматической капли и ее локализация.
Поскольку сперматогенез осуществляется непрерывно, то на момент исследования в эякуляте присутствуют сперматозоиды, находящиеся на разных этапах жизненного цикла, в том числе и погибающие. Для оценки ультраструктуры сперматозоидов отбирались клетки с сохранными, четко визуализирующимися органеллами.
В общей сложности было просмотрено свыше 1500 срезов от 130 человек и произведено 1520 микрофотографий при увеличениях от 2200 до 71000.
Для выполнения статистического анализа результатов исследований использована компьютерная программа Microsoft Excel XP. Выполнена предварительная оценка нормальности распределения. Значения непрерывных величин представлены в виде M+m (M – среднее арифметическое, m – средняя квадратичная ошибка среднего значения) с учетом среднеквадратичного отклонения. При оценке достоверности различий (p) между признаками с нормальным распределением применялся коэффициент Стьюдента (t). Уровень статистической значимости принимали соответствующий p < 0,05.
РЕЗУЛЬТАТЫ
Результаты ультраструктурного анализа сперматозоидов подростков представлены в таблице 1. Следует учитывать, что возможна комбинация различных патологических изменений сперматозоидов у одного обследуемого.
Таблица 1. Результаты ЭМИС у подростков с варикоцеле и подростков группы сравнения
Table 1. Results of EMES in adolescents with varicocele and adolescents in the comparison group
| Показатель Indicator |
Подростки с варикоцеле Adolescents with varicocele, n (%) |
Подростки без варикоцеле Adolescents without varicocele, n (%) |
|---|---|---|
| Нормозооспермия / Normozoospermia | 47 (47%) | 19 (63,3%) |
| Олигозооспермия / Oligozoospermia | 16 (16%) | 4 (13,3%) |
| Тератозооспермия (дисплазия сперматозоидов) / Tgratozoospermia (sperm dysplasia) | 12 (12%) | 2 (6,6%) |
| Аномалии головок сперматозоидов (менее 30% головок сперматозоидов имеют нормальную форму и типичное строение структур головки) Anomalies of the sperm heads (less than 30% of the sperm heads have a normal shape and a typical structure of the structures of the head) |
19 (19%) | 3 (10%) |
| Признаки повреждения ДНК сперматозоидов (наличие неконденсированного, вакуолизированного хроматина) Signs of sperm DNA damage (presence of non-condensed, vacuolated chromatin) |
14 (14%) | 2 (6,7%) |
| Избыточность акросомы, ее некомпактное содержание / Excessive acrosome, its non-compact content | 26 (26%) | 7 (23,3%) |
| Преждевременная деградация акросомы / Premature degradation of the acrosome | 12 (12%) | 3 (10%) |
| Аномалии структуры центриоли, сегментированных столбиков в шейках сперматозоидов Anomalies in the structure of centrioles, segmented columns in the necks of spermatozoa |
— | — |
| Набухание митохондрий, деструкция крист, неупорядоченное положение митохондрий в среднем отделе жгутика Swelling of mitochondria, destruction of cristae, disordered position of mitochondria in the middle section of the flagellum |
38 (38%) | 7 (23,3%) |
| Патологические изменения аксонемы / Pathological changes in the axoneme | — | — |
| Аномалии фиброзной оболочки в основном отделе жгутика сперматозоида (избыточность) Anomalies of the fibrous membrane in the main section of the sperm flagellum (redundancy) |
2 (2%) | — |
| Наличие цитоплазматических капель в области жгутика с признаками его дисплазии The presence of cytoplasmic droplets in the area of the flagellum with signs of its dysplasia |
22 (22%) | 6 (20%) |
| Наличие сегментоядерных нейтрофилов / Presence of segmented neutrophils: - единичные клетки / Single cells - пиоспермия / pyospermia |
21 (21%) 5 (5%) |
6 (20%) 1 (3,3%) |
| Наличие бактерий / Presence of bacteria: - единичные или в небольшом количестве / Singly or in small quantities - бактериоспермия / Bacteriospermia |
24 (24%) 7 (7%) |
4 (13,3%) — |
| Слизь / Mucus | 24 (24%) | 7 (23,3%) |
| Амилоидные тельца / Amyloid cells | 18 (18%) | 4 (13,3%) |
| Наличие клеток сперматогенеза / Presence of spermatogenesis cells: - единичные клетки / Single cells - в большом количестве / In quantities - клетки с признаками деструкции / Cells with signs of destruction |
11 (11%) 5 (5%) 10 (10%) |
4 (13,3%) 2 (6,7%) 2 (6,7%) |
Примечание: статистически значимых различий (р < 0,05) между сравниваемыми группами не установлено
Note: there were no statistically significant differences (p < 0.05) between the compared groups
Под нормозооспермией в формате ЭМИС понимали преобладание сперматозоидов с типичной структурой головки (не менее 30% от всех просмотренных сперматозоидов), шейки и жгутика (рис. 1).
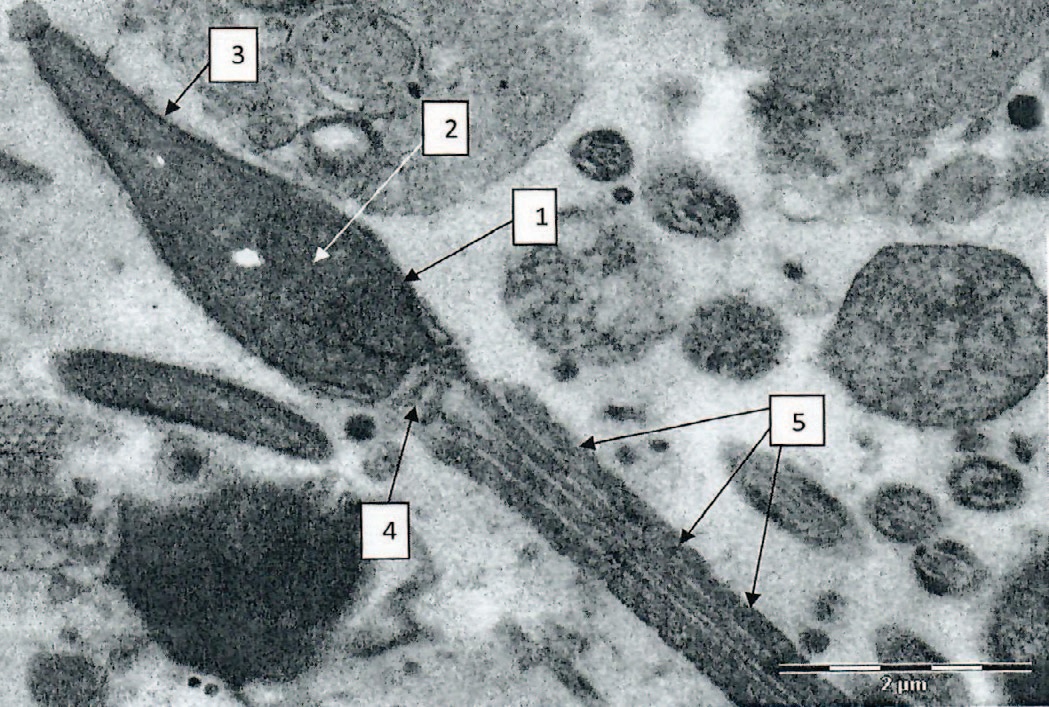
Рис. 1. Сперматозоид. Головка, типичная форма (1), зрелый хроматин гомогенного вида (2), акросома (3), шейка (4), средний отдел жгутика, типичная структура митохондрий (5). х 11000
Fig. 1. Sperm. Head, typical shape (1), mature homogeneous chromatin (2), acrosome (3), neck (4), middle part of the flagellum, typical structure of mitochondria (5). x 11000
Нормозооспермия является наиболее распространенным заключением в обеих группах, чаще диагностирована у подростков без варикоцеле, но статистически значимого различия не зафиксировано.
Заключение «олигозооспермия» было применено в тех случаях, когда отмечалось уменьшение количества сперматозоидов в исследуемой пробе, при этом ультраструктура сперматозоидов могла оставаться без патологических изменений. Частота встречаемости такого заключения приблизительно одинакова в обеих группах.
Тератозооспермия была диагностирована в тех случаях, когда в эякуляте преобладали сперматозоиды с различными вариантами дисплазии головок и жгутиков (рис. 2 а, б).
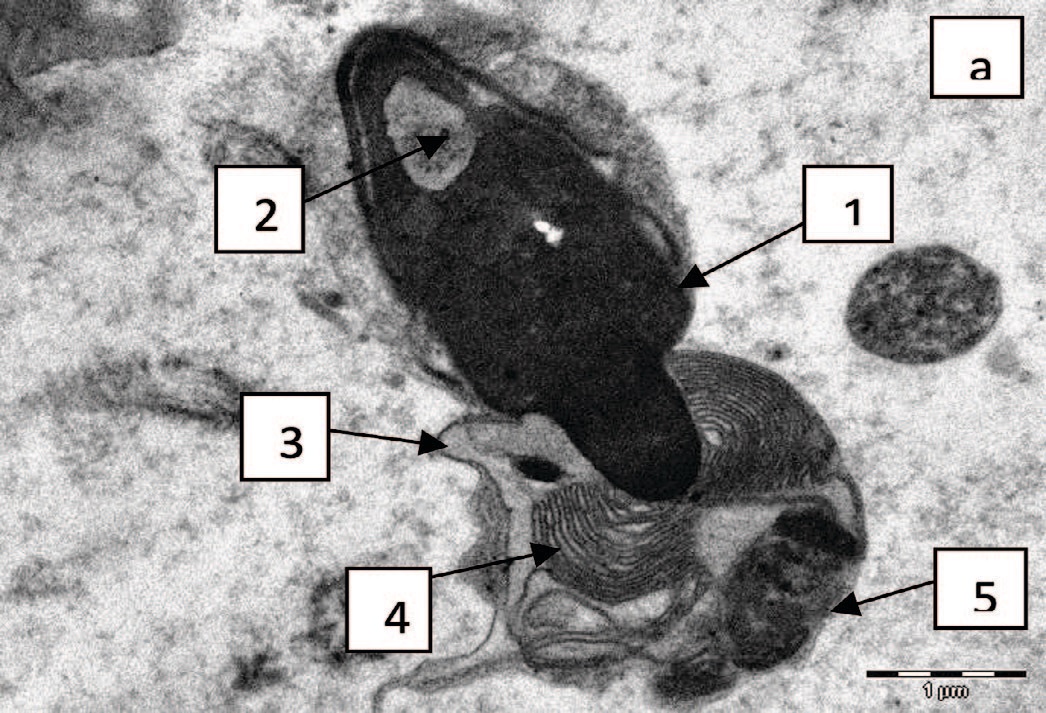
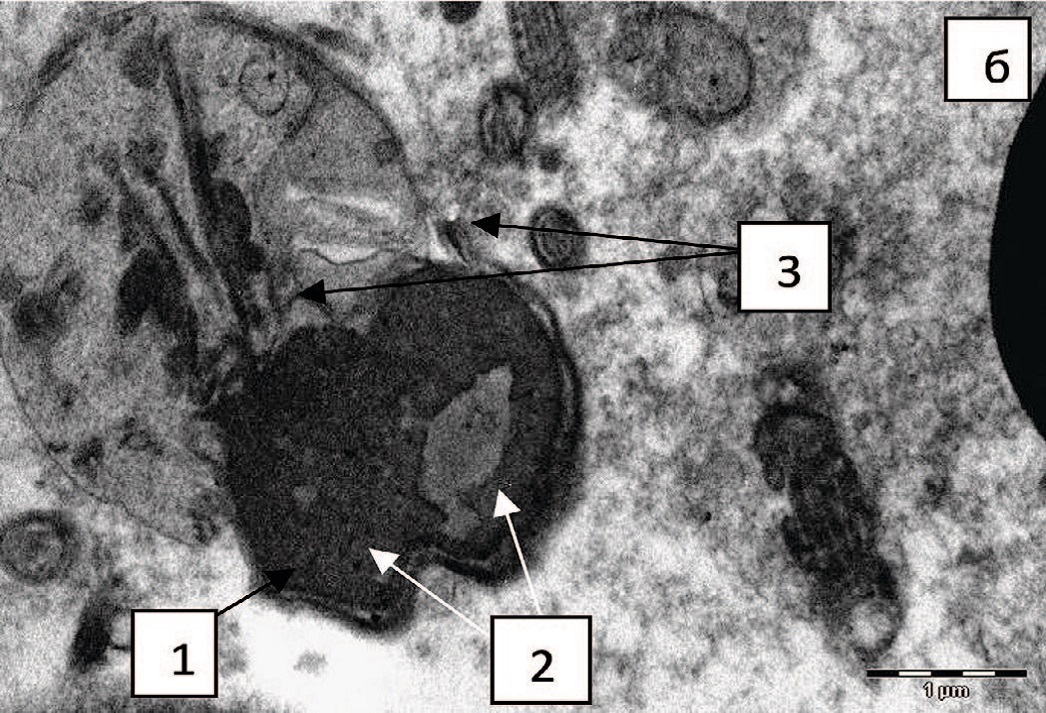
Рис. 2. Аномальные формы сперматозоидов, тяжелая дисплазия: а – аномальная форма головки сперматозоида (1), вакуолизированный хроматин (2), цитоплазмати- ческая капля (3), содержащая гиперплазированную ядерную мембрану (4), элементы недифференцированного жгутика (5); б – сдвоенная головка сперматозоида (1), неконденсированный, вакуолизированный хроматин (2), цитоплазматическая капля, содержащая недифференцированный жгутик (3). х 8900
Fig. 2. Abnormal forms of spermatozoa, severe dysplasia: a - abnormal shape of the head of the spermatozoon (1), vacuolated chromatin (2), cytoplasmic droplet (3) containing a hyperplastic nuclear membrane (4), elements of an undifferentiated flagellum (5); б - double head of the spermatozoon (1), non-condensed, vacuolated chromatin (2), cytoplasmic droplet containing an undifferentiated flagellum (3). x 8900
Все остальные патологические изменения встречаются в диагностически не значимом количестве, но их наличие обращает на себя внимание, а различные комбинации аномалий существенно повышают риск формирования инфертильности.
Не установлено статистически значимых различий в частоте встречаемости патологических изменений сперматозоидов между группами, хотя у подростков с варикоцеле чаще диагностируются аномальные формы головок сперматозоидов, признаки повреждения хроматина (рис. 3 а, б), аномалии структуры акросомы (рис. 4 а, б, рис. 5 а, б) и ее деградация (рис. 5 в, г).
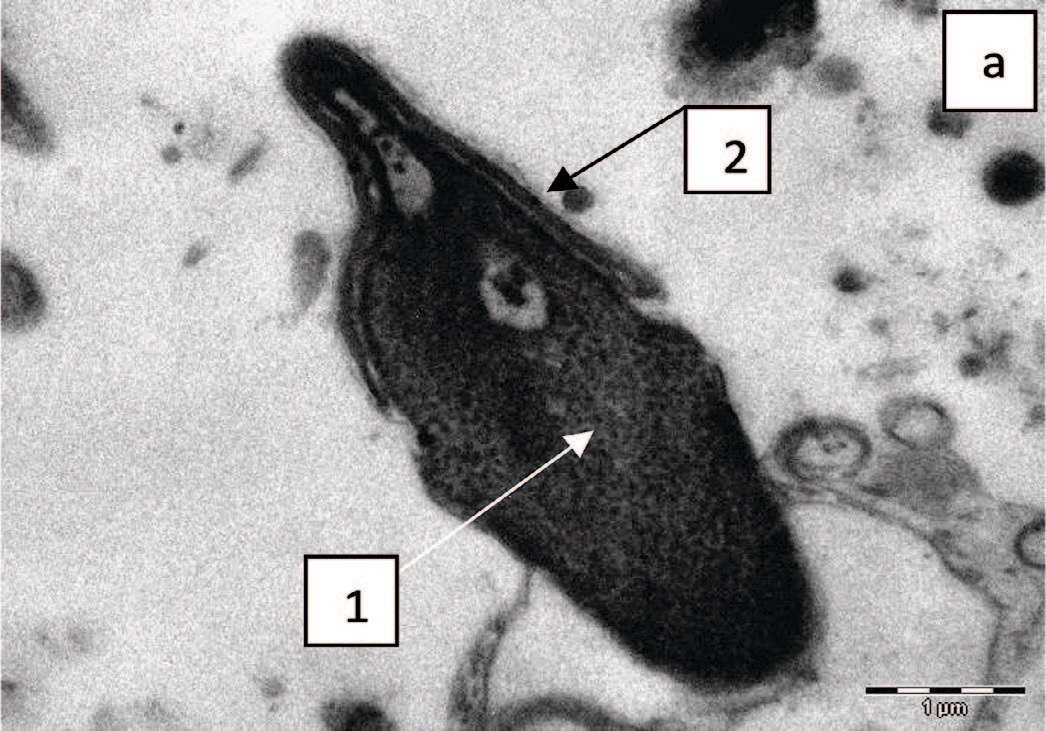
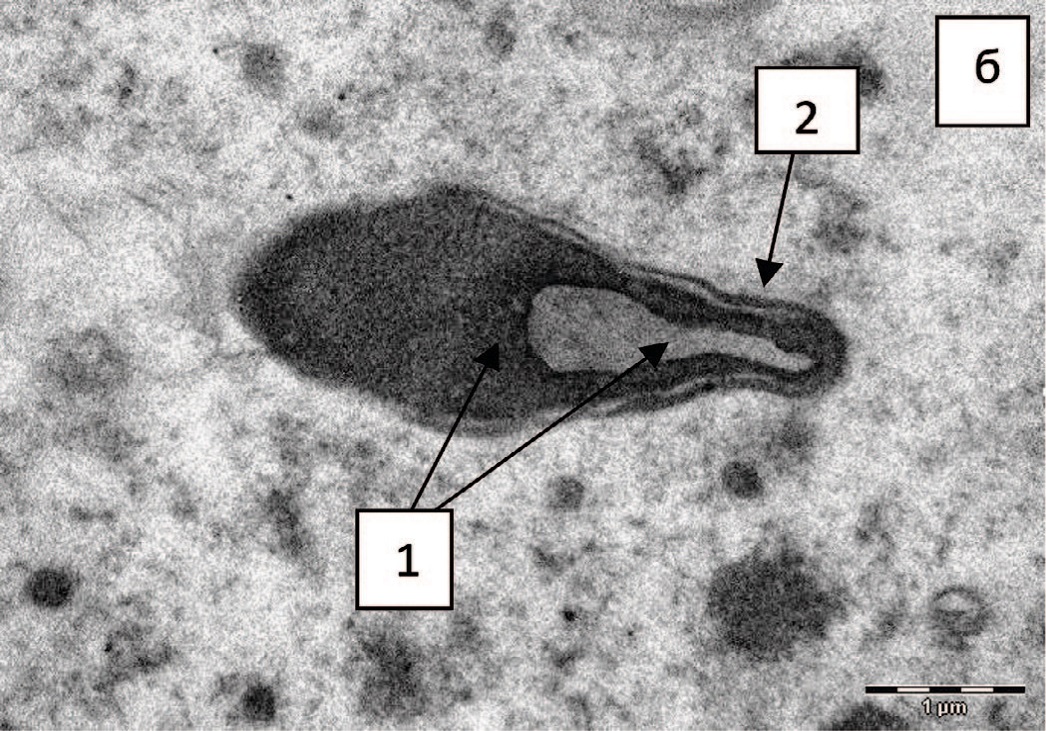
Рис. 3. Головки сперматозоидов: а – макроголовка, аномальная форма, неконденсированный гранулярный хроматин (1), уменьшенный размер акросомы (2), х 11000; б – типичная форма и размер головки сперматозоида, неконденсированный, гранулярный, вакуолизированный хроматин (1), типичная структура акросомы (2), х 14000
Fig. 3. Spermatozoa heads: a - macrohead, abnormal shape, non-condensed granular chromatin (1), reduced acrosome size (2), x 11000; б – typical shape and size of the sperm head, non-condensed, granular, vacuolated chromatin (1), typical acrosome structure (2), x 14000
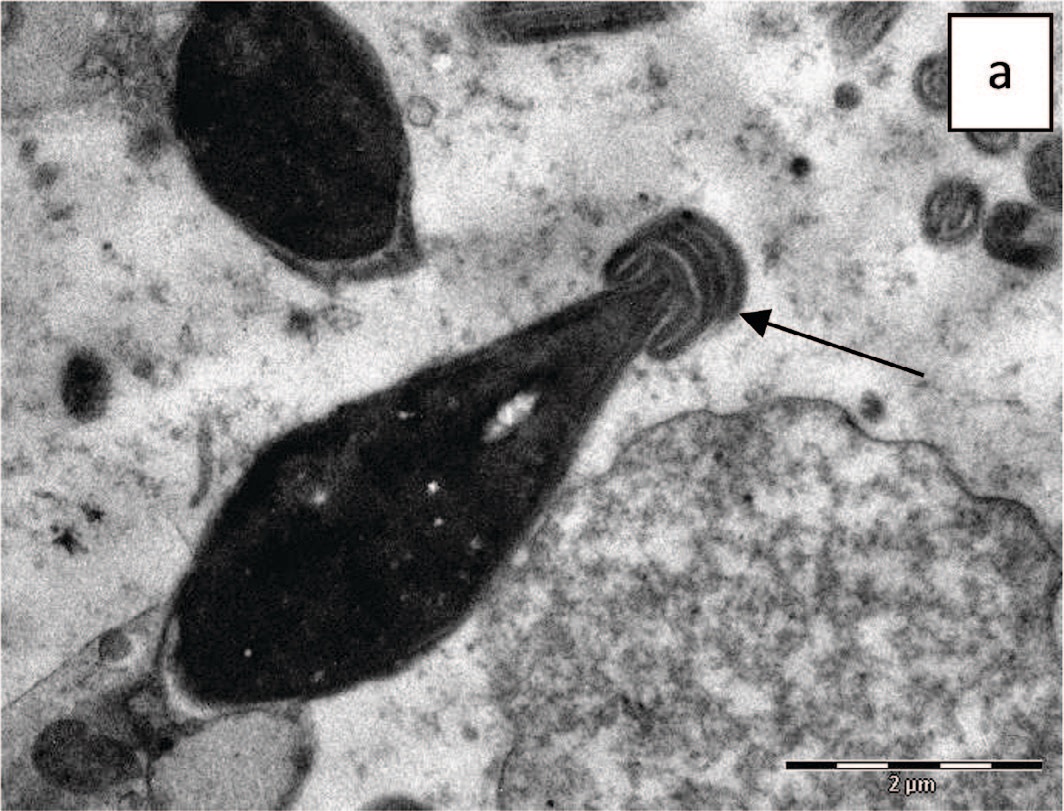
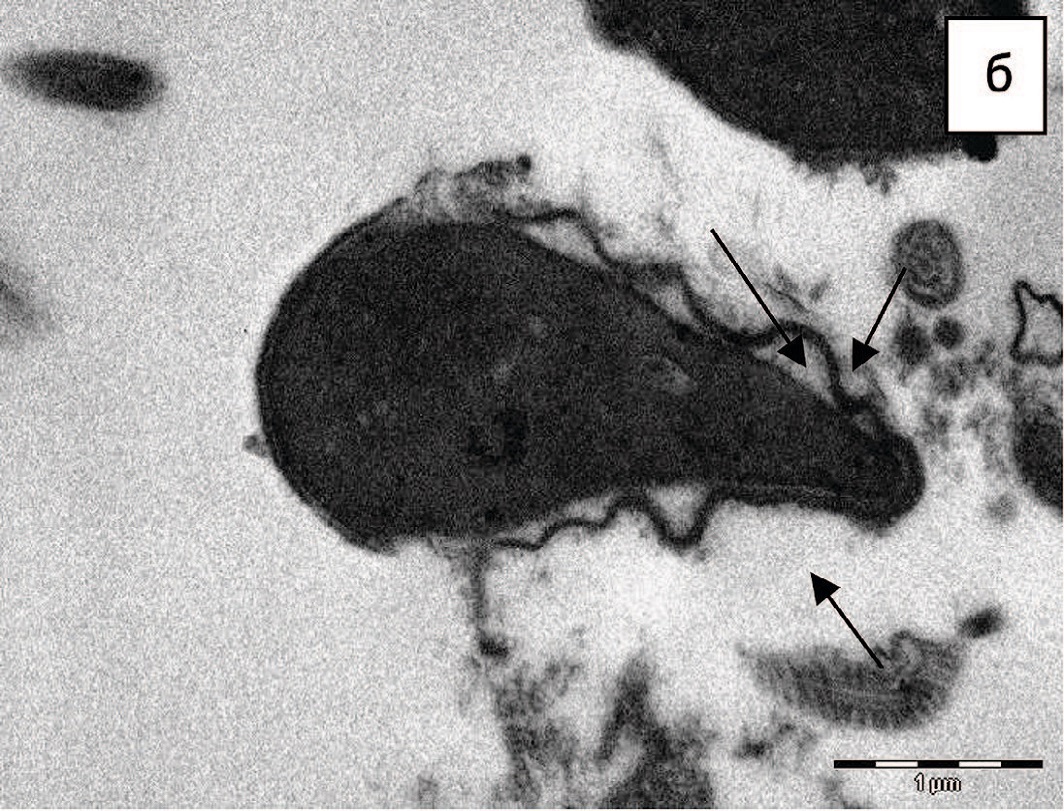
Рис. 4. Варианты избыточности акросомы: а – дисплазия акросомы, ее избыточность, складчатость, х 14000; б – избыточность акросомы, ее удаленное положение с расширением постакросомального пространства (показано стрелками), х 14000
Fig. 4. Variants of acrosome redundancy: a - acrosome dysplasia, its redundancy, folding, x 14000; б – redundancy of the acrosome, its remote position with the expansion of the postacrosomal space (shown by arrows), x 14000
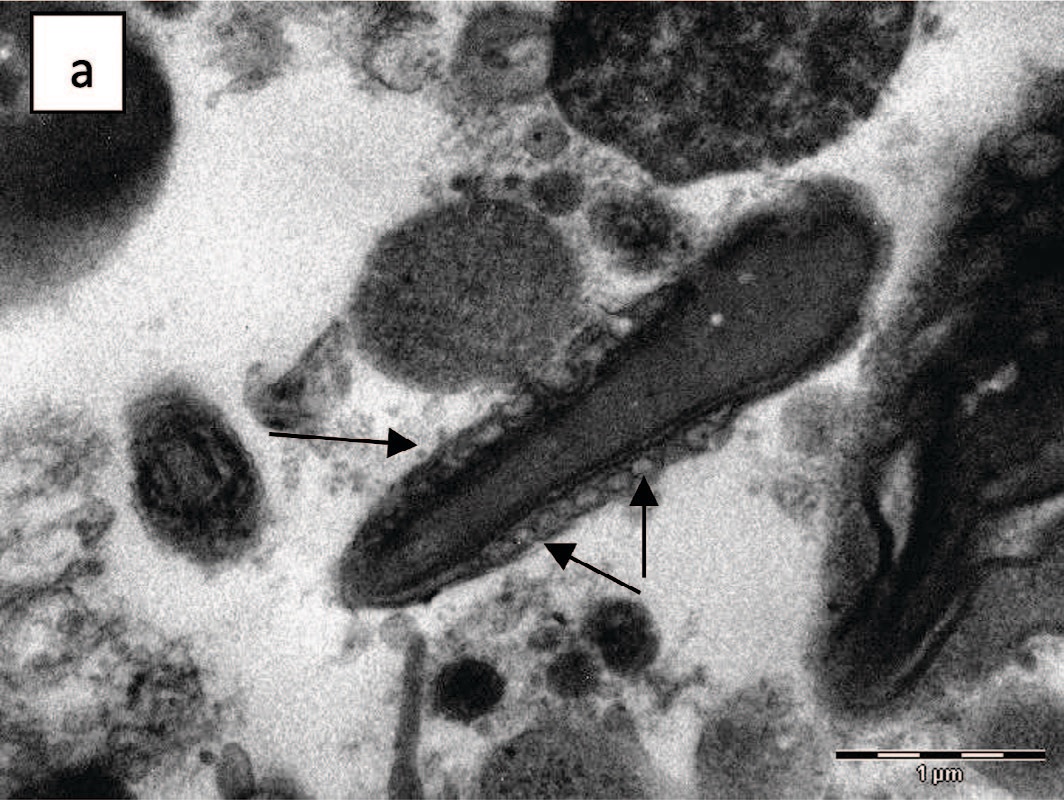
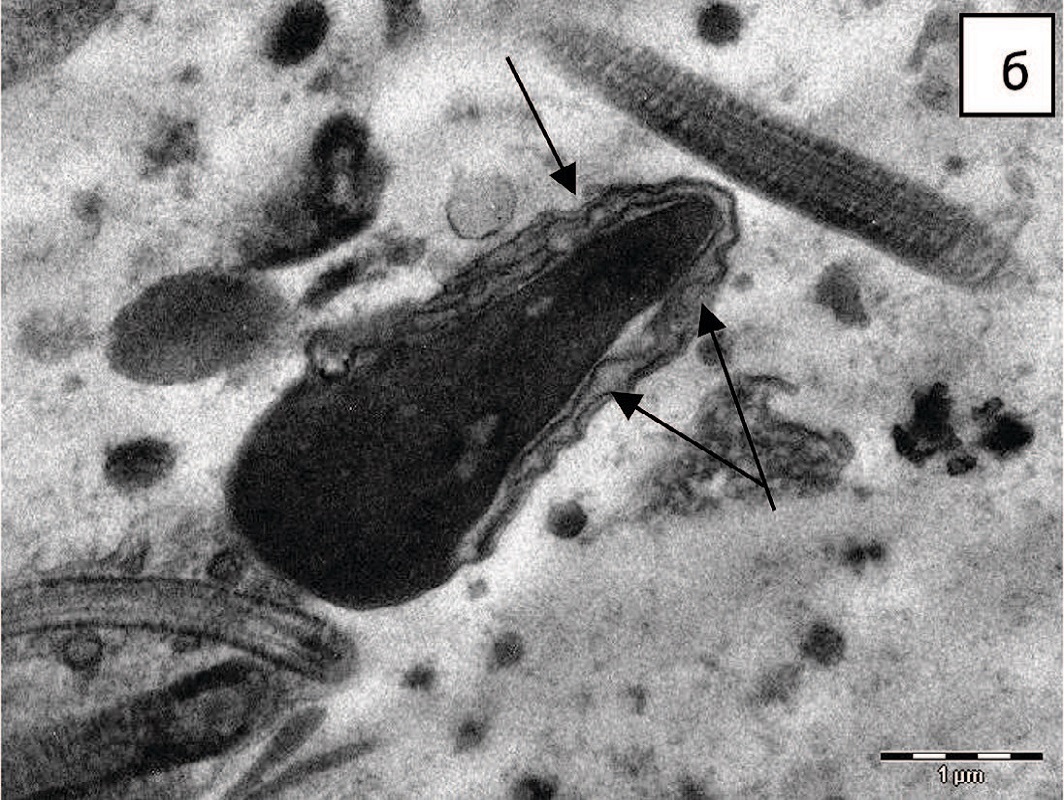
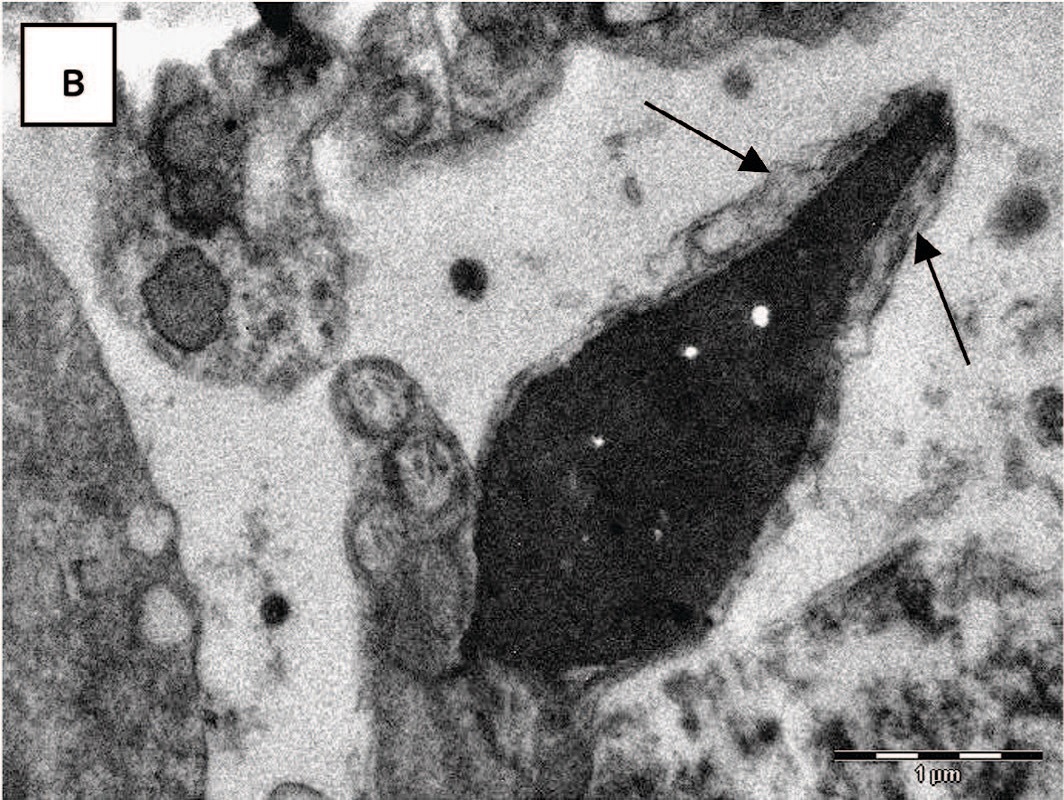
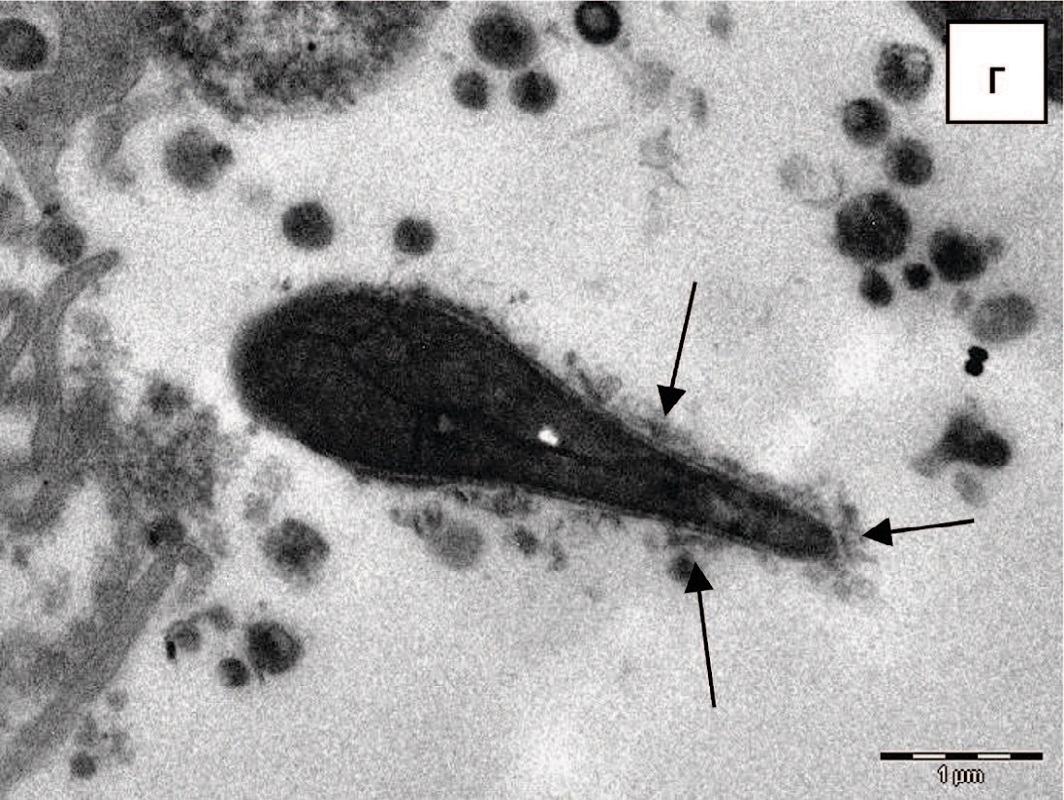
Рис. 5. Варианты патологических изменений акросомы: а,б – некомпактное содержание акросомы; в,г – деградация акросомы (показано стрелками), х 14000
Fig. 5. Variants of pathological changes in the acrosome: a, б – non-compact content of the acrosome; в,г – acrosome degradation (shown by arrows), x 14000
В структуре шеек и аксонемы жгутикоа значимого количества патологических изменений не обнаружено ни в одной из групп обследуемых.
В среднем отделе жгутика выявлено повреждение митохондрий, их набухание, деструкция крист, нередко неупорядоченное положение вокруг аксонемы. Чаще такие изменения были выявлены у подростков с варикоцеле, но статистически значимой разницы с пациентами группы сравнения не установлено (рис. 6 а, б).
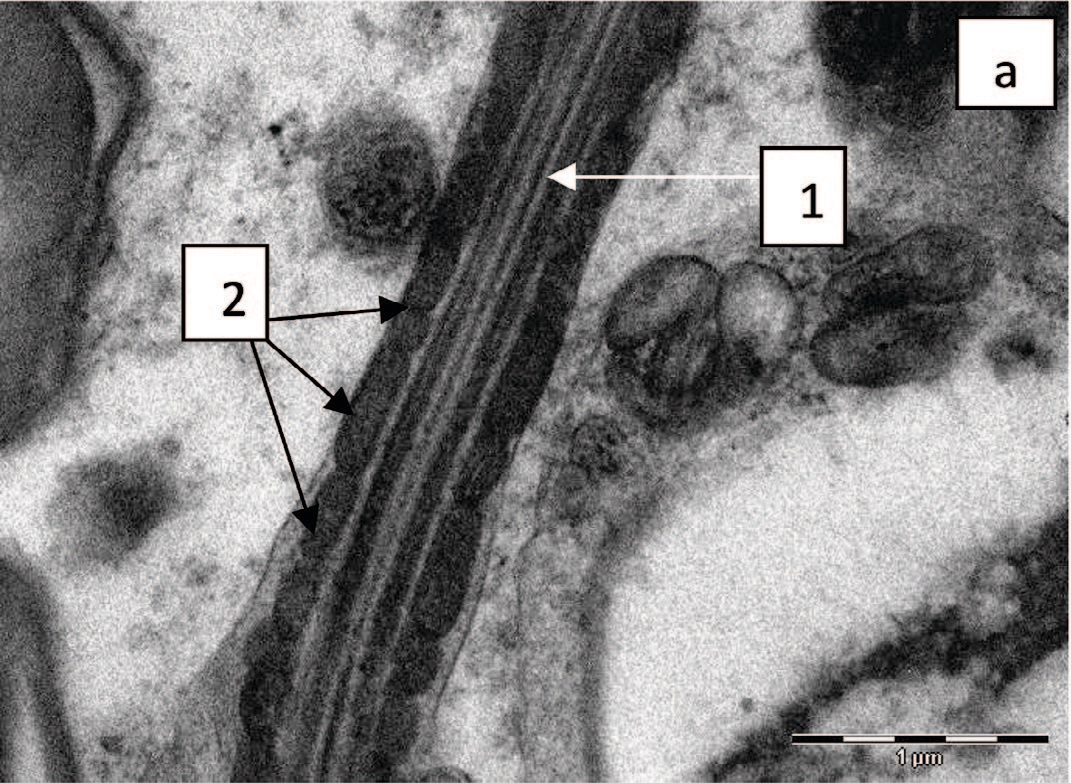
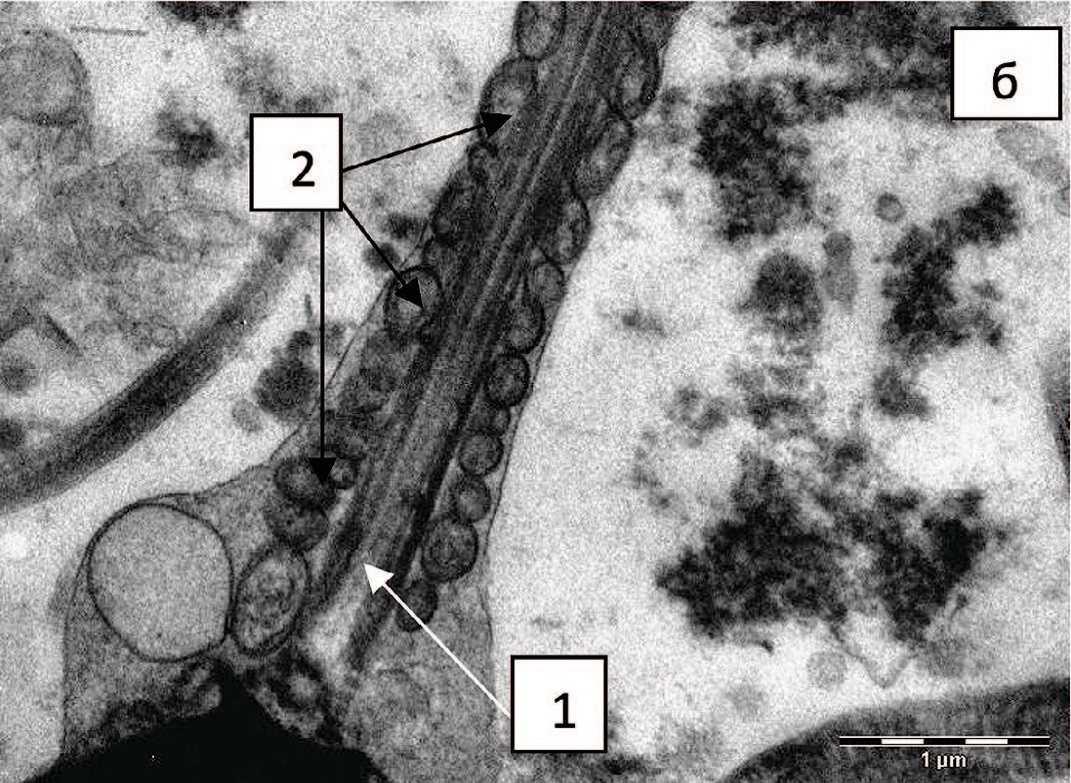
Рис. 6. Фрагмент среднего отдела жгутика: а – аксонема (1), митохондрии, имеющие типичную структуру (2); б – аксонема (1), набухание митохондрий, деструкция крист (2), х 14000
Fig. 6. Fragment of the middle section of the flagellum: a - axoneme (1), mitochondria with a typical structure (2); б – axoneme (1), swelling of mitochondria, destruction of cristae (2), x 14000
Не установлено статистически значимой разницы в частоте выявления сегментоядерных нейтрофилов в эякуляте подростков обеих групп, причем это касается как случаев, при которых обнаружены единичные клетки, так и случаев пиоспермии (рис. 7).
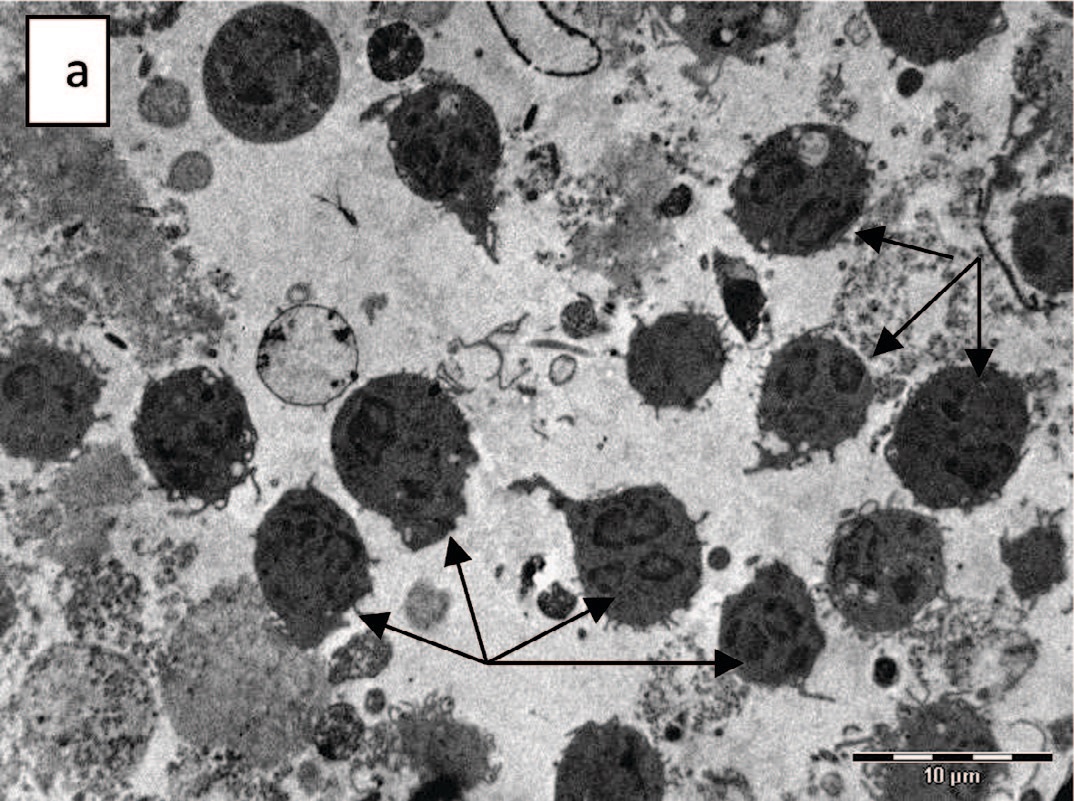
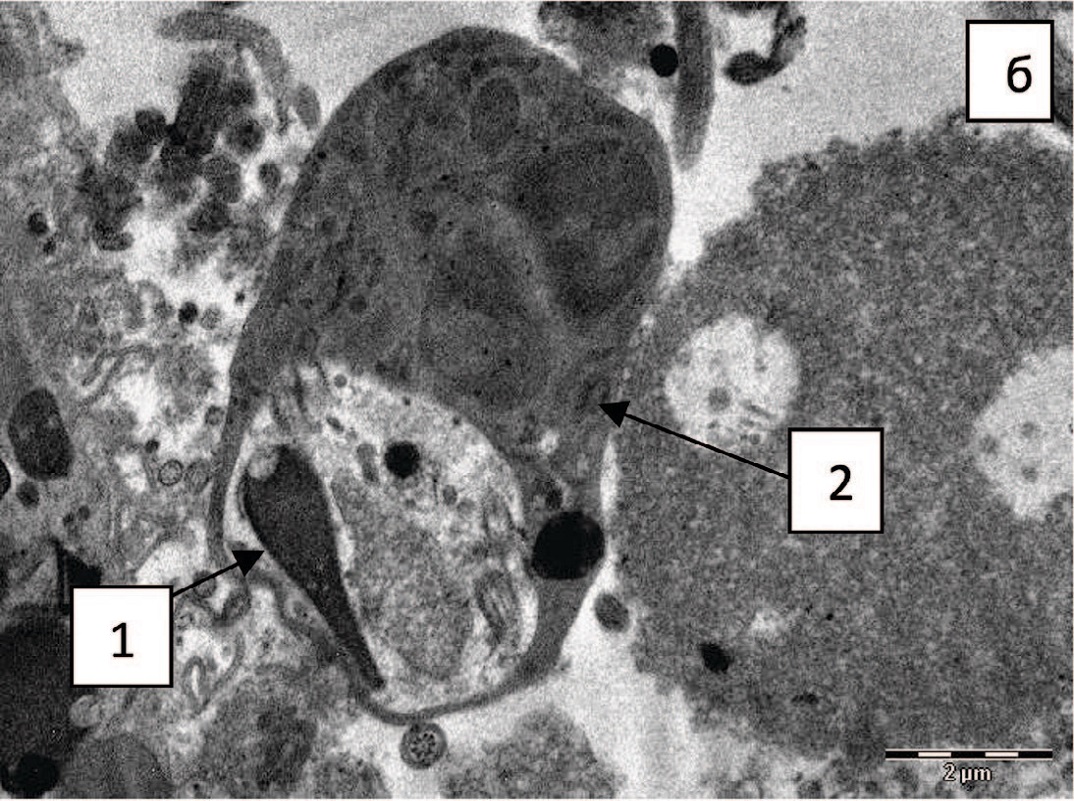
Рис. 7. Сегментоядерные нейтрофилы в эякуляте: а – пиоспермия, х 2200; б – фагоцитоз сперматозоида (1) сегментоядерным нейтрофилом (2), х 3500
Fig. 7. Segmented neutrophils in the ejaculate: a - pyospermia, x 2200; б – phagocytosis of sperm (1) by segmented neutrophil (2), x 3500
Бактерии в эякуляте чаще обнаружены у подростков с варикоцеле, но статистически значимого различия в количестве случаев в обеих группах не зафиксировано (рис. 8 а). Клетки сперматогенеза более часто были выявлены у подростков без варикоцеле (рис. 8 б), но у подростков с варикоцеле чаще были определены деструктивные изменения этих клеток, хотя статистически значимой разницы между группами не удалось установить.
В ходе исследования не было выявлено ультраструктурных изменений сперматозоидов, характерных для варикоцеле.
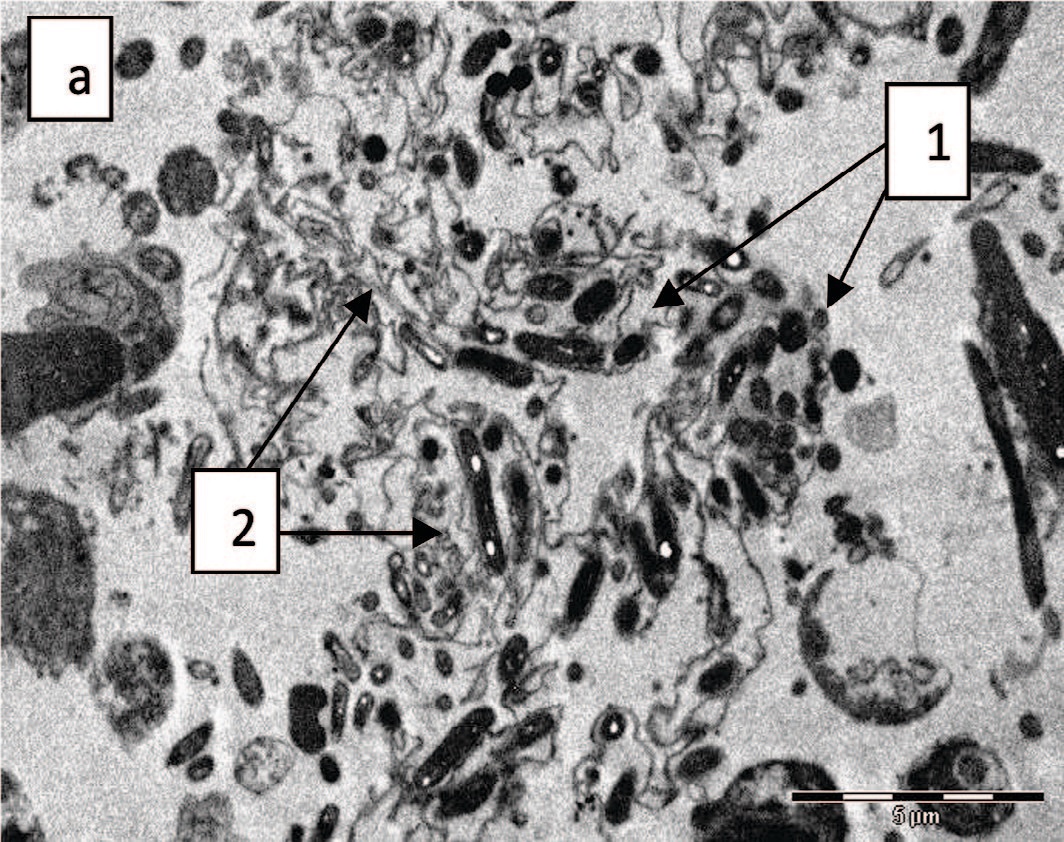
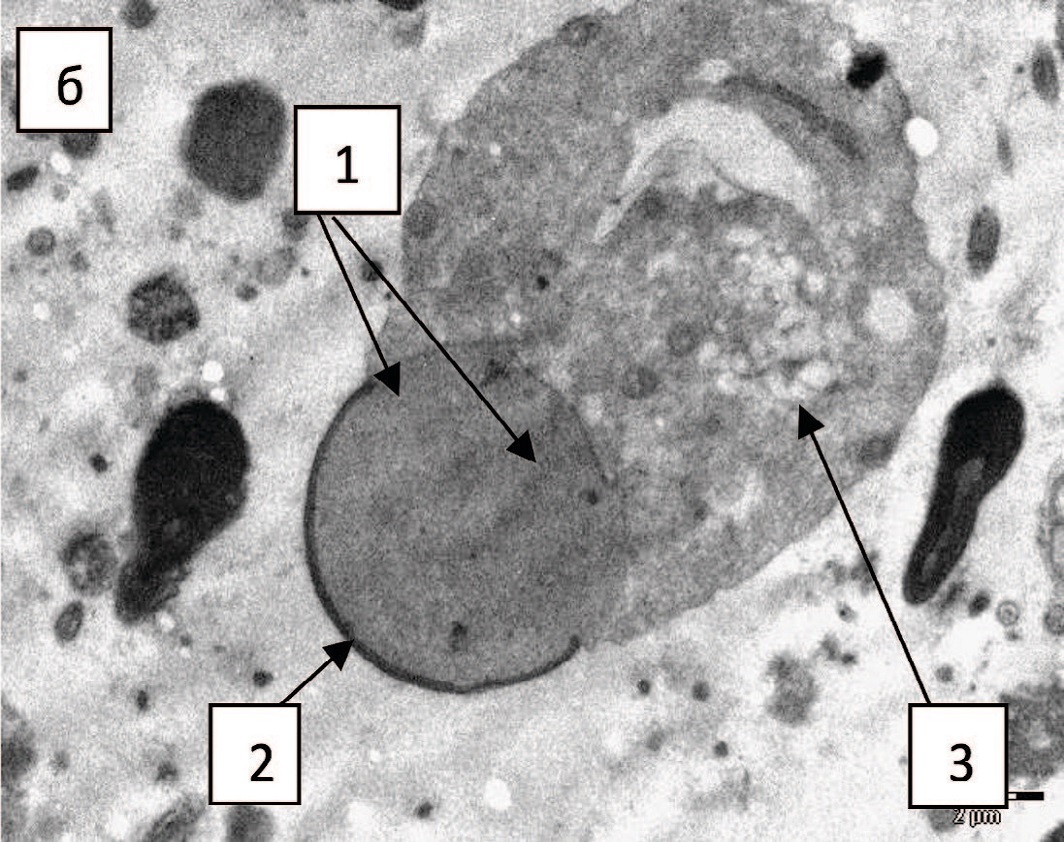
Рис. 8. Эякулят: а – адгезия бактерий (1) на тяжах слизи (2), х 3500; б - клетка сперматогенеза, круглая головка с разреженным хроматином (1), акросома (2), цитоплазма (3), х 7100
Fig. 8. Ejaculate: a - adhesion of bacteria (1) on mucus strands (2), x 3500; б – spermatogenesis cell, round head with sparse chromatin (1), acrosome (2), cytoplasm (3), x 7100
ОБСУЖДЕНИЕ
В связи с широким распространением варикоцеле среди бесплодных мужчин, это патологическое состояние рассматривается как основная причина инфертильности [12, 25-27]. Несмотря на полиэтиологичность варикоцеле окислительный стресс является ключевым моментом в патофизиологии бесплодия при варикоцеле [3, 17, 18, 28-31]. Окислительный стресс формируется в результате избыточного образования активных форм кислорода (АФК) и/или недостатка антиоксидантов, что и приводит к нарушению молекулярной организации клеточных структур, диагностируемой при электронной микроскопии сперматозоидов [2, 12, 32-34].
Проведя анализ полученных в результате исследования данных, было установлено, что у подростков обеих групп наиболее часто диагностирована нормозооспермия. Вероятно, это объясняется активным пубертатным периодом, гормональным подъемом и на этом фоне даже небольшие отклонения гомеостаза легко восстанавливаются протеомом семенной плазмы и в том числе, антиоксидантной системой [22].
Тем не менее у подростков обеих групп выявлены сходные патологические изменения структуры сперматозоидов, а это значит, что АФК присутствуют в эякуляте и оказывают негативное воздействие. В оптимальном количестве АФК необходимы для улучшения функции сперматозоидов, поскольку они контролируют количество половых клеток, индуцируя апоптоз или стимулируя пролиферацию сперматогоний, регулируют реакцию акросомы, стабильность митохондриальных мембран и подвижность сперматозоидов, конденсацию хроматина [33, 35]. Избыток АФК приводит к перекисному окислению полиненасыщенных жирных кислот в мембранах сперматозоидов, обусловливая нарушение структуры и функции сперматозоидов [35]. Увеличение АФК в эякуляте приводит к фрагментации ДНК сперматозоидов, под которой понимают одно- и двухцепочечные разрывы ДНК из-за нарушения замены гистонов на протамины, приводящие к нарушению конденсации генетического материала и появлению точечных мутаций, полиморфизмов, делеций, хромосомных перестроек [12, 25, 27, 29, 33-36]. На ультраструктурном уровне это может проявляться аномалиями головок, наличием неконденсированного, вакуолизированного хроматина и чаще встречается у подростков с варикоцеле.
Перекисное окисление мембран сперматозоидов и окислительная деградация липидов приводит к изменению «текучести» мембраны, образованию в ней крупных пор, изменение ионной проницаемости, приводя к формированию некомпактного содержания акросомы, ее преждевременной деградации [33, 34]. Из результатов исследования видно, что акросома является наиболее уязвимой структурой, наряду с митохондриями, изменения в ней выявляются гораздо чаще, чем в других структура у подростков обеих групп.
Повреждения мембран митохондрий в результате негативного воздействия избытка АФК приводит к их набуханию, деструкции крист и, в итоге, нарушению подвижности сперматозоидов. Кроме того, потенциальной целью атаки АФК является не только ядерная, но и митохондриальная ДНК, являющаяся более уязвимой, поскольку ядерная ДНК более плотно упакована протаминами [14]. Повреждение митохондриальной ДНК также приводит к образованию делеций и полиморфизмов, формированию митохонриальной дисфункции [12]. У подростков с варикоцеле чаще выявлены патологические изменения митохондрий. Остальные структуры – центриоль, сегментированные столбики, аксонема, фиброзные волокна – являются, видимо, более устойчивыми к действию АФК структурами, поскольку патологические изменения в них выявлены в небольшом количестве.
Источниками АФК являются сперматозоиды (зрелые, молодые клетки, аномальные формы), лейкоциты, клетки эпидидимиса, эндотелиальные клетки при варикоцеле, наличие бактерий [10, 11, 14, 25, 28, 32-37]. Как видно из полученных в ходе исследования данных, в эякуляте пациентов обеих групп присутствуют практически все из перечисленных источников АФК и при снижении антиоксидантной защиты можно ожидать возникновения патологических изменений сперматозоидов.
Таким образом в подростковом возрасте у обследованных с варикоцеле и без варикоцеле, определены признаки повреждения ультраструктуры сперматозоидов, но они компенсированы, количество их невелико. Как правило, в подростковом возрасте не проводят исследование эякулята и многие факторы (наличие бактерий, лейкоцитов), а также патологические изменения остаются не диагностированными и не подвергаются коррекции, приводя в дальнейшем к тяжелому повреждению сперматозоидов и развитию бесплодия. Варикоцеле является неуклонно прогрессирующим заболеванием и к моменту реализации репродуктивной функции способствовать развитию инфертильности будут также возрастные изменения и формирование андрогенного дефицита, воздействие негативных факторов окружающей среды и профессиональных вредностей, присоединение соматических и инфекционно-воспалительных заболеваний репродуктивного тракта, появление вредных привычек. Все это будет приводить к увеличению продукции АФК на фоне снижения антиоксидантной защиты и усугублению повреждения ультраструктуры сперматозоидов, снижению фертильного потенциала.
ВЫВОДЫ
- В подростковом возрасте наиболее часто выявлена типичная ультраструктура сперматозоидов.
- У подростков с варикоцеле чаще выявлены повреждения хроматина, акросомы, митохонрий, но статистически значимых различий по сравнению с подростками без варикоцеле не установлено.
- Не выявлено специфических изменений структуры сперматозоидов, характерных для варикоцеле. Работа выполнена в рамках госзадания ИИФ УрО РАН, тема № ФФФФ-Ф18-1180205900108-7
ЛИТЕРАТУРА
1. Лихоносов Н.П., Аюб А.Х., Бабенко А.Ю., Боровец С.Ю. Роль ингибина В в регуляции сперматогенеза и его клиническая значимость при мужском бесплодии. Урологические ведомости 2019;9(1):39-45. [Likhonosov N.P., Ayub A.Kh., Babenko A.Yu., Borovets S.Yu. The role of inhibin B in the regulation of spermatogenesis and its clinical significance in male infertility. Urulogy reports = Urologicheskiye vedomosti 2019;9(1):39-45 (In Russian)]. https://doi.org/org/10.17816/uroved9139-45.
2. Шевырин А.А. Современный взгляд на лечение нарушений мужской фертильной функции. РМЖ. Медицинское обозрение 2018;26(12):30-35. [Shevyrin A.A. A modern view on the treatment of disorders of male fertility. RMZH. Meditsinskoye obozreniye = The journal for medical practitioners «Russian Medical Review» 2018;26(12):30-35. (In Russian)].
3. Выборнов С.В., Асфандияров Ф.Р., Сеидов К.С., Круглов В.А. Антиоксиданты в лечении пациентов с воспалительными заболеваниями мужской репродуктивной системы, осложненными экскреторно-токсической формой бесплодия. Экспериментальная и клиническая урология 2018(3):74-78. [Vybornov S.V., Asfandiyarov F.R., Seidov K.S., Kruglov V.A. Antioxidants in the treatment of patients with inflammatory diseases of the male reproductive system, complicated by an excretory-toxic form of infertility. Eksperimental'naya i klinicheskaya urologiya 2018 = Experimental and clinical urology (3):74-78. (In Russian)].
4. Хайрутдинов К.Н., Ситдыкова М.Э., Зубков А.Ю. Мужское бесплодие – проблема XXI века. Практическая медицина 2018;16(6):185-189. [Khayrutdinov K.N., Sitdykova M.E., Zubkov A.YU. Male infertility is a problem of the XXI century. Prakticheskaya meditsina = Practical medicine 2018;16(6):185-189. (In Russian)]. https://doi.org/10.32000/2072-1757-2018-16-6-185-189.
5. Шмидт А.А., Замятин С.А., Гончар И.С., Коровин А.Е. Факторы риска развития мужской инфертильности. Клиническая патофизиология 2019(4):56-60. [Shmidt A.A., Zamyatin S.A., Gonchar I.S., Korovin A.Ye. Risk factors for the development of male infertility. Klinicheskaya patofiziologiya = Clinical Pathophysiology 2019(4):56-60. (In Russian)].
6. Потехин Е.С., Михайлюк Е.В., Непомнящих А.С. Спермограмма как инструмент оценки мужской фертильности. Научное обозрение 2020(1):11-14. [Potekhin Ye.S., Mikhaylyuk Ye.V., Nepomnyashchikh A.S. Spermogram as a tool for assessing male fertility. Nauchnoye obozreniye = Science review 2020(1):11-14. (In Russian)].
7. Авадиева Н.Э. Применение ДНК фрагментации спермы в андрологической практике. Вестник урологии 2019;7(1):7-11. [Avadiyeva N.E. Application of sperm DNA fragmentation in andrological practice. Vestnik urologii = Urology Herald 2019;7(1):7-11. (In Russian)]. https://doi.org/10.21886/2308-6424-2019-7-1-7-11.
8. Ефремов Е.А., Шеховцев С.Ю., Бутов А.О., Кастрикин Ю.В., Кодзоба А.С., Гараев Т.И. Влияние варикоцеле на гормональный фон и репродуктивную систему мужчины. Экспериментальная и клиническая урология 2019(1):102-106. [Yefremov Ye.A., Shekhovtsev S.YU., Butov A.O., Kastrikin YU.V., Kodzoba A.S., Garayev T.I. Influence of varicocele on the hormonal background and the male reproductive system. Eksperimental'- naya i klinicheskaya urologiya = Experimental and clinical urology 2019(1):102-106. (In Russian)].
9. Колесникова Л.И., Колесников С.И., Курашова Н.А., Баирова Т.А. Причины и факторы риска мужской инфертильности. Вестник РАМН 2015;70(5):579-584. [Kolesnikova L.I., Kolesnikov S.I., Kurashova N.A., Bairova T.A. Causes and risk factors of male infertility. Vestnik RAMN = Annals of the Russian Academy of Medical Sciences 2015;70(5):579-584. (In Russian)]. https://doi.org/10.15690/vramn.v70.i51445.
10. Курило Л.Ф., Сорокина Т.М., Матющенко Г.Н., Евдокимов В.В., Малолина Е.А., Ковалык В.П., Яковлева В.А., Гомберг М.А., Кущ А.А. Влияние бессимптомных инфекций урогенитального тракта на показатели эякулята у мужчин с бесплодием и варикоцеле. Андрология и генитальная хирургия 2016;17(2):98-103. [Kurilo L.F., Sorokina T.M., Matyushchenko G.N., Yevdokimov V.V., Malolina Ye.A., Kovalyk V.P., Yakovleva V.A., Gomberg M.A., Kushch A.A. Effect of asymptomatic infections of the urogenital tract on ejaculate parameters in men with infertility and varicocele. Andrologiya i genital'naya khirurgiya = Andrology and Genital Surgery 2016;17(2):98-103. (In Russian)]. https://doi.org/10.17650/2070-9781-2016-17-2-98-103.
11. Евдокимов В.В., Жуков О.Б., Кастрикин Ю.В., Байжуманов А.А., Туровецкий В.Б., Пирутин С.К. Оксидативный стресс и патозооспермия. Экспериментальная и клиническая урология 2017(2):73-77. [Yevdokimov V.V., Zhukov O.B., Kastrikin YU.V., Bayzhumanov A.A., Turovetskiy V.B., Pirutin S.K. Oxidative stress and pathozoospermia. Eksperimental'naya i klinicheskaya urologiya = Experimental and clinical urology 2017(2):73-77. (In Russian)].
12. Hassanin AM, Ahmed HH, Kaddah AN. A Global View of the Pathophysiology of Varicocele. Andrology 2018;6(5):654-661. https://doi.org/10.1111/andr.12511.
13. Rehman KU, Zaneb H, Qureshi AB, Yousaf MS, Numan A, Majeed KA, Rabbani I, Khan TM, Rehman H. Correlation Between Testicular Hemodynamic and Semen Quality Indices in Clinical Varicocele Patients in Pakistan. Biomed Res Int 2019;7;2019:7934328. https://doi.org/10.1155/2019/7934328.
14. Cho CL, Esteves SC, Agarwal A. Novel insights into the pathophysiology of varicocele and its association with reactive oxygen species and sperm DNA fragmentation. Asian J Androl 2016;18(2):186-93. https://doi.org/10.4103/1008-682X.170441.
15. Zhang Y, Ma T, Su Z, Ye M, Tian H, Li J, Liu J. Varicocele affects sperm quality in infertile men in South China: a cross-sectional study of 5447 cases. Medicine (Baltimore) 2017;96(31):e7707. https://doi.org/10.1097/MD.0000000000007707.
16. Cannarella R, Calogero AE, Condorelli RA, Giacone F, Aversa A, Vignera SL. Management and Treatment of Varicocele in Children and Adolescents: An Endocrinologic Perspective. J Clin Med 2019;8(9):1410. https://doi.org/10.3390/jcm8091410.
17. Busetto GM, Del Giudice F, Virmani A, Sciarra A, Maggi M, Ferro M. Body Mass Index and Age Correlate With Antioxidant Supplementation Effects on Sperm Quality: Post Hoc Analyses From a Double-Blind Placebo-Controlled Trial. Andrologia 2020;52(3):e13523. https://doi.org/10.1111/and.13523.
18. Неймарк А.И., Неймарк Б.А., Давыдов А.В., Салдан И.П., Ноздрачев Н.А. Реабилитация пациентов с мужским бесплодием после варикоцелеэктомии. Эффективная фармакотерапия 2018(9):8-12. [Neymark A.I., Neymark B.A., Davydov A.V., Saldan I.P., Nozdrachev N.A. Rehabilitation of patients with male infertility after varicocelectomy. Effektivnaya farmakoterapiya = Effective pharmacotherapy 2018(9):8-12. (In Russian)].
19. Kumar M, Selvam P, Agarwal A. Sperm and Seminal Plasma Proteomics: Molecular Changes Associated With Varicocele-Mediated Male Infertility. World J Mens Health 2019. Published online. https://doi.org/10.5534/wjmh.190018.
20. Agarwal A, Rana M, Qiu E, AlBunni H, Bui AD, Henkel R. Role of Oxidative Stress, Infection and Inflammation in Male Infertility. Andrologia 2018;50(11):e13126. https://doi.org/10.1111/and.13126. 21. Nguyen TT, Trieu TS, Tran TO, Luong TLA. Evaluation of sperm DNA fragmentation index, Zinc concentration and seminal parameters from infertile men with varicocele. Andrologia 2019;51(2):e13184. https://doi.org/10.1111/and.13184.
21. Alargkof V, Kersten L, Stanislavov R, Kamenov Z, Nikolinakos P. Relationships Between Sperm DNA Integrity and Bulk Semen Parameters in Bulgarian Patients With Varicocele. Arch Ital Urol Andro 2019;91(2). https://doi.org/10.4081/aiua.2019.2.125.
22. Esteves SC, Agarwal A. Afterword to varicocele and male infertility: current concepts and future perspectives. Asian J Androl 2016;18(2):319–322. https://doi.org/10.4103/1008-682X.172820.
23. Охрана репродуктивного здоровья мальчиков и юношей-подростков: Информационное письмо МЗ РФ; М. 1999;49 с. [Protection of the reproductive health of boys and adolescents: Information letter of the Ministry of Health of the Russian Federation. MН of Russia; M. 1999; 49 р. (In Russian)].
24. Santana VP, Miranda-Furtado CL, Pedroso DCC, Eiras MC, Vasconcelos MAC, Ramos ES. The Relationship Among Sperm Global DNA Methylation, Telomere Length, and DNA Fragmentation in Varicocele: A Cross-Sectional Study of 20 Cases. Syst Biol Reprod Med 2019;65(2):95-104. https://doi.org/10.1080/19396368.2018.1557762.
25. Cho CL, Esteves SC, Agarwal A. Indications and Outcomes of Varicocele Repair. Panminerva Med 2019;61(2):152-163. https://doi.org/ 10.23736/S0031-0808.18.03528-0.
26. Tahamtan S, Tavalaee M, Izadi T, Barikrow N, Zakeri Z, Lockshin RA. Reduced Sperm Telomere Length in Individuals With Varicocele Is Associated With Reduced Genomic Integrity. Sci Rep 2019;9(1):4336. https://doi.org/10.1038/s41598-019-40707-2.
27. Santana VP, Miranda-Furtado CL, de Oliveira-Gennaro FG, Dos Reis RM. Genetics and epigenetics of varicocele pathophysiology: an overview. J Assist Reprod Genet 2017;34(7):839-847. https://doi.org/10.1007/s10815-017-0931-5.
28. Кириленко Е.А., Онопко В.Ф. Окислительный стресс и мужская фертильность: современный взгляд на проблему. Бюллетень ВСНЦ СО РАМН 2017;2(2):102-108. [Kirilenko Ye.A., Onopko V.F. Oxidative stress and male fertility: a modern view of the problem. Byulleten' VSNTS SO RAMN = The journal Acta Biomedica Scientifica 2017;2(2):102-108. (In Russian)].
29. Калиниченко С.Ю., Тюзиков И.А. Окислительный стресс и мужское бесплодие – взаимосвязанные пандемии XXI в. Современные фармакотерапевтические возможности патогенетической коррекции нарушений сперматогенеза препаратами L-карнитина/ацетил- L-карнитина. Урология и нефрология. Спецвыпуск «Мужское здоровье» 2017(22):6-19. [Kalinichenko S.YU., Tyuzikov I.A. Oxidative stress and male infertility are interconnected pandemics of the 21st century. Modern pharmacotherapeutic possibilities of pathogenetic correction of spermatogenesis disorders with L-carnitine/acetyl-L-carnitine preparations. Urologiya i nefrologiya. Spetsvypusk «Muzhskoye zdorov'ye» = Urology and Nephrology. Special Issue "Men's Health" 2017(22):6-19. (In Russian)].
30. Баженов И.В., Филлипова Е.С. Роль окислительного стресса в патогенезе мужского бесплодия. Урология и нефрология 2018(29):50-58. [Bazhenov I.V., Fillipova Ye.S. The role of oxidative stress in the pathogenesis of male infertility. Urologiya i nefrologiya = Urology and Nephrology 2018(29):50-58. (In Russian)].
31. Agarwal A, Rana M, Qiu E, AlBunni H, Bui AD, Henkel R. Role of Oxidative Stress, Infection and Inflammation in Male Infertility. Andrologia 2018;50(11):e13126. https://doi.org/10.1111/and.13126.
32. Barati E, Nikzad H, Karimian M. Oxidative Stress and Male Infertility: Current Knowledge of Pathophysiology and Role of Antioxidant Therapy in Disease Management. Cell Mol Life Sci 2020;77(1):93-113. https://doi.org/10.1007/s00018-019-03253-8.
33. Кульченко Н.Г. Основные виды антиоксидантной терапии патоспермии. Вестник медицинского института «РЕАВИЗ» 2018(1):41-48. [Kul'chenko N.G. The main types of antioxidant therapy for pathospermia. Vestnik meditsinskogo instituta «REAVIZ» = Bulletin of Medical university "REAVIZ" 2018(1):41-48. (In Russian)].
34. Majzoub A, Esteves SC, Gosálvez J, Agarwal A. Specialized sperm function tests in varicocele and the future of andrology laboratory. Asian J Androl 2016;18(2):205-12. https://doi.org/10.4103/1008-682X.172642.
35. Tanaka T, Kobori Y, Terai K, Inoue Y, Osaka A, Yoshikawa N, at al. Seminal Oxidation-Reduction Potential and Sperm DNA Fragmentation Index Increase Among Infertile Men With Varicocele. Hum Fertil (Camb) 2020(20):1-5. https://doi.org/10.1080/14647273.2020.1712747. PMID: 31955637 36. Martins AD, Agarwal A. Oxidation reduction potential: a new biomarker of male infertility. Panminerva Med 2019;61(2):108-117. https://doi.org/10.23736/ S0031-0808.18.03529-2.







