Растущая распространенность мочекаменной болезни (МКБ) продолжает оставаться серьезной проблемой для здравоохранения развитых стран [1-6]. Воздействие социальных факторов и изменение стиля жизни населения считаются главными причинами роста частоты случаев МКБ за последние десятилетия [7].
Оксалат кальция представляет на сегодняшний день основную минеральную фазу, обнаруживаемую в уролитах в 70-75% случаях МКБ [8, 9]. Высокая частота рецидивов кальцийоксалатных камней (около 50%) [3] и неудовлетворительные результаты метафилактики, проводимой зачастую неадекватно, указывают на необходимость разработки новых методов как выявления индивидуальных причин возникновения и развития оксалатного уролитиаза, как и методов совершенствования мониторинга противорецидивного лечения.
Нередко оксалатный уролитиаз развивается, несмотря на то, что индивидуальные лабораторные показатели пациентов лежат в соответствующих диапазонах нормы. И этот факт становится общей проблемой в повседневной урологической практике. В большинстве случаев образование кальций-оксалатных камней является процессом идиопатическим. В 70-85% случаев у пациентов с оксалатными камнями отсутствуют изменения известных лабораторных показателей, свидетельствующих о литогенных нарушениях [10, 11, 12], поскольку процесс камнеобразования является результатом сложного дисбаланса между многочисленными промоторными и ингибиторными факторами мочи [13, 14].
К показателям риска развития уролитиаза относят, главным образом, биохимические показатели мочи, в частности, показатели избыточной экскреции с мочой таких литогенных ионов и веществ, как кальций, оксалаты, ураты, фосфаты и показатели сниженной экскреция цитратов и магния. Важными параметрами являются также значения рН мочи и объем суточной мочи. Степень риска камнеобразования обычно оценивают по соотношению между промоторами (инициаторами и ускорителями) и ингибиторами этого процесса.
С использованием биохимических и физико-химических показателей мочи было предложено большое разнообразие диагностических индексов и коэффициентов, отражающих соотношение промоторов (кальция, оксалатов) и ингибиторов (цитратов, магния) оксалатного литогенеза [15-18].
Наиболее известен индекс Тизелиуса [AP(CaOx)], применяемый для оценки риска развития кальций-оксалатного уролитиаза, наиболее распространенного вида МКБ [19]. AP(CaOx) индекс H.G. Tiselius разработал в качестве аналитического инструмента для расчета произведения ионной активности по отношению к оксалату кальция на основе данных биохимических показателей мочи [20]. AP(CaOx) объединяет наиболее влияющие параметры мочи в соответствующий индекс и рассчитывается как: APCaOx = (1.9 х Ca0.84 х Ox)/(Mg0.12 х Cit0.22 х V1.03), где AP [activity product] – произведение активности ионов кальция и оксалата; V(мл) суточный объем мочи, значения суточной экскреции (мМоль/сут) кальция (Ca), оксалата (Ox), магния (Mg), и цитратов (Cit) [20, 21].
Другой тип индексов риска основан на компьютерном воспроизведении известных моделей термодинамического равновесия, описывающих сложные химические взаимодействия наиболее важных компонентов мочи. С помощью этих моделей в результате многократных итераций рассчитываются ионные активности и концентрации потенциально возможных сосуществующих комплексов, на основе анализа исходного химического состава мочи. Учитываются лишь некоторые важные компоненты, такие как [H3O+], [Na+], [K+], [Ca2+], [Mg2+], [NH4+], [SO42−], [PO43−], [Cit2] – лимонная кислота, [Ox2] – щавелевая кислота, что позволяет в итоге рассчитать значения относительной перенасыщенности и индексы насыщения для всех возможных преципитирующих солей. Этими функциями обладают компьютерные программы EQUIL [22, 23] и JESS [24-26].
Такие подходы на основе классической термодинамики дают лучшие результаты по оценке перенасыщенности мочи, но используют в анализе большее количество исходных химических компонентов мочи (23 параметра в улучшенной версии EQUIL93 [22]). Однако, по-видимому, именно большое число вводимых переменных и связанные с этим трудозатраты мешают, также как и для индекса Тизелиуса, широкому использованию программ EQUIL и JESS.
В тоже время, описанные методы и подходы не способны учесть влияния на процесс кристаллои камнеобразования целой группы веществ более сложной структуры, обладающих способностью модулировать процесс формирования кристаллов и уролитов. Это так называемые макромолекулы мочи, экскретируемые в мочу клетками тубулярного эпителия [27-29]. Среди них – гликопротеид Тамма-Хорсфалла [30-32], гликозаминогликаны [33, 34] остеопонтин (уропонтин) [35-37], нефрокальцин [38, 39], протромбин F1 (фрагмент протромбина) [40, 41], бикунин (фрагмент интер-альфа-ингибитора (I-alpha-I) трипсина) [42, 43] и даже «неидентифицированные биомакромолекулы» [44].
Влияние макромолекул на процесс образования кристаллои камнеобразование довольно сложное. При одних условиях макромолекулы оказывают ингибиторное влияние, при других – промоторное. Например, гликопротеид Тамма-Хорсфалла у здоровых лиц обладает ингибиторным влиянием на нуклеацию и агрегацию кристаллов оксалата кальция. У больных оксалатным уролитиазом, особенно в сочетании с гипероксалатурией и/или гиперкальцийурией, этот белок способен активировать оба эти процесса, а также процесс адгезии микрокристаллов на поверхности эпителия сосочков и чашечек [45]. Другой сложный белок мочи – нефрокальцин способен ингибировать нуклеацию и так же, как белок ТаммаХорсфалла замедляет агрегацию кристаллов. Однако в отличие от здоровых лиц оба этих белка у больных уролитиазом проявляют лишь слабую антиагрегационную активность, а при гиперкальциурии белок Тамма-Хорсфалла может даже ускорять агрегацию кристаллов оксалата кальция [45]. Подобные функциональные различия выявляются среди некоторых фракций гликозаминогликанов. К примеру, гепаран-сульфат мочи здоровых людей активнее ингибирует рост кристаллов оксалата кальция, чем аналогичная фракция, выделенная из мочи больных [46].
Таким образом, инициация процесса кристаллообразования, а в дальнейшем и камнеобразования, зависит от баланса трех важных сил, ответственных за сохранение метастабильного состояния мочи – промоторов, ингибиторов и макромолекул мочи.
В связи с этим возникает необходимость в разработке особых дополнительных методов и подходов в диагностическом исследовании, которые позволили бы выявить этот дисбаланс. Такие методы должны давать интегральную оценку литогенному потенциалу мочи с учетом всех участвующих в кристаллообразовании факторов.
Одним из методов такого рода является метод расчета Боннского индекса риска – Bonn-Risk-Index (BRI) при оксалатном уролитиазе[47]. BRI численно соответствует количеству ионов оксалата [Ox2] (или мМоль оксалата аммония), требуемого для индукции образования кристаллов оксалата кальция в 200,0 мл суточной мочи, что регистрируется по началу падения концентрации ионизированного кальция [Ca2+].
Однако в процессе сбора суточной мочи может происходить изменение свойств макромолекул мочи и/или других модификаторов кристаллообразования. Предварительная фильтрация мочи, применяемая в этом методе, может менять литогенные свойства мочи, поскольку при этом удаляются нативные кристаллы оксалата кальция. Отсутствие стандартизации условий запуска кристаллообразования делает невозможным нивелировать влияние различных исходных концентраций главных взаимодействующих ионов [Ca2+] и [Ox2] на характер процесса формирования кристаллов, что, в конечном счете, не дает полного представления о состоянии системы промоторы-ингибиторы у пациента.
В связи с этим предложен метод для оценки динамики кристаллообразования, с помощью которого можно оценить результирующий эффект взаимовоздействия ингибиторов и промоторов, включая макромолекулы мочи и другие субстанции, способные влиять на этот процесс. При этом используется нативная утренняя моча пациентов, в которой присутствуют естественные потенциальные модификаторы кристаллообразования (например, макромолекулы мочи и другие). Кроме того, исключен прямой эффект различия концентраций главных ионов, формирующих кристаллы оксалата кальция, так как индукция кристаллообразования выполняется при стандартных условиях (при одинаковых стартовых концентрациях [Ca2+] и [Ox2]).
МАТЕРИАЛЫ И МЕТОДЫ
Кристаллообразующую активность мочи исследовали у 111 пациентов (в возрасте 23 до 67 лет) с оксалатным уролитиазом, который у 68 человек (39 мужчин и 29 женщин) имел нерецидивное течение. У 43 пациентов (27 мужчин и 16 женщин) была выявлена рецидивная форма оксалатного уролитиаза.
В качестве контроля исследовались биохимические показатели 86 практически здоровых людей (38 мужчины и 48 женщин) в возрасте от 21 года до 62 лет, не имевших урологических заболеваний.
Скорость образования кристаллов оксалата кальция оценивали по разработанной в лаборатории оригинальной методике [48]. Регистрировали показатель начальной скорости кристаллообразования (НСК) по динамике падения концентрации ионов кальция с использованием прибора Microlyte 3+2 (Kone, Финляндия) при добавлении в модельную систему мочи больных оксалатным уролитиазом.
Таблица 1. Индексы риска камнеобразования у здоровых лиц и больных оксалатным уролитиазом
| Индекс | Здоровые | Больные | P | AUC | ДЧ* (%) |
ДС* (%) |
||
|---|---|---|---|---|---|---|---|---|
| M ± m | n1 | M ± m | n2 | |||||
| ОПМ(СаОх) | 7,74 ± 0,702 | 55 | 19,54 ± 1,193 | 90 | <0,00001 | 0,865 | 67,8 | 87,5 |
| НСК | 1,58 ± 0,020 | 83 | 1,69 ± 0,017 | 109 | <0,00005 | 0,685 | 59,6 | 76,2 |
| ОПМ(СаОх)-НСК | 12,39 ± 1,205 | 55 | 32,12 ± 2,049 | 90 | <0,00001 | 0,875 | 74,4 | 85,7 |
| CaOxCitr | 0,50 ± 0,079 | 97 | 1,69 ± 0,379 | 91 | <0,01 | 0,806 | 75,8 | 75,0 |
| CaOxCitr-НСК | 0,81 ± 0,131 | 67 | 2,85 ± 0,589 | 92 | <0,005 | 0,811 | 77,2 | 75,0 |
| AP(CaOx) | 1,51 ± 0,168 | 67 | 2,88 ± 0,217 | 92 | <0,00001 | 0,776 | 70,7 | 75,0 |
| AP(CaOx)-НСК | 2,41 ± 0,280 | 67 | 4,86 ± 0,361 | 92 | <0,00001 | 0,787 | 75,0 | 73,5 |
р статистический показатель достоверности различия между здоровыми (n1) и больными (n2); AUC (Area Under Curve) – площадь под ROC-кривой; ДЧ – диагностическая чувствительность (Sensitivity) и ДС – диаг ностическая специфичность (Specificity);
*P <0,0001 при указанных значениях AUC, ДЧ и ДС;
ОПМ(СаОх) – индекс относительной перенасыщенности мочи, рассчитанный с помощью программы EQUIL2;
НСК – индекс начальной скорости кристаллообразования в значениях остаточной концентрации ионизиро ванного кальция (мМоль/л), регистрируемой через 10 сек. после индукции кристаллообразования;
ОПМ(СаОх)-НСК – комбинированный индекс, где ОПМ(СаОх)-НСК = ОПМ(СаОх) х НСК; CaOxCitr – комбинированный индекс, равный [Ca2+] x [Ox2] / [Citr2]; AP(CaOx) – индекс Тизелиуса (см. формулу в тексте);
AP(CaOx)-НСК комбинированный индекс, равный AP(CaOx) х НСК
Цельная моча в большинстве подобных экспериментальных систем не используется, вследствие ее высокой ингибиторной активности [49]. Требуется разведение мочи для достижения полной ионизации кальция и доведения его уровня до стандартной концентрации [49, 50]. Учитывая это обстоятельство, в данной работе условия измерения были подобраны таким образом, чтобы достичь одинаковой стартовой концентрации общего кальция (4,0 мМоль/л) и практически полной его ионизации.
Для исследования использовали порцию утренней мочи. Всем больным проводили клинический анализ мочи с микроскопией осадка. При наличии лабораторных признаков воспалительного процесса мочу пациента исключали из дальнейшего исследования.
Перед исследованием мочу разводили в 5 раз физиологическим раствором. Концентрацию ионизированного кальция (Ca2+) в разведенной моче больных доводили 10% раствором CaCl2 до 4 мМоль/л. Реакцию запускали добавлением равного объема двух миллимолярного раствора оксалата натрия при постоянном перемешивании на магнитной мешалке. Скорость падения ионов Ca2+ в системе регистрировали через 10 сек, 5 мин, 10 мин и 30 мин после инициации кристаллообразования.
Расчет индекса относительной перенасыщенности мочи (ОПМ) при оксалатном уролитиазе [индекс ОПМ(CaOx)] проводили с помощью программы EQUIL2 [22, 23]. Входными данными служили величины концентрации в моче калия, натрия, кальция, магния, фосфатов, оксалатов, цитратов, мочевой кислоты и значения рН. Производили расчет параметров образующихся в данных условиях и теоретически возможных ионных пар и, в конечном счете – индекса относительной перенасыщенности мочи для выбранной пары ионов (в нашем случае – ионов [Ca+2] и [Ox-2]).
Рассчитывали также индекс Тизелиуса [AP (CaOx)] [19] и сходный с ним упрощенный концентрационный коэффициент – индекс CaOxCitr, предложенный нами. Последний представляет собой отношение концентраций в моче (мМоль/л) основных промоторов и ингибиторов кальций-оксалатного кристаллообразования и рассчитывается как: индекс CaOxCitr = [Ca2+] x [Ox2] / [Citr2].
Для оценки диагностической чувствительности и диагностической специфичности данного индекса был использован ROC-анализ (Receiver Operator Characteristic – операционная характеристика приёмника, технический термин и статистический метод, заимствованный из систем обработки сигналов). ROC-анализ выполнялся с помощью программы MedCalc.v12.3.0.0.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Учитывая большие возможности программы EQUIL2, эту программу использовали для расчета индекса ОПМ(CaOx) у здоровых лиц и больных оксалатным уролитиазом. Высокая точность вычислений с помощью программы EQUIL2 была подтверждена эмпирическими данными лабораторных исследований физико-химических свойств растворов в эксперименте, а также результатами ряда клинических наблюдений [51-54].
Метастабильное состояние мочи зависит от сложного взаимодействия различных видов ионов, растворенных веществ и их производных. На метастабильное состояние мочи оказывает влияние степень диссоциации веществ, ионная сила и активность ионов, что, в конечном счете, определяет склонность литогенных соединений к формированию твердых фаз, то есть кристаллов.
Алгоритм оценки метастабильности мочи, реализованный в программе EQUIL2 [22, 23], учитывает взаимовлияние ионов друг на друга в моделях термодинамического равновесия, описывающих поведение каждой ионной пары при данных условиях температуры, ионного окружения и значениях рН.
Результаты значений всех индексов и их производных представлены в таблице 1 и на рисунках 1 и 2.
Можно видеть, что средние значения всех индексов статистически значимо отличались у больных и здоровых. Так, индекс относительной перенасыщенности мочи – индекс ОПМ(CaOx) – у больных оксалатным уролитиазом более, чем вдвое превышал соответствующий показатель у здоровых лиц (19,54 ± 1,193 и 7,74 ± 0,702 соответственно, р < 0,00001).
Однако для использования всех указанных индексов в диагностических целях требуется определять для каждого из них значения диагностической чувствительности и диагностической специфичности. Это выполняется с помощью построения ROC-кривых с вычислением величин порога или точки отсечения (cut-off value).
В результате этого анализа строится ROC-кривая, отражающая зависимость количества верно классифицированных положительных примеров (наличие признака или заболевания) от количества неверно классифицированных отрицательных примеров (отсутствие признака или заболевания).
В идеальном случае график ROC-кривой должен проходить через верхний левый угол, где доля истинно положительных случаев составляет 100% (идеальная чувствительность), а доля ложно положительных примеров равна нулю (идеальная специфичность). Поэтому чем ближе кривая к верхнему левому углу, тем выше предсказательная способность модели. Наоборот, чем ближе кривая к диагональной прямой (Рис. 2А, ROC-кривая для индекса НСК), тем менее эффективна модель при различении двух классов (например, больных и здоровых).
Применение индекса ОПМ(CaOx) в ROC-анализе показало, что диагностическая специфичность его была достаточно высокой – 87,5% при умеренно выраженной диагностической чувствительности в 67,8%, (табл. 1), р < 0,0001).
Как отмечалось выше, индекс ОПМ(CaOx) описывает только физико-химические взаимодействия ионов, не учитывая влияния других активных модификаторов мочи на процесс кристаллообразования, например, группы макромолекул мочи.
В связи с этим был использован метод, дающий возможность непосредственной регистрации параметров скорости формирования кристаллов. Для интегральной оценки активности образования кристаллов использовали такой физико-химический параметр, как показатель начальной скорости кристалообразования (НСК). Этот показатель был выбран в силу того, что, как ранее было нами отмечено [48], гиперкальциурия у больных оксалатным уролитиазом, по-видимому, способна повреждать защитные механизмы, направленные на поддержание метастабильности мочи, что проявляется замедлением начальной скорости кристаллообразования.
Показатель начальной скорости кристалообразования (НСК), выражали величиной остаточной концентрации ионизированного кальция, которую регистрировали через 10 сек. после индукции кристаллообразования. У больных оксалатным уролитиазом этот показатель был выше (1,69 ± 0,017 мМоль/л), чем у здоровых (1,58 ± 0,020 мМоль/л, р< 0,00005), хотя диагностическая чувствительность показателя начальной скорости кристалообразования (НСК) была невысокой и составляла 59,6%, при диагностической специфичности 76,2% (табл. 1, р < 0,0001)
Следует подчеркнуть, что оба показателя характеризуют разные независимые процессы. Так, индекс ОПМ(CaOx) указывает на степень перенасыщения мочи и уровень ее метастабильности, а показатель НСК отражает динамику процесса индуцированного кристаллообразования по скорости включения ионизированного кальция в состав образующихся кристаллов оксалата кальция.
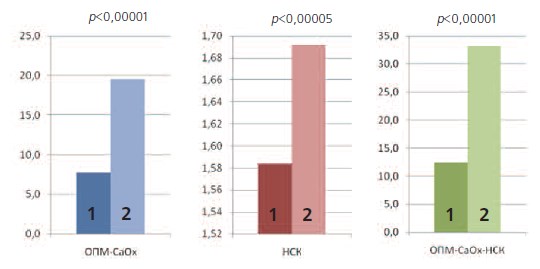
Рис. 1. Диагностические индексы для здоровых лиц (1) и больных оксалатным уролитиазом (2). ОПМ-СаОх – индекс относительной перенасыщенности мочи, рассчитанный с помощью программы EQUIL2; НСК – индекс начальной скорости кристаллообразования в значениях остаточной концентрации ионизированного кальция (мМоль/л), регистрируемой через 10 сек. после индукции кристаллообразования; ОПМ-СаОх-НСК – комбинированный индекс, рассчитанный как произведение индексов ОПМ-СаОх и НСК
Поэтому с целью повышения качества диагностики свойства каждого из этих индексов были объединены в единый комплексный показатель – индекс ОПМ(СаОх)-НСК, который вычислялся как ОПМ(СаОх) х НСК.
Полученный комбинированный индекс ОПМ(СаОх)-НСК у здоровых (12,39±1,205; n=55) и больных (32,12±2,049; n=90) имел выраженные отличия при высокой степени статистической достоверности (р < 0,00001, фактически р = 0,00000000001).
Сочетание свойств обоих показателей в комбинированном индексе ОПМ(СаОх)-НСК дает повышение уровня диагностической чувствительности с 59,6% (при использовании только индекса НСК) до 74,4% (р = 0,029) при сохранении достаточно высокой диагностической специфичности – 85,7% (табл. 1, рис. 2)
Что касается других индексов – CaOxCitr, AP(CaOx) и их сочетаний с индексом НСК, то при почти одинаковых с индексом ОПМ(СаОх)-НСК значениях показателей диагностической чувствительности (70,7 – 77,2%), показатели диагностической специфичности у них не смогли превысить значения 85,7%, характерного для индекса ОПМ(СаОх)-НСК (табл. 1, рис. 2Б).
Визуальное сравнение кривых ROC не всегда позволяет выявить наиболее эффективную модель классификации. Чаще всего методом сравнения ROC-кривых является оценка площади под кривыми, (Area Under Curve) – показатель AUC. Существует экспертная шкала для значений AUC, по которой можно судить о качестве модели [55], используемой для классификации.
Согласно этой шкале модель с использованием только показателя НСК относится к моделям среднего качества (значение AUC в пределах 0,6-0,7). К моделям с хорошим качеством классификации признаков (AUC в пределах 0,7-0,8) относятся индексы AP(CaOx) и AP(CaOx)-НСК. Очень хорошим качеством классификации обладают индексы имеющие AUC в пределах 0,8-0,9.
Можно видеть, что индексы ОПМ(СаОх) и особенно ОПМ(СаОх)НСК, имеющие значения AUC 0,865 и 0,875 соответственно, обладают поэтому более высоким качеством классификации и различения больных и здоровых, по сравнению с индексами CaOxCitr и CaOxCitr-НСК, имеющими значения AUC, близкие к 0,8 (табл. 1, рис. 2А).
Однако применение комбинированного индекса ОПМ(СаОх)-НСК не позволило четко дифференцировать больных с рецидивной формой (37 больных) от пациентов со спорадическим типом оксалатного уролитиаза (56 больных). Уровень диагностической чувствительности составлял 57,1%, диагностической специфичности 54,1% (р =0,65), значение AUC было равно 0,528, что характерно для моделей классификации неудовлетворительного качества.
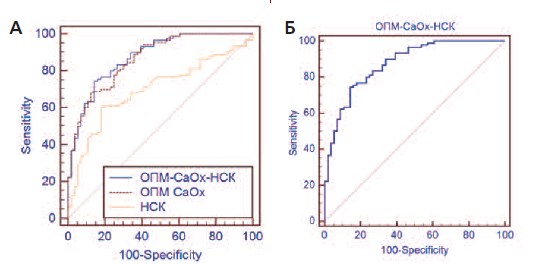
Рис. 2. ROC-кривые диагностических индексов. А сравнение ROC-кривых для трех индексов: НСК, ОПМ(СаОх) и ОПМ(СаОх)-НСК Б – ROC-кривая индекса ОПМ(СаОх)-НСК с оптимальными значениями диагностической чувствиельности (74,4%) и диагностической специфичности (85,7%) при значении точки отсечения 18,75
По-видимому, в литогенезе рецидивной формы оксалатного уролитиаза в большей степени участвуют другие механизмы, способные изменять состав и пассаж внутриканальцевой мочи, активируя тем самым нуклеацию и рост кристаллов оксалата кальция [56]. Возможно, патогенетические механизмы этой формы уролитиаза способны проявлять себя, нарушая адгезивные свойства уротелия с образованием бляшек Рэндалла [57, 58], либо повреждая другие процессы, ответственные за периодичность формирования уролитов и требующие дальнейшего изучения.
Тем не менее, сочетание различных диагностических подходов дает возможность выбрать комбинированный диагностический индекс, основанный на оценке степени перенасыщенности мочи и начальной скорости кристаллообразования – ОПМ(СаОх)-НСК. Этот индекс позволяет более детально оценивать литогенные свойства мочи у больных оксалатным уролитиазом, характеризуется оптимальным сочетанием достаточно высоких значений диагностической чувствительности и специфичности. С практической точки зрения альтернативой ему может быть выбор более простого индек-са CaOxCitr, дающего удовлетворительные результаты по диагностической чувствительности и специфичности.
ЗАКЛЮЧЕНИЕ
Предложенные подходы могут быть использованы для оценки риска развития оксалатной формы МКБ наряду с общепринятым определением метаболических литогенных факторов, а также для контроля качества проводимого профилактического лечения.
ЛИТЕРАТУРА
1. Trinchieri A. (Epidemiological trends in urolithiasis: impact on our health-care systems. // Urol Res. 2006. Vol. 34. P. 151–156.
2. Ansari MS, Gupta NP. Impact of socioeconomic status in etiology and management of urinary stone disease. // Urol Int. 2003. Vol. 70. P. 255–261.
3. Tiselius HG. Epidemiology and medical management of stone disease. // BJU Int. 2003. Vol. 91. P.:758–767.
4. Hesse A, Brandle E, Wilbert E, Köhrmann KU, Alken P. Study on the prevalence and incidence of urolithiasis in Germany comparing the years 1979 vs. 2000. // Eur Urol. 2003. Vol. 44. P. 709–713.
5. Romero V, Akpinar H, Assimos DG. Kidney Stones: A Global Picture of Prevalence, Incidence, and Associated Risk Factors. // Rev Urol. 2010. Vol. 12, N 2/3. P. 86-96.
6. Lee MC, Bariol SV. Changes in upper urinary tract stone composition in Australia over the past 30 years. // BJU Int. 2013. Vol. 112, Suppl 2. P. 65-68.
7. López M, Hoppe B. History, epidemiology and regional diversities of urolithiasis. // Pediatr Nephrol. 2010. Vol. 25, N 1 P. 49–59.
8. Berg W, Schanz H, Eisenwinter B, Schorch P. The incidence distribution and development of a trend of urinary stone substances: an evaluation of the data on over 210,000 urinary stone analyses from the area of the former DDR. // Urologe A. 1992. Vol. 31. P. 98–102.
9. Schubert G. Stone analysis. // Urol Res. 2006. Vol. 34. P. 146–150.
10. Smith LH. The medical aspects of urolithiasis: an overview. // J Urol. 1989. Vol. 141, N 2. P. 707-710.
11. Mandel NS, Mandel GS. Urinary tract stone disease in the United States veteran population, II. Geographical analysis of variations in composition. // J Urol. 1989. Vol. 142. P. 1516-1521.
12. Lemann JJr. Pathogenesis of idiopathic hypercalciuria and nephrolithiasis. // In: Coe FL, Favus MJ, eds. Disorders of bone and mineral metabolism. New York: Raven Press, 1992. P. 685-706.
13. Batinić D, Milosević D, Blau N, Konjevoda P, Stambuk N, Barbarić V,Subat-Dezulović M, Votava-Raić A, Nizić L, Vrljicak K. Value of the urinary stone promoters/inhibitors ratios in the estimation of the risk of urolithiasis.// J Chem Inf Comput Sci. 2000. Vol. 40. P. 607–610.
14. Laube N, Rodgers A, Allie-Hamdulay S, Straub M. Calcium oxalate stone formation risk—a case of disturbed relative concentrations of urinary components. // Clin Chem Lab Med. 2008. Vol. 46. P. 1134–1139.
15. Berg W, Mäurer F, Brundig P, Bothor C, Schulz E. Possibilities of computing urine parameters as a means of classification of normals and patients suffering from calcium oxalate lithiasis. // Eur Urol. 1983. Vol. 9. P. 353–358.
16. King JS Jr, O’Connor FJ Jr, Smith MJ, Crouse L. The urinary calcium magnesium ratio in calcigerous stone formers. // Invest Urol. 1968. Vol. 6. P. 60–65.
17. Parks JH, Coe FL: A urinary calcium-citrate index for the evaluation of nephrolithiasis. // Kidney Int. 1986. Vol. 30. P. 85–90.
18. Tiselius HG. Different estimates of the risk of calcium oxalate crystallization in urine. // Eur Urol. 1983. Vol. 9. P. 231–234.
19. Knoll T. Epidemiology, pathogenesis and pathophysiology of urolithiasis. // Eur Urol Suppl. 2010. Vol. 9. P. 802–806.
20. Tiselius HG. Risk formulas in calcium oxalate urolithiasis. // World J Urol. 1997. Vol. 15. P. 176–185.
21. Tiselius HG. An improved method for the routine biochemical evaluation of patients with recurrent calcium oxalate stone disease. // Clin Chim Acta. 1982. Vol. 122. P. 409–418.
22. Brown CM, Ackermann DK, Purich DL. EQUIL93: a tool for experimental and clinical urolithiasis. // Urol Res. 1994. Vol. 22. P. 119–126.
23. Werness PG, Brown CM, Smith LH, Finlayson B. EQUIL 2: a basic computer program for the calculation of urinary supersaturation. // J Urol. 1985. Vol. 134. P. 1242–1244.
24. May PM, Murray K: JESS, a joint expert specification system-I. // Talanta. 1991. Vol. 38. P. 1409–1417.
25. May PM, Murray K. JESS, a joint expert specification system— II. The thermodynamic database. // Talanta. 1991. Vol. 38. P. 1419–1426.
26. Rodgers A, Allie-Hamdulay S, Jackson G. Therapeutic action of citrate in urolithiasis explained by chemical specification: increase in pH is the determinant factor. // Nephrol Dial Transplant. 2006. Vol. 21. P. 361–369.
27. Worcester EM. Urinary calcium oxalate crystal growth inhibitors. // J Am Soc Nephrol. 1994. Vol. 5, Suppl. 1. P. 46–53.
28. Aggarwal KP, Narula S, Kakkar M, Tandon C. Nephrolithiasis: molecular mechanism of renal stone formation and the critical role played by modulators. // Bio Med Res Int. 2013. Vol. 2013. 21 p.
29. Khan SR, Kok DJ. Modulators of urinary stone formation. // Front Biosci. 2004. Vol. 9. P. 1450–1482.
30. Gokhale JA, Glenton PA, Khan SR. Characterization of TammHorsfall protein in a rat nephrolithiasis model. // J Urol. 2001. Vol. 166. P. 1492–1497.
31. Mo L, Huang HY, Zhu XH, Shapiro E, Hasty DL, Wu XR. TammHorsfall protein is a critical renal defense factor protecting against calcium oxalate crystal formation. // Kidney Int. 2004. Vol. 66. P. 1159–1166.
32. Hess B. The role of Tamm-Horsfall glycoprotein and nephrocalcin in calcium oxalate monohydrate crystallization processes. // Scanning Microsc. 1991. Vol. 5. P. 689–695.
33. Miyake O,Yoshimura K, Tsujihata M, Yoshioka T, Koide T, Takahara S, Okuyama A. Possible causes for the low prevalence of pediatric urolithiasis // Urology. 1999. Vol. 53, N 6. P. 1229-1234.
34. Erturk E, Kiernan M, Schoen SR. Clinical association with urinary glycosaminoglycans and urolithiasis. // Urology. 2002. Vol. 59, N 4. P. 495–499.
35. Christensen B, Petersen TE, Sørensen ES. Posttranslational modification and proteolytic processing of urinary osteopontin. // Biochem J. 2008. Vol. 411. P. 53–61.
36. Wang LJ, Zhang W, Qiu SR, Zachowicz WJ, Guan X, Tang R, Hoyer JR, De Yoreo JJ, Nancollas GH. Inhibition of calcium oxalate monohydrate crystallization by the combination of citrate and osteopontin. // J Cryst Growth. 2006. Vol. 291. P. 160–165.
37. Konya E, Umekawa T, Iguchi M, Kurita T. The role of osteopontin on calcium oxalate crystal formation. // Eur Urol. 2003. Vol. 43. P. 564–571.
38. Nakagawa Y. Properties and function of nephrocalcin: mechanism of kidney stone inhibition or promotion. // Keio J Med. 1997. Vol. 46, N 1. P. 1–9.
39. Lieske J.C., Deganello S. Nucleation, adhesion, and internalization of calcium-containing urinary crystals by renal cells. // J Am Soc Nephrol. 1999. Vol. 10, Suppl. 14. P. 422-429.
40. Grover PK, Ryall RL. Inhibition of calcium oxalate crystal growth and aggregation by prothrombin and its fragments in vitro: relationship between protein structure and inhibitory activity // Eur J Biochem. 1999. Vol. 263, N 1. P. 50-56.
41. Cook AF, Grover PK, Ryall RL. Face-specific binding of prothrombin fragment 1 and human serum albumin to inorganic and urinary calcium oxalate monohydrate crystals. // BJU Int. 2009. Vol. 103, N 6. P. 826-835.
42. Médétognon-Benissan J, Tardivel S, Hennequin C, Daudon M, Drüeke T, Lacour B. Inhibitory effect of bikunin on calcium oxalate crystallization in vitro and urinary bikunin decrease in renal stone formers. // Urol Res. 1999. Vol. 27, N 1. P. 69–75.
43. Atmani F, Khan SR. Role of urinary bikunin in the inhibition of calcium oxalate crystallization. // J Am Soc Nephrol. 1999. Vol . 10, N 14. P. 385–388.
44. Sørensen S, Hansen K, Bak S, Justesen SJ. An unidentified macromolecular inhibitory constituent of calcium oxalate crystal growth in human urine. // Urol Res. 1990. Vol. 18. P. 373–379.
45. Worcester EM. Urinary calcium oxalate crystal growth inhibitors. // J Am Soc Nephrol. 1994. Vol. 5, Suppl 1. P. 46-53.
46. Shum DK, Gohel MD. Separate effects of urinary chondroitin sulphate and heparan sulphate on the crystallization of urinary calcium oxalate: differences between stone formers and normal control subjects. // Clin Sci. 1993. Vol. 85, N 1. P. 33-39.
47. Laube N, Schneider A, Hesse A. A new approach to calculate the risk of calcium oxalate crystallization from unprepared native urine. // Urol Res. 2000. Vol. 28. P. 274–280.
48. Голованов С.А., Дрожжева В.В. Кристаллообразующая активность мочи при оксалатном уролитиазе // Экспериментальная и клиническая урология. 2010. N 2. С. 24-29
49. Tiselius H.-G., Fornander A.M., Nilsson A. Inhibition of calcium oxalate crystallization in urine // Urol Res. 1987. Vol. 15. P. 83-86.
50. Sarig S, Garti M, Azoury R, Wax Y, Perlberg P. A Method for discrimination between calcium oxalate stone formers and normals // J Urol. 1982. Vol. 128. P. 645-649.
51. Ogawa Y, Hatano T. Comparison of the Equil2 program and other methods for estimating the ion-activity product of urinary calcium oxalate: a new simplified method is proposed.// Int J Urol. 1996. Vol. 3, N 5. P. 383-385.
52. Hoppe B, Leumann E, von Unruh G, Laube N, Hesse A. Diagnostic and therapeutic approaches in patients with secondary hyperoxaluria. // Front Biosci. 2003. Vol. 8. P. 437-443.
53. Agrawal V, Liu XJ, Campfield T, Romanelli J, Enrique Silva J, Braden GL. Calcium oxalate supersaturation increases early after Roux-en-Y gastric bypass. // Surg Obes Relat Dis. 2014. Vol. 10, N 1. P. 88-94.
54. Milošević D1, Batinić D, Turudić D, Batinić D, Topalović-Grković M, Gradiški IP. Demographic characteristics and metabolic risk factors in Croatian children with urolithiasis. // Eur J Pediatr. 2014. Vol. 173, N 3. P. 353-359.
55. Файнзильберг Л.С., Жук Т.Н. Гарантированная оценка эффективности диагностических тестов на основе усиленного ROC-анализа. // Управляющие системы и машины. 2009. N 5. С. 3–13.
56. Robertson WG. Potential role of fluctuations in the composition of renal tubular fluid through the nephron in the initiation of Randall's plugs and calcium oxalate crystalluria in a computer model of renal function. // Urolithiasis. 2014. Vol. 43, Suppl. 1. P. 93-107.
57. Evan A1, Lingeman J, Coe FL, Worcester E. Randall's plaque: pathogenesis and role in calcium oxalate nephrolithiasis. // Kidney Int. 2006 . Vol. 69, N 8. P. 1313-1318.
58. Matlaga BR1, Coe FL, Evan AP, Lingeman JE. The role of Randall's plaques in the pathogenesis of calcium stones. // J Urol. 2007. Vol. 177, N 1. P. 31-38.







