Основной причиной, заставляющей мужчин с доброкачественной гиперплазией предстательной железы (ДГПЖ) обращаться к врачу, являются нарушения мочеиспускания, проявляющиеся как в виде затруднения мочеиспускания (обструктивная симптоматика), так и в симптомах гиперактивности мочевого пузыря (ирритативная симптоматика), что существенно ухудшает качество жизни этих больных. Исследования последних лет свидетельствуют, что важную роль в патогенезе дисфункции мочевого пузыря у этих больных играет фактор хронической ишемии мочевого пузыря [1-3], как индуцированной расстройством микроциркуляции в стенке гипертрофированного мочевого пузыря, обусловленным инфравезикальной обструкцией (ИВО), так и вследствие нарушения кровоснабжения тазовых органов вследствие сосудистых заболеваний без ИВО, что приводит к формированию гиперактивности мочевого пузыря (ГАМП) [4-6]. В литературе имеются данные, свидетельствующие, что терапевтическое действие препаратов, используемых для лечения расстройства мочеиспускания у больных ДГПЖ (α-адреноблокаторы, ингибиторы 5α-редуктазы, ингибиторы фосфодиэстеразы-5), в определенной степени связано с улучшением кровоснабжения мочевого пузыря [3, 7, 8]. Эти данные позволяют полагать, что медикаментозная нейтрализация метаболических нарушений, обусловленных хронической ишемией, может препятствовать развитию дисфункции мочевого пузыря при ИВО.
В литературе имеются публикации, подтверждающие эту точку зрения. Описано улучшение функциональных показателей обструктивного мочевого пузыря при действии препаратов, улучшающих синтез АТФ в клетках [9, 10], улучшающих микроциркуляцию [11], препаратов с антиоксидантным и антигипоксическим действием [12-14], блокаторов кальциевых каналов [15, 16]. Нами в предыдущих исследованиях было доказано существенное улучшение метаболических показателей и функционального состояния обструктивного мочевого пузыря при терапии синтетическим антиоксидантом под условным названием SkQR1, защищающим митохондрии от ишемического повреждения [17].
Эти данные свидетельствуют о перспективности включения противоишемической терапии в комплекс медикаментозного лечения расстройств мочеиспускания у больных ДГПЖ. Однако, для подавляющего большинства препаратов их эффективность изучена в экспериментальных исследованиях и эти препараты не разрешены для клинического применения. В связи с этим, в данном экспериментальном исследовании мы поставили задачу оценить эффективность комплекса фармакопейных препаратов с антиоксидантным и противоишемическим действием, разрешенных для использования в клинической практике, для предупреждения дисфункции мочевого пузыря при экспериментально вызванной ИВО у крыс.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование было проведено в 5 сериях опытов на 28 самках белых беспородных крыс массой 260290 г. Самки крыс были выбраны в связи с легкостью моделирования у них ИВО, в отличие от самцов, у которых имеются серьезные трудности в доступе к уретре за пределами предстательной железы и ее катетеризации, что делает модель ИВО у самок крыс общепринятой для моделирования расстройств мочеиспускания, имитирующих аналогичные расстройства при ДГПЖ [18].
Все эксперименты проводили с соблюдением принципов Европейской конвенции о гуманном отношении к животным в условиях общего обезболивания (ингаляция паров эфира или внутрибрюшинное введение тиопентала натрия в дозе 45-50 мг/кг). Эвтаназия животных производилась избыточным введением наркотического вещества (эфир или тиопентал натрия в зависимости от условий эксперимента).
1-ю серию (контроль) составили 5 интактных крыс, у которых не проводили никаких манипуляций. Во 2-й серии (6 крыс) моделировали ИВО путем дозированного сужения предпузырного отдела уретры. Для этого в условиях эфирного наркоза выполняли нижнесрединную лапаротомию, выделяли мочевой пузырь, находящийся у крыс в брюшной полости, и предпузырный отдел мочеиспускательного канала. Уретру катетеризировали через наружное отверстие мочеиспускательного канала кубитальным катетером 18G (наружный диаметр 1,3 мм) и наполняли мочевой пузырь. Под предпузырный отдел уретры подводили лигатуру, которую завязывали на катетере. Катетер удаляли, после чего контролировали, не привела ли манипуляция к полной обструкции мочевого пузыря (надавливали на мочевой пузырь и наблюдали выделение введенного физиологического раствора из наружного отверстия уретры). Рану брюшной полости ушивали. В 3-й серии (5 крыс) после аналогичного моделирования ИВО животные со следующего дня получали терапию α-адреноблокатором доксазозином, растворенным в питьевой воде (расчетная суточная дозировка препарата – 0,05 мг/кг/сутки). Этот препарат был выбран в связи с лучшей растворимостью в воде, а также исходя из данных литературы об отсутствии существенных различий в его эффективности по сравнению с другими препаратами этой фармакологической группы [19, 20]. В 4-й серии (6 крыс) для терапии расстройств мочеиспускания использовали комплекс препаратов с противоишемическим действием: α-токоферол добавлялся к стандартному комбикорму в суточной дозе 10 мг/кг, трентал, антиоксидант мексидол и блокатор кальциевых каналов дилтиазем добавляли в питьевую воду в суточной дозировке 4 мг/кг, 5 мг/кг и 2 мг/кг соответственно. В 5-й серии (6 крыс) проводили комбинированную терапию α-блокатором и комплексом противоишемических препаратов в аналогичных дозировках.
Животные всех опытных групп подвергались исследованию через 1 месяц после моделирования ИВО.
Оценку кровоснабжения и функциональной активности мочевого пузыря проводили с помощью разработанной в НИИ урологии совместно с НПФ «Биола» (Россия) методики высокочувствительной импедансометрии с гармоническим анализом микроколебаний биоимпеданса, позволяющей оценить состояние микроциркуляции органа и его сократительную активность [21]. Спектральный анализ этих колебаний позволяет выделить пик на частоте сердцебиений, называемый С1, характеризующий состояние микроциркуляции в исследуемом органе. Одновременно определяли функциональное состояние мочевого пузыря по данным динамической регистрации внутрипузырного давления. Исследование проводили как на фоне опорожненного мочевого пузыря, так и в процессе инфузионной цистометрии, для осуществления которой мочевой пузырь пунктировали укороченным внутривенным катетером G18 (наружный диаметр 1,3 мм), который через трехходовой кран соединяли с системой для инфузии мочевого пузыря и с датчиком давления (рис. 1).
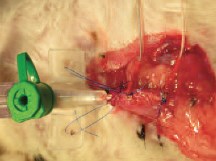
Рис. 1. Внешний вид мочевого пузыря, подготовленного для функционального исследования
Выраженность клеточного повреждения в обструктивном мочевом пузыре в условиях ИВО и терапии определяли по степени ферментурии и активности ферментов в стенке органа. Информативность этих параметров была нами доказана в предыдущих исследованиях [22]. Для сбора мочи животных на сутки помещали в обменные клетки. В суточной моче определяли активность трансаминаз (АЛТ и АСТ), щелочной фосфатазы (ЩФ), лактатдегидрогеназы (ЛДГ), гамма-глутамилтранспептидазы (ГГТП), холинэстеразы (ХЭ), общей креатинфосфокиназы (КФК). Рассчитывали удельную активность ферментов в пересчете на 1 мМ креатинина мочи. Для определения активности этих ферментов в стенке мочевого пузыря готовили гомогенат ткани в физиологическом растворе при соотношении раствор/ ткань 10:1. В нем определяли активность вышеуказанных ферментов в пересчете на 1 мг белка гомогената. Определение активности ферментов проводили на биохимическом анализаторе «Advia 1200» (фирма Bayer-Simens, ФРГ) с использованием стандартных наборов реактивов.
В конце эксперимента удаляли мочевой пузырь, определяли его массу взвешиванием на электронных весах “Acculab” (США) и брали образцы ткани для гистологического исследования с окраской срезов гематоксилином и эозином.
Статистическую обработку цифрового материала проводили с помощью компьютерных программ MS Excel 2007 и Statistica 8.0. Групповые значения показателей выражали в виде средней арифметической и ошибки средней (М±m). Значимость различий между средними значениями исследуемых групп оценивали по критерию t Стьюдента. Статистически значимыми считали различия при p< 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Через 1 месяц после моделирования ИВО у всех крыс опытных групп выявляли выраженную гипертрофию мочевого пузыря. Масса органа возрастала с 103±13 мг (у интактных животных) до 463±87 мг в группе крыс с ИВО без терапии, до 695±122 мг в группе с ИВО на фоне терапии доксазозином, до 318±49 мг при терапии комплексом противоишемических препаратов и до 403±73 мг при комбинированной терапии ИВО. Различия по сравнению с интактными животными во всех опытных группах оказались высокодостоверными (p< 0,001), тогда как между группами достоверных различий не выявили в связи с большим разбросом индивидуальных значений. Гистологическое исследование подтвердило формирование выраженной гипертрофии детрузора во всех опытных группах, что проявлялось в гипертрофии гладкомышечных клеток и формировании их мощных пучков, окруженных прослойками соединительной ткани.
Исследование состояния уродинамики нижних мочевых путей показало, что степень ИВО во всех опытных группах была примерно одинаковой, о чем свидетельствовали цифры детрузорного давления, при котором начиналось мочеиспускание (табл. 1). Во всех группах они достоверно превышали норму, но между группами статистических различий не выявлено. При этом емкость мочевого пузыря через 1 месяц после формирования ИВО существенно различалась. Неожиданным для нас оказалось значительное перерастяжение мочевого пузыря в группах с терапией доксазозином при снижении тонуса детрузора (Pdet базальное). Емкость мочевого пузыря у крыс этой серии превышала норму в 10-12 раз. В контрольной серии опытов (ИВО без терапии) емкость мочевого пузыря возросла примерно в 2 раза. Терапия комплексом противоишемических препаратов способствовала меньшему ее возрастанию, как при изолированной терапии (p< 0,05), так и в комбинации с доксазозином (p<0,01).
Таблица 1. Показатели уродинамики крыс с ИВО при различных вариантах медикаментозной терапии
| Показатели | Норма | ИВО (контроль) |
ИВО+противоишемический комплекс | ИВО+ доксазозин |
ИВО+доксазозин + противоишемический комплекс |
|---|---|---|---|---|---|
| Pdet базальное (см Н2О) |
2,8±0,2 | 4,1±0.2 | 2,6±0,2* | 0,2±0,1*** | 3,2±0,3 |
| P det при мочеиспускании (см Н2О) |
36,8±2,1 | 48,6±2,6 | 48,2±2,1 | 42,2±1,1 | 54,7±2,2 |
| ΔPdet (см Н2О) Базальное Макс. наполнение |
1,9±0,2 5,3±1,1 |
1,4±0,2 11,8±0,3 |
6,8±2,1* 8,5±0,2* |
0,8±0,1 3,9±0,2*** |
1,3±0,1 4,7±0,2*** |
| Емкость МП (мл) | 0,6±0,1 | 1,2±0,1 | 0,8±0,1* | 9,2±0,3*** | 6,8±0,2*** |
Нарушение функционального состояния мочевого пузыря при моделировании ИВО проявлялось также в формировании его гиперактивности, индикатором которой служило увеличение амплитуды спонтанных колебаний внутрипузырного давления (ΔPdet) вне фазы мочеиспускания. Их амплитуда у крыс с ИВО без терапии при наполнении мочевого пузыря возрастала более чем в 2 раза. У крыс, получавших противоишемическую терапию ΔPdet возрастала по сравнению с нормой, но при его наполнении амплитуда спонтанных сокращений возрастала незначительно, оставаясь достоверно ниже, чем в контрольной группе. В группах животных, получавших доксазозин и комплексную терапию, амплитуда спонтанных колебаний внутрипузырного давления не отличалась от нормальных значений, то есть, не происходило развития гиперактивности детрузора.
При исследовании взаимосвязи улучшения функциональной полноценности обструктивного мочевого пузыря на фоне медикаментозной терапии с состоянием кроснабжения органа выявили неоднозначное влияние разных вариантов лечения. Величина кардиального пика С1 на импедансной спектрограмме органа, являющегося индикатором состояния микроциркуляции, при ИВО достоверно уменьшалась, особенно при максимальном наполнении мочевого пузыря, свидетельствуя о его хронической ишемии. На фоне терапии доксазозином кровоснабжение обструктивного мочевого пузыря не улучшалось, а даже имело тенденцию к ухудшению, тогда как при терапии комплексом противоишемических препаратов происходила достоверная интенсификация микроциркуляции в стенке мочевого пузыря, приближая его параметры к нормальным значениям (табл. 2). Комбинированная терапия крыс с ИВО доксазозином и противоишемическими препаратами улучшала кровоснабжение опорожненного мочевого пузыря, но не препятствовала его ухудшению при максимальном наполнении органа, хотя это ухудшение было менее выражено, чем в группе животных с терапией одним доксазозином (p< 0,05).
Таблица 2. Состояние микроциркуляции (размер пика С1) в стенке обструктивного мочевого пузыря при различных вариантах медикаментозной терапии
| Показатели | Норма | ИВО (контроль) |
ИВО+противоишемический комплекс | ИВО+ доксазозин |
ИВО+доксазозин + противоишемический комплекс |
|---|---|---|---|---|---|
| С1 базальный (мОм) |
33,2±1,7 | 20,3±1,4 | 27,6±1,1* | 12,9±0,5*** | 16,5±0,3** |
| С1 при наполнении МП (мОм) | 31,9±2,1 | 12,7±0,5 | 16,2±0,7* | 7,6±0,2*** | 8,5±0,3*** |
Достоверность различий по сравнению с контролем *-p<0,05, **-p<0,01,***p<0,001.
Выраженность повреждения клеточных структур мочевого пузыря крыс с ИВО оценивали по степени возрастания активности ферментов в моче при уменьшении их активности в стенке органа. В контрольной серии (ИВО без терапии) активность исследованных ферментов в моче достоверно превышала нормальные значения, за исключением ГТПП и ХЭ при снижении активности всех ферментов в гомогенате ткани мочевого пузыря (табл. 3, 4). Противоишемическая терапия, а также терапия доксазозином достоверно снижали выход в мочу цитоплазматических ферментов (АСТ, АЛТ, ЛДГ, КФК), при сохранении высокой ферментативной активности в стенке мочевого пузыря, тогда как активность мембраносвязанных ферментов (ЩФ, ГГТП) и ХЭ достоверно не менялась. Комбинированная терапия дополнительно не улучшала параметры ферментурии по сравнению с использованием препаратов по отдельности.
Таблица 3. Выраженность ферментурии у крыс с ИВО при разных вариантах медикаментозной терапии (МЕ/мМ креатинина)
| Ферменты | Норма | ИВО (контроль) |
ИВО+противоишемический комплекс | ИВО+ доксазозин |
ИВО+доксазозин + противоишемический комплекс |
|---|---|---|---|---|---|
| АСТ | 1,5±0,3 | 2,9±0,3 | 0,6±0,1*** | 1,1±0,1** | 2,0±0,2 |
| АЛТ | 1,1±0,4 | 3,3±0,5 | 0,5±0,1*** | 0,9±0,1*** | 5,0±0,6 |
| ЩФ | 25,1±5,3 | 59,1±16,2 | 53,65±9,1 | 15,4±2,6* | 350,5±119,3* |
| ГГТП | 72,7±14,2 | 71,5±12,2 | 90,3±6,9 | 18,7±1,9*** | 100,3±27,8 |
| ЛДГ | 4,9±1,3 | 22,3±2,7 | 8,5±0,6** | 5,1±0,3*** | 100,6±28,3* |
| ХЭ | 11,9±3,0 | 8,1±1,8 | 3,90±0,6 | 3,6±0,8 | 7,4±1,3 |
Достоверность различий по сравнению с контролем: * -p<0,05, ** p<0,01, *** p<0,001
На наш взгляд, особенно важное значение имеет сохранение высокой активности КФК в стенке обструктивного мочевого пузыря в опытах с медикаментозной терапией (табл. 4), убыль которой в контрольной серии свидетельствует о выраженном повреждении мышечной оболочки мочевого пузыря, что может быть основой формирования дисфункции детрузора. При этом отмечали повышение активности этого фермента в крови крыс с ИВО в контрольной серии – 675±22 по сравнению с 187±14 Ед/л у интактных крыс (p< 0,001), тогда как в опытных сериях с терапией противоишемическими препаратами и доксазозином активность КФК достоверно не отличалась от нормы (201±11, 167±9 и 227±14 в сериях с терапией противоишемическими препаратами, доксазозином и их комбинацией соответственно). Это подтверждает вывод о лучшей сохранности детрузора при медикаментозной профилактике функциональных нарушений.
Таблица 4. Активность ферментов в стенке обструктивного мочевого пузыря при разных вариантах медикаментозной терапии (МЕ/мг белка)
| Ферменты | Норма | ИВО (контроль) |
ИВО+противоишемический комплекс | ИВО+ доксазозин |
ИВО+доксазозин + противоишемический комплекс |
|---|---|---|---|---|---|
| АСТ | 312±12 | 108±6 | 181±10** | 232±3*** | 206±13*** |
| АЛТ | 35,7±0,8 | 18,9±0,7 | 16,5±0,4 | 29,2±0,6* | 20,1±0,4 |
| ЩФ | 371±98 | 143±34 | 70±11 | 147±21 | 85±13 |
| ГГТП | 12,3±3,2 | 2,8±0,5 | 0 | 3,2±0,3 | 2,6±0,4 |
| ЛДГ | 1687±76 | 627±33 | 890±39** | 1552±78*** | 990±43** |
| ХЭ | 47,1±4,8 | 23,8±3,1 | 28,8±2,2 | 41,4±3,5* | 27,5±2,9 |
| КФК | 6334±309 | 601±45 | 4269±128*** | 5695±233*** | 4003±187*** |
Достоверность различий по сравнению с контролем: * -p<0,05, ** p<0,01, *** p<0,001
ОБСУЖДЕНИЕ
Проведенное исследование показало, что при одинаковой степени выраженности ИВО и гипертрофии мочевого пузыря терапия комплексом препаратов с противоишемическим действием оказывает протективное действие на функциональные и метаболические изменения, вызванные ИВО, по выраженности сопоставимое с действием α-адреноблокатора доксазозина. Положительные функциональные сдвиги проявлялись в уменьшении признаков гиперактивности детрузора, снижении базального внутрипузырного давления и степени перерастяжения мочевого пузыря. Об уменьшении метаболических расстройств свидетельствовала меньшая степень клеточного повреждения, в том числе гладкомышечных клеток детрузора, проявляющаяся в сохранении близкой к норме ферментативной активности в стенке мочевого пузыря. У животных контрольной группы активность КФК повышалась не только в моче за счет выхода фермента из поврежденных гладкомышечных клеток детрузора, но и в крови, свидетельствуя о высокой степени повреждения органа. На фоне противоишемической терапии активность КФК в крови и стенке мочевого пузыря приближалась к нормальным значениям, что свидетельствовало о выраженном цитопротективном эффекте этих препаратов на мышечную оболочку детрузора. Значительную роль в этом действии играло улучшение параметров микроциркуляции в обструктивном мочевом пузыре. По всей видимости, именно с этими факторами в значительной степени связано уменьшение дисфункции мочевого пузыря, выявленное в этой серии опытов.
Несколько разноречивыми оказались результаты опытов с терапией доксазозином. В этих опытах, как и ожидалось, выявлено значительное уменьшение тонуса мочевого пузыря на фоне выраженного увеличения его объема и ослабление признаков гиперактивности гипертрофированного детрузора. Однако, при этом параметры микроциркуляции в стенке мочевого пузыря достоверно ухудшались. Эти данные расходятся с результатами, опубликованными другими авторами, в которых показано, что терапия α-адреноблокаторами (тамсулозином, празозином) животных с экспериментально вызванной ИВО или хронической ишемией мочевого пузыря наряду с улучшением функционального состояния органа сопровождается улучшением его кровоснабжения [23-25]. По данным Е.Л. Вишневского и соавт. [1] у больных ДГПЖ, получавших доксазозин, также улучшалось кровоснабжение мочевого пузыря. Такое отличие может быть связано с особенностями действия различных α-адреноблокаторов, поскольку M. Yono и соавт. [25] не обнаружили влияния селективного αблокатора нафтопидила на состояние кровоснабжения ишемизированного мочевого пузыря у спонтанно гипертензивных крыс. Кроме того, в наших опытах крысы начинали получать доксазозин сразу после моделирования ИВО еще до формирования гипертрофии мочевого пузыря, тогда как в клинических условиях пациенты получают терапию уже на фоне длительно существующей обструкции, что также может влиять на действие препарата. По всей видимости, положительное влияние доксазозина в наших опытах на функциональное состояние обструктивного мочевого пузыря может быть связано с прямым действием препарата на его рецепторный аппарат или на вышележащие отделы нейрогенной регуляции.
Совместное использование доксазозина и комплекса противоишемических препаратов не усиливало защитного эффекта терапии крыс с ИВО по сравнению с действием препаратов по отдельности.
Данные литературы подтверждают полученные нами данные о целесообразности использования противоишемической терапии при расстройствах мочеиспускания, вызванных ИВО. О необходимости использования фармакологических препаратов, уменьшающих последствия хронической гипоксии мочевого пузыря (антиоксиданты, препараты улучшающие реологию крови, препараты улучшающие энергетический обмен) сообщали K.M. Azadzoi и S. Matsumoto [26, 27], хотя в литературе пока имеется незначительное количество публикаций, посвященных этому вопросу. В частности, в опытах in vitro с определением сократимости полосок, выкроенных из стенки мочевого пузыря, показано, что в условиях гипоксии сократимость полосок существенно снижается, а добавление инозина, являющегося предшественником АТФ, в перфузионную среду восстанавливает силу сокращений детрузора [9].
Положительное влияние оказывают также препараты с антиоксидантным действием. Предварительное введение антиоксиданта эдаравона, нейтрализующего активные радикалы кислорода, крысам с острой 30-минутной задержкой мочи предупреждало накопление маркеров окислительного повреждения клеточных структур (малонового диальдегида и 8-деоксигуанозина) и препятствовало снижению сократительной активности детрузора [13]. В опытах на кроликах с ранее моделированной инфравезикальной обструкцией, Y. Kawai и соавт. [14], показали, что растительный препарат эвипростат, обладающий антиоксидантным действием и широко используемый для лечения больных ДГПЖ в Японии и Германии, уменьшал на 70% экскрецию с мочой маркера оксидантного стресса 8-гидроксил-2-деоксигуанозина (8ОНdG), содержание которого в контрольной группе (без терапии препаратом) возрастала в 3,8 раза. Аналогичная динамика была получена и в клиническом исследовании: экскреция 8OHdG на фоне 4-недельного приема препарата снижалась в 2,5 раза, что сопровождалось уменьшением баллов IPSS с 16,6 до 13,7 и уменьшением QoL с 4,2 до 3,2 [12]. Это дало авторам основание считать, что терапевтический эффект эвипростата связан с его антиоксидантной активностью.
Блокаторы кальциевых каналов также обладают выраженным противоишемическим действием, уменьшая выраженность клеточного повреждения. В работе H.P. Liu и соавт. [15] показано, что у мышей-самцов с моделированной ДГПЖ путем хронического введения тестостерона и у самок с гиперактивностью детрузора, вызванной частичной инфравезикальной обструкцией, терапия блокатором Саканалов амлодипином уменьшала значения индекса мочевого пузыря, порога давления и давления мочеиспускания, а также увеличивала интервал между мочеиспусканиями. Комбинация амлодипина с теразозином в низкой дозе (в 2,5 раза ниже терапевтической) усиливала положительный эффект и приводила к значительному уменьшению частоты спонтанных сокращений мочевого пузыря вне фазы изгнания мочи.
У крыс со спонтанно развившейся гипертонией, которая сопровождалась стойким ухудшением кровотока в сосудах мочевого пузыря и дисфункцией мочеиспускания, терапия ингибитором рецептора ангиотензина II 1-го типа олмесартаном наряду с нормализацией интрамурального кровотока в стенке мочевого пузыря существенно улучшала параметры мочеиспускания [28].
Добавление теноксикама (ингибитора циклооксигеназы-2, блокирующего синтез простагландинов) к базовой терапии α-адреноблокатором доксазозином существенно увеличивало терапевтический эффект, приводя к более выраженному уменьшению симптомов IPSS, QoL и симптомов гиперактивности мочевого пузыря (OABSS) [29].
ЗАКЛЮЧЕНИЕ
Полученные результаты свидетельствуют о перспективности дальнейшего изучения эффективности противоишемической терапии с целью уменьшения расстройств мочеиспускания при ИВО, вызванной доброкачественной гиперплазией предстательной железы.
ЛИТЕРАТУРА
1. Вишневский А.Е. Роль нарушений энергетического метаболизма в патогенезе расстройств мочеиспускания у больных доброкачественной гиперплазией простаты и обоснование его медикаментозного лечения. // Дисс. докт. М. 2006. 240 с.
2. Azadzoi KM, Chen BG, Radisavljevic ZM, Siroku MB. Molecular reactions and ultrastructural damage in the chronically ischemic bladder. // J Urol. 2011. Vol. 186, N 5. P. 2115-2122.
3. Nomiya M, Andersson KE, Yamaguchi O. Chronic bladder ischemia and oxidative stress: New pharmacotherapeutic targets for lower urinary tract symptoms. // International Journal of Urology. 2015. Vol. 22, N 1. Р. 40-46.
4. Кирпатовский В.И., Мудрая И.С., Мкртчян К.Г., Ревенко С.В., Ефремов Г.Д., Надточий О.Н., Кабанова И.В. Ишемия тазовых органов как самостоятельный патогенетический фактор развития доброкачественной гиперплазии предстательной железы и дисфункции мочевого пузыря. // Бюлл. экспер. биол. и мед. 2014. Т. 158, № 12. С. 676-680.
5. Kapoor H, Gupta E, Sood A. Chronic pelvic ischemia: etiology, pathogenesis, clinical presentation and management. // Minerva Urol Nefrol. 2014. Vol. 66, N 2. P.127-137.
6. Andersson KE, Nomiya M, Sawada N, Yamaguchi O. Pharmacological treatment of chronic pelvic ischemia. // Ther Adv Urol. 2014. Vol. 6, N 3. P. 105-114.
7. Zarifpour M, Nomiya M, Sawada N, Andersson KE. Protective effect of tadalafil on the functional and structural changes of the rat ventral prostate caused by chronic pelvic ischemia. // The Prostate 2014. Vol. 75, N 3.
8. Yamaguchi O, Nomiya M, Andersson KE. Functional Consequences of Chronic Bladder Ischemia. // Neurourology and Urodynamics. 2014. Vol. 33, N 1.
9. Li S, Juan YS, Kogan BA, Mannikarottu A, Leggett R, Schuler C, Levin RM. Effects of inosine on response to in vitro hypoxia in absence of substrate on bladder dysfunction in adult rats. // Urology. 2009. Vol. 73, N 3. P. 661-664.
10. Kim JW, Jang HA, Bae JH, Lee JG. Effects of coenzyme Q10 on bladder dysfunction induced by chronic bladder ischemia in a rat model. // J Urol. 2013. Vol. 189, N 6. P. 2371-2376.
11. Shimizu S, Saito M, Oiwa H, Ohmasa F, Tsongapi P, Oikawa R, Dimitriadis F, Martin DT, Satoh I, Kinoshita Y, Tomita S. Olmesartan ameliorates urinary dysfunction in the spontaneously hypertensive rat via recovering bladder blood flow and decreasing oxidative stress. // Neurourol. Urodyn. 2013. doi: 10.1002/nau.22405.
12. Matsumoto S, Hanai T, Matsui T. Eviprostat suppresses urinary oxidative stress in a rabbit model of partial bladder outlet obstruction and in patients with benign prostatic hyperplasia. // Phytother Res. 2010. Vol. 24, N 2. P. 303-303.
13. Shimizu S, Saito M, Kinoshita Y, Kazuyama E, Tamamura M, Satoh I, Satoh K. Acute urinary retention and subsequent catheterization cause lipid peroxidation and oxidative DNA damage in the bladder: preventive effect of edaravone, a free-radical scavenger. // BJU Int. 2009. Vol. 104, N 5. P. 713-717.
14. Kawai Y, Oka M, Kyotani J, Oyama T, Matsumoto S, Kakizaki H. Effect of the phytotherapeutic agent eviprostat on the bladder in a rat model of bladder overdistension/emptying. // Neurourol Urodyn. 2013. Vol. 32, N 7. P. 1031-1037.
15. Liu HP, Chen GL, Liu P, Xu XP. Amlodipine alone or combined with terazosin improves lower urinary tract disorders in rat models of benign prostatic hyperplasia or detrusor instability: focus on detrusor overactivity. // BJU Int. 2009. Vol. 104, N 11. P. 1752-1757.
16. Saito M, Ohmasa F, Tsounapi P, Inoue S, Dimitriadis F, Kinoshita Y, Satoh K. Nicorandil ameliorates hypertension-related bladder dysfunction in the rat. // Neurourol Urodyn. 2012. Vol. 31, N 5. P. 695-701.
17. Кирпатовский В.И., Плотников Е.Ю., Мудрая И.С., Голованов С.А., Дрожжева В.В., Хромов Р.А., Черников Д.Ю., Скулачев В.П., Зоров Д.Б. Роль окислительного стресса и митохондрий в развитии дисфункции мочевого пузыря при острой задержке мочи. // Биохимия. 2013. Т. 78. № 5. С. 706-713.
18. Liuel P, Duquenne C, Martin D. Experimental bladder instability following bladder outlet obstruction in the female rat. // J. Urol. 1998. Vol. 160, N 6 (Pt 1). P. 2253-2257.
19. Abolyosr A, Elsagheer GA, Abdel-Kader MS, Hassan AM, Abou-Zeid AM. Evaluation of the effect of sildenafil and/or doxazosin on benign prostatic hyperplasia-related lower urinary tract symptoms and erectile dysfunction. // Urol Ann. 2013. Vol. 5, N 4. P.237-240.
20. Araki T, Monden K, Araki M. Comparison of 7 α(1)-adrenoceptor antagonists in patients with lower urinary tract symptoms associated with benign prostatic hyperplasia: a short-term crossover study. // Acta Med Okayama. 2013. Vol. 67, N 4. P. 245-251. 21. Мудрая И.С., Ибрагимов А.Р., Кирпатовский В.И., Ревенко С.В., Нестеров А.В., Гаврилов И.Ю. Оценка функционального состояния мочевого пузыря крыс методом Фурье-импедансной цистометрии. // Экспериментальная и клиническая урология. 2010. № 3. С. 21-26.
22. Кирпатовский В.И., Мудрая И.С., Федяков Р.П., Голованов С.А., Дрожжева В.В., Черников Д.Ю., Елисеев Д.Э., Надточий О.Н., Сыромятникова Е.В. Ферментурия, как маркер повреждения мочевого пузыря при острой задержке мочи. // Экспериментальная и клиническая урология. 2012. № 1. С. 20-23.
23. Goi Y, Tomiyama Y, Nomiya M, Sagawa K, Aikawa K, Yamaguchi O. Effects of silodosin, a selective α1A-adrenoceptor antagonist, on bladder blood flow and bladder function in a rat model of atherosclerosis induced chronic bladder ischemia without bladder outlet obstruction. // J Urol. 2013. Vol.190, N 3. P. 1116-1122.
24. Mine S, Yamamoto T, Mizuno H, Endo K, Matsukawa Y, Funahashi Y, Kato M, Hattori R, Gotoh M. Effect of tamsulosin on bladder microcirculation in rat model of bladder outlet obstruction using pencil lens charge-coupled device microscopy system. // Urology. 2013. Vol. 81, N 1. P. 155-159.
25. Yono M, Yamamoto Y, Imanishi A, Yoshida M, Ueda S, Latifpour J. Differential effects of prazosin and naftopidil on pelvic blood flow and nitric oxide synthase levels in sponta-neously hypertensive rats. // J Recept Signal Transduct Res. 2008. Vol. 28, N 4. P. 403-412.
26. Azadzoi KM, Radisavljevic ZM, Golabek T, Yalla SV, Siroky MB.Oxidative modification of mitochondrial integrity and nerve fiber density in the ischemic overactive blad-der. // J Urol. 2010. Vol. 83, N 1. P. 362-369.
27. Matsumoto S., Kakizaki H. Causative significance of bladder blood flow in lower urinary tract symptoms. // Int. J. Urol. 2012. Vol. 19, N 1. P. 20-25.
28. Shimizu S, Saito M, Oiwa H, Ohmasa F, Tsongapi P, Oikawa R, Dimitriadis F, Martin DT, Satoh I, Kinoshita Y, Tomita S. Olmesartan ameliorates urinary dysfunction in the spontaneously hypertensive rat via recovering bladder blood flow and decreasing oxidative stress. // Neurourol. Urodyn. 2013. doi: 10.1002/nau.22405.
29. Ozdemir T, Bozkurt O, Demir O. Combination therapy with doxazosin and tenoxicam for the management of lower urinary tract symptoms. // Urology. 2009. Vol. 74, N 2. P. 431-435.







