Гиперактивный мочевой пузырь (ГМП) — это симптомокомплекс, сопровождающийся ургентностью, никтурией (более 2 раз за ночь) с недержанием мочи или без такового и учащенным мочеиспусканием (более 8 раз в течение дня) при отсутствии доказанной инфекции или другой очевидной патологии нижних мочевых путей (НМП) [1-3]. За последний год в мире было зафиксировано более 546 млн случаев ГМП [4,5]. Распространенность ГМП среди женщин в США составляет 17%, а среди лиц старше 65 лет он выявляется более чем у 30% [6].
Несмотря на отсутствие однозначных данных о распространенности ГМП в России, принято считать, что она аналогична таковой в европейских странах [7]. За последние 10 лет количество пациентов с ГМП постоянно растет. В странах Азии и Южной Америки оно увеличилось на 22%, в Северной Америке — на 18%, а в странах Африки — на 31% [6]. К сожалению, многие пациенты не получают адекватного лечения и профессиональной помощи.
Симптомы ГМП негативно влияют на все аспекты повседневной жизни пациентов, в том числе на социальные (необходимость частых мочеиспусканий вне зависимости от местонахождения, что приводит к постоянному поиску туалетов и значительно ухудшает качество жизни пациентов), психологические (снижение самооценки, связанное с недержанием мочи), физические (ограничения физической активности из-за страха недержания мочи) и профессиональные (снижение производительности), что приводит значительному снижению качества жизни [8].
Первой линией терапии ГМП в настоящее время является фармакотерапия антагонистами мускариновых рецепторов, эффективность которых подтверждается многочисленными клиническими исследованиями [9-16]. Они блокируют М2- и М3-холинорецепторы, что приводит к снижению детрузорной гиперактивности в период накопления мочи и, соответственно, увеличению адаптационной способности мочевого пузыря. Одним из современных антагонистов мускариновых рецепторов для лечения синдрома ГМП является фезотеродин (Товиаз®, Pfizer) [17].
езотеродин ингибирует как М3-рецепторы, посредством которых осуществляется передача импульса на сокращение детрузора, так и М2-рецепторы, воздействие на которые препятствует расслаблению гладкой мускулатуры мочевого пузыря [12,13]. При этом фезотеродин воздействует на М3-холинорецепторы других органов (слюнных желез и т. д.) значительно слабее, что определяет селективность действия именно в отношении мочевого пузыря и минимизирует нежелательные эффекты от применения М-холиноблокаторов: сухость во рту, запоры, головную боль и нарушение зрения [12-16]. Цель исследования – изучение эффективности фезотеродина в терапии женщин с синдромом гиперактивного мочевого пузыря.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включено 60 женщин c симптомами ГМП в возрасте от 20 до 45 лет. Критерии исключения: стрессовое недержание мочи, конкременты мочевого пузыря и дистального отдела мочеточников, гематурия, онкологические заболевания органов мочевыделительной системы, оперативные пособия на органах малого таза, инфекции верхних и нижних мочевыводящих путей, а также отягощенный аллергический анамнез, неконтролируемая закрытоугольная глаукома и другие противопоказания к применению фезотеродина [17].
Всем женщинам было проведено обследование: сбор анамнеза заболевания и жизни, физикальное обследование, осмотр на гинекологическом кресле с проведением «кашлевой пробы». Каждой пациентки было предложено ежедневное заполнение дневников мочеиспускания, по данным которых оценивались частота мочеиспускания, императивные позывы, ноктурия, произведена оценка качества жизни по шкале Sf-36. Лабораторный мониторинг включал общий анализ крови, общий анализ мочи, а также бактериологическое исследование проб мочи с посевом урокультуры на твердые питательные среды для исключения инфекции мочевых путей.
Всем женщинам был назначен препарат фезотеродин (Товиаз®, Pfizer) в дозировке 4 мг 1 раз в сутки, который они принимали в течение 8 недель. Через 8 недель (60-е сутки) была произведена оценка эффективности и безопасности лечения. Она включала анализ дневников мочеиспускания, по данным которых определялось количество микций, ургентных позывов и ночных мочеиспусканий, а также оценивалось количества побочных эффектов (cухость во рту, запор, диспепсия, головная боль, острая задержка мочи, эпизоды инфекции нижних мочевых путей).
Также была произведена оценка качества жизни по шкале Sf-36. По результатам 8-недельного курса терапии больные были разделены на две группы. В группу 1 были включены женщины, у которых проведенная терапия была эффективна (снижение количества микций, отсутствие ноктурии и ургентных позывов). В данной группе была продолжена терапия фезотеродином в дозировке 4 мг 1 раз в сутки. В группу 2 были включены пациентки, у которых была отмечена низкая эффективность лечения (сохранялись поллакиурия, ноктурия и ургентные позывы). Им было предложено увеличение дозы препарата до 8 мг в сутки.
Через 8 недель (120-е сутки) была произведена сравнительная оценка эффективности и безопасности проведенной терапии в двух группах. Статистическую обработку результатов проводили с помощью программы MS Exсel 11.0 из стандартного пакета MS Office 2013, а также программного обеспечения IBM SPSS Statistics 21.0. При проверке статистических гипотез применяли методы параметрической (t-test Cтьюдента) статистики. При оценке достоверности выявленных различий между средними значениями выборок рассчитывали параметр р, вероятность справедливости нулевой гипотезы была принята равной 5 % (р < 0,05).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При обращении у всех женщин были выявлены симптомы, характерные проявлениям ГМП: поллакиурия, ургентные позывы к мочеиспусканию, ноктурия более 2-х раз за ночь. В ходе первичного физикального обследования, гинекологического осмотра и на основании данных лабораторных анализов у всех пациенток были исключены инфекционно-воспалительные заболевания нижних мочевых путей и стрессовое недержание мочи, которые могли бы вызвать сходную симптоматику. Полученные в ходе обследования на 1-е сутки данные представлены в таблице 1. По прошествии 8 недель (60-е сутки) терапии фезотерадином у женщин в целом была отмечена положительная динамика (табл. 2).
Таблица 1. Результаты обследования женщин в 1-е сутки терапии
Table 1. The results of examination of women on the 1st day of therapy
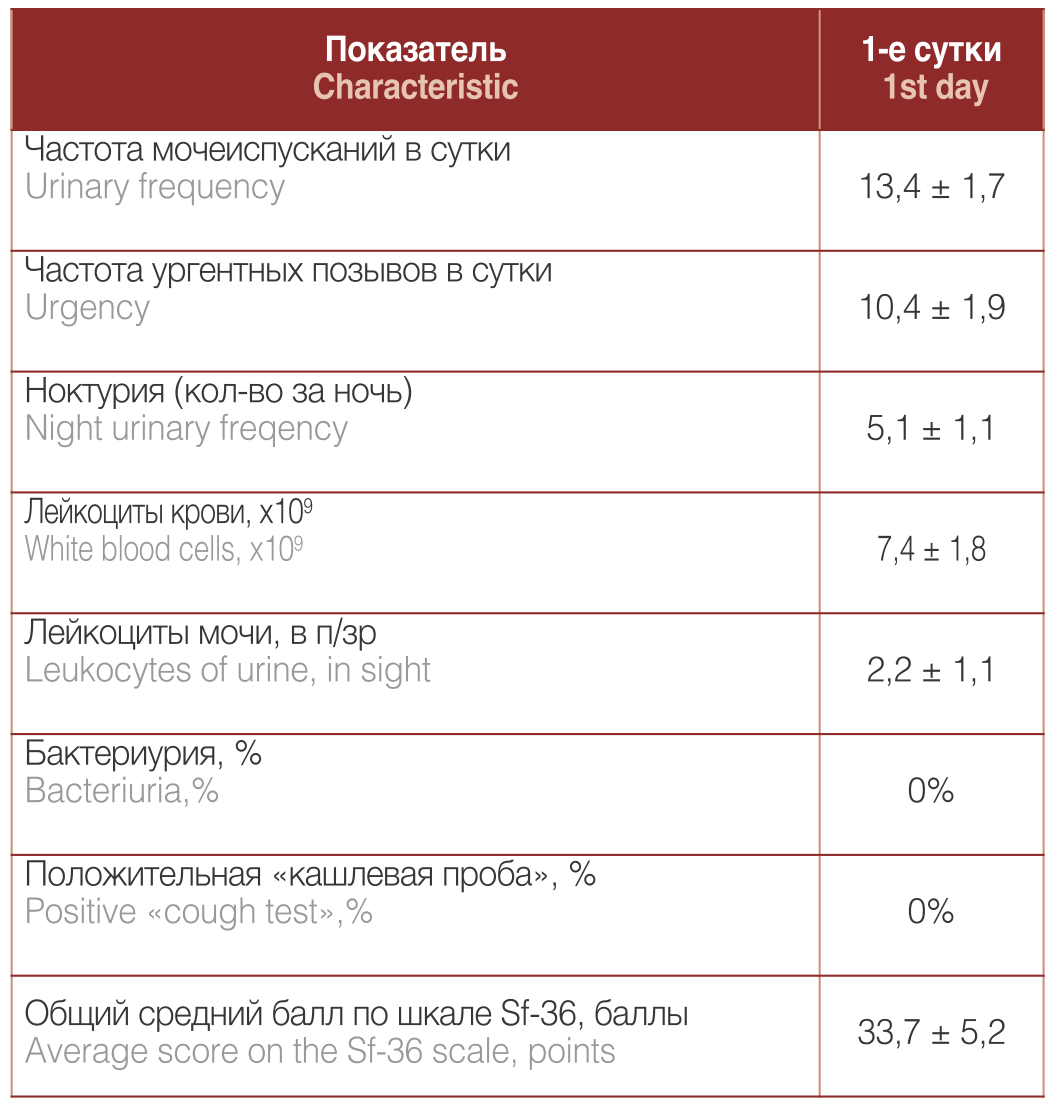
Таблица 2. Динамика клинических показателей и качества жизни пациенток через 8 недель терапии фезотерадином в дозировке 4 мг 1 раз в сутки
Table 2. The dynamics of clinical indicators and quality of life of patients after 8 weeks of therapy with fesoteradine in a dosage of 4 mg 1 time per day
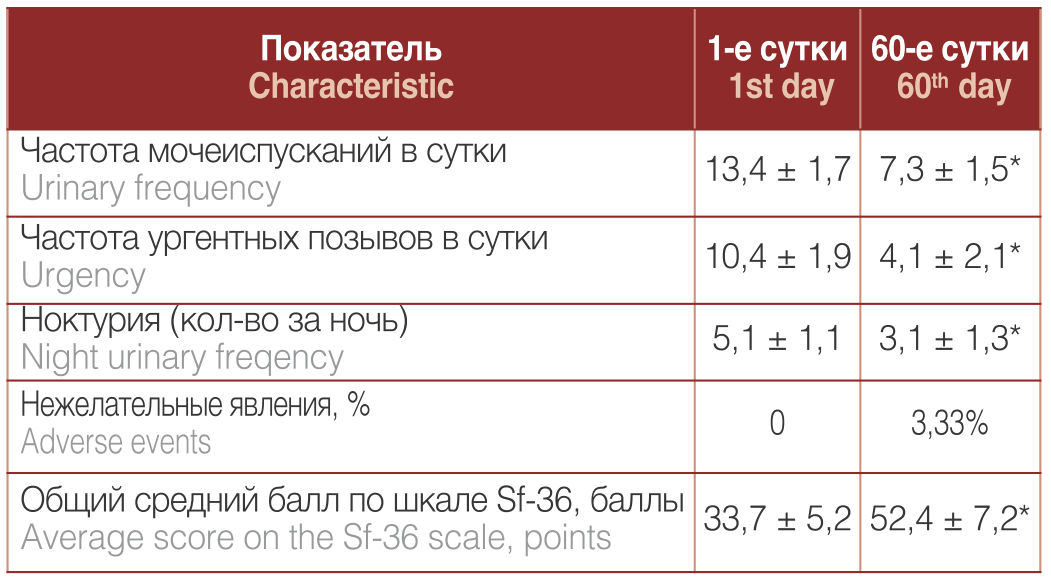
Примечание. Статистическая значимость различий: * — по сравнению с результатами предыдущего исследования при p < 0,05.
NOTE Statistical significance of differences:* – compared with the results of the previous study at p <0.05
Прием фезотеродина в течение 8 недель в дозировке 4 мг 1 раз в сутки позволил уменьшить общее количество микций, а также ургентных и ночных позывов на мочеиспускание по данным дневников мочеиспускания. Кроме того, было отмечено повышение качества жизни по шкале Sf-36. Нежелательные явления были зарегистрированы у 2 (3,3%) пациенток и проявились в виде сухости во рту. По результатам 8-недельного курса терапии был произведен анализ случаев низкой эффективности лечения (пациентки, у которых сохранялись поллакиурия, ноктурия и ургентные позывы), на основании которого женщины были разделены на две группы для проведения второго этапа исследования.
В группу 1 вошли 47 (78,3%) женщин, которым была продолжена терапия фезотеродином в дозировке 4 мг 1 раз в сутки в течение последующих 8 недель. В группу 2 вошли 13 (26,7%) женщин, которым было предложено увеличение дозы препарата до 8 мг в сутки. Длительность терапии также составила 8 недель. По окончании второго этапа был повторно проведен анализ эффективности и безопасности терапии в двух группах (табл. 3). В группе пациенток, перешедших на более высокую дозировку препарата, была отмечена достоверная положительная динамика (p < 0,05).
Таблица 3. Сравнительная динамика клинических показателей и качества жизни пациенток на 60-е и 120-е сутки терапии фезотеродином в двух группах.
Table 3. Comparative dynamics of clinical indicators and quality of life of patients on the 60th and 120th day of fesoterodine therapy in two groups.
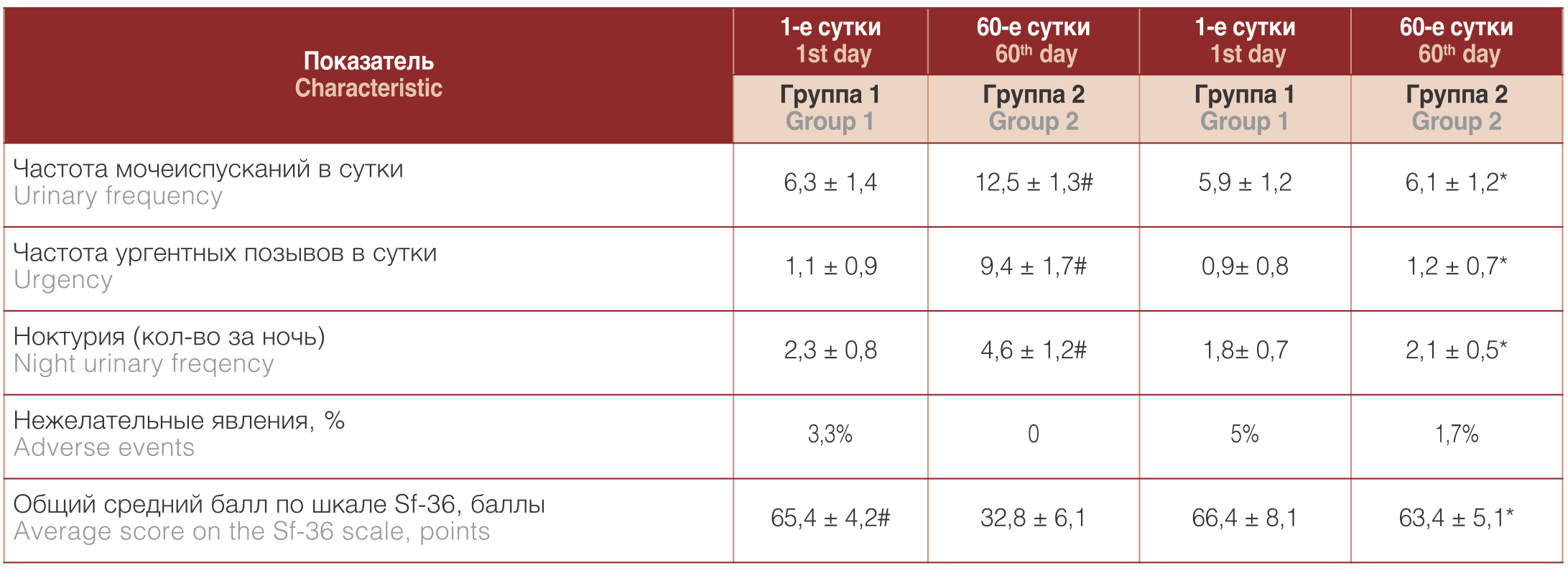
Примечание. Статистическая значимость различий: # — по сравнению с 1-й группой, *— по сравнению с результатами предыдущего исследования при p < 0,05.
NOTE Statistical significance of differences: # - compared with the 1st group, * - compared with the results of the previous study at p <0.05
В группе 1 были получены сопоставимые результаты, близкие к нормальным значениям. Достоверных различий в исследуемых показателях между группами выявлено не было (p > 0,05). Были зарегистрированы 2 случая нежелательных явлений (сухость во рту и запор), таким образом их количество возросло до 4 и составило 6,7% от общего числа больных. По данным опросников Sf-36 отмечено значимое повышение качества жизни в обеих группах (p < 0,05).
Фезотеродин — конкурентный специфический антагонист мускариновых рецепторов как М2-, так и М3-подтипа. На фоне его применения у пациентов с ГМП снижается число мочеиспусканий и эпизодов императивного недержания мочи, увеличивается средний объем мочи при мочеиспускании [12-16]. Фезотеродин быстро и интенсивно гидролизуется неспецифическими эстеразами плазмы крови до 5-гидроксиметил толтеродина (5-ГMT) — основного фармакологически активного метаболита, определяющего антимускариновую активность препарата [17]. Препарат не имеет ограничений к применению, связанных с заболеваниями центральной нервной системы, поскольку практически не проникает через гематоэнцефалический барьер (ГЭБ). 5-ГМТ обладает ограниченной способностью преодолевать ГЭБ и, являясь субстратом P-гликопротеина, быстро выводится из мозга, поэтому при применении фезотеродина отсутствует риск ухудшения когнитивной деятельности, включая память, что делает применение препарата предпочтительным у пожилых пациентов [16,17]. Фезотеродин является единственным антихолинергическим препаратом, одобренным для лечения ГМП у пожилых пациентов (оценка B — полезный по классификации FORTA) [1-3,18].
Фармакологические свойства фезотеродина, подтвержденные клиническими исследованиями [9-15], обеспечивают ряд преимуществ для пациентов: высокая эффективность лечения ГМП и относительно хорошая переносимость, что подтверждается результатами данного исследования. Необходимо также отметить, что синдром ГМП относится к изнурительным хроническим расстройствам и крайне негативно влияет на качество жизни больных [1–7]. Полученные в ходе исследования данные свидетельствуют, что купирование симптомов, характерных для ГМП, способствует повышению качества жизни пациенток данной категории.
В ряде клинических исследований получены несомненные доказательства дозозависимой эффективности фезотеродина [10-13]. По сравнению с 4 мг и плацебо фезотеродин 8 мг продемонстрировал статистически большую эффективность, что согласуется с полученными в ходе исследования результатами. Тем не менее, на наш взгляд, целесообразно применение препарата в начальной дозировке 4 мг в сутки, которая позволила достичь положительных результатов терапии у 78,3% больных к 8-ой неделе терапии при незначительном количестве побочных эффектов. При этом последующее повышение дозировки препарата до 8 мг в сутки позволило устранить СНМП у оставшихся пациенток. В тоже время переход на более высокую дозу препарата не привел к повышению количества побочных эффектов у женщин 2 группы.
ЗАКЛЮЧЕНИЕ
Таким образом, препарат Товиаз® (фезотеродин) имеет высокий профиль безопасности и эффективно купирует симптомы нижних мочевых путей у женщин с синдромом гиперактивного мочевого пузыря, а также позволяет повысить качество их жизни. Полученные данные обосновывают целесообразность применения двух различных доз фезотеродина в клинической практике: рекомендуемая начальная доза составляет 4 мг для всех пациентов с возможным увеличением дозы фезотеродина до 8 мг у пациентов, которым требуется большая доза для оптимального облегчения симптомов.
ЛИТЕРАТУРА
- Урология. Российские клинические рекомендации [под ред. Ю.Г. Аляева, П.В. Глыбочко, Д.Ю. Пушкаря]. М.: ГЭОТАР-Медиа, 2018. 480 с. [Urology. Russian clinical guidelines [ed. Yu. G. Alyaev, P. V. Glybochko, D. Yu. Pushkar]. M.: GEOTAR-Media, 2018. 480 p. (In Russian)]
- Gratzke C, Bachmann A, Descazeaud A, Drake MJ, Madersbacher S, Mamoulakis C, et al. EAU Guidelines on the Assessment of Non-neurogenic Male Lower Urinary Tract Symptoms including Benign Prostatic Obstruction. Eur Urol 2015;67(6):1099-1109 doi: 10.1016/j.eururo.2014.12.038.
- Недержание мочи у женщин: Клинические рекомендации. Утверждены Российским обществом урологов, 2016. URL: https://medi.ru/klinicheskie-rekomendatsii/nederzhanie-mochi-u-zhenschin_14098/. [Urinary incontinence in women: Clinical recommendations. Approved by the Russian society of urology, 2016. URL: https://medi.EN/klinicheskierekomendatsii/nederzhanie-mochi-u-zhenschin_14098/.
- Irwin DE, Kopp ZS, Agatep B, Milsom I, Abrams P.Worldwide prevalence estimates of lower urinary tract symptoms, overactive bladder, urinary incontinence and bladder outlet obstruction. BJU Int 2011;108(7):1132–1138. doi: 10.1111/j.1464-410X.2010.09993.x.
- Heesakkers J., Espuña Pons M., Toozs Hobson P., Chartier-Kastler E.. Dealing with complex overactive bladder syndrome patient profiles with focus on fesoterodine: in or out of the EAU guidelines? Res Rep Urol 2017;9:209–218. doi: 10.2147/RRU.S146746.
- Gormley E.A., Lightner D.J., Faraday M., Vasavada S.P.. Diagnosis and treatment of overactive bladder (non-neurogenic) in adults: AUA/SUFU guideline amendment. J Urol 2015;193(5):1572–1580. doi: 10.1016/j.juro.2015.01.087.
- Касян Г.Р., Ходырева Л.А., Дударева А.А., Тупикина Н.В., Пушкарь Д.Ю. Синдром гиперактивности мочевого пузыря в клинической практике врача-уролога: методические рекомендации. М.; 2016. 40 с. [Kasyan G.R., Khodyreva L.A., Dudareva A.A., Tupikina N.V., Pushkar D.Yu. The Syndrome of overactive bladder in clinical practice urologist: methodical recommendations. M.; 2016. 40 p. ( In Russian)].
- Irwin DE, Abrams P, Milsom I, Kopp Z, Reilly K. Understanding the elements of overactive bladder: questions raised by the EPIC study. BJU Int 2008;101(11):1381–1387. doi: 10.1111/j.1464-410X.2008.07573.x.
- Кузьменко А.В., Кузьменко В.В., Гяургиев Т.А. Эффективность применения фезотеродина у больных после трансуретральной резекции простаты. Урология 2019;(1):52-55. [Kuzmenko A.V., Kuzmenko V.V., Gyaurgiev T.A. Efficacy of fesoterodine in patients after transurethral resection of the prostate. Urologiia = Urology 2019;(1):52-55. (In Russian)].
- Meek PD, Evang SD, Tadrous M, Roux-Lirange D, Triller DM, Gumustop B. Overactive bladder drugs and constipation: a meta-analysis of randomized, placebo-controlled trials. Dig Dis Sci 2011;56(1):7–18. doi: 10.1007/ s10620-010-1313-3
- Herbison P, McKenzie JE. Which anticholinergic is best for people with overactive bladders?Anetwork meta-analysis. Neurourol Urodyn 2019;38(2):525–534. doi: 10.1002/nau.23893.
- Nitti VW, Dmochowski R, Sand PK, Forst HT, Haag-Molkenteller C, Massow U, et al. Efficacy, safety and tolerability of Fesoterodine for overactive bladder syndrome. J Urol 2007;178(6):2488-94. doi: 10.1016/j.juro.2007.08.033
- Chapple C1, Van Kerrebroeck P, Tubaro A, Haag-Molkenteller C, Forst HT, Massow U, et al. Clinical efficacy, safety, and tolerability of once-daily fesoterodine in subjects with overactive bladder. Eur Urol 2007;52:1204–1212. doi: 10.1016/j.eururo.2007.07.009
- Margulis AV, Hallas J, Pottegård A, Kristiansen NS, Atsma WJ, Franks B, et al.Comparison of cardiovascular events among treatmentsfor overactive bladder: a Danish nationwide cohort study. Eur J Clin Pharmacol 2018;74(2):193–199. doi: 10.1007/s00228-017-2359-3.
- Margulis AV, Linder M, Arana A, Pottegård A, Berglind IA, Bui CL, et al. Patterns of use of antimuscarinic drugs to treat overactive bladder in Denmark, Sweden, and the United Kingdom. PLoS One 2018;13(9):e0204456. doi: 10.1371/journal.pone.0204456
- Kay GG, Maruff P, Scholfield D, Malhotra B, Whelan L, Darekar A, et al. Evaluation of cognitive function in healthy older subjects treated with fesoterodine. Postgrad Med 2012;124(3):7–15. doi: 10.3810/pgm.2012.05.2543
- Инструкция по применению лекарственного препарата Товиаз® ЛП002016. URL: http://grls.rosminzdrav.ru/Grls_View_ v2.aspx?routingGuid=b8090193–4145–48de-9447–50c97e012a55&t=. [Instruction for use of Toviaz® LP-002016. URL: http://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=b8090193–4145–48de9447–50c97e012a55&t= (access date: 05.02.2019) (in Russian)].







