Мочекаменная болезнь (МКБ) – широко распространенное заболевание, отражающее нарушение обмена веществ, финальным проявление которого является образование конкрементов в органах мочевой системы. Огромная антропогенная нагрузка, которую несет современное человечество в результате прогрессивно ухудшающейся экологической обстановки, изменившегося характера и качества питания, увеличения неблагоприятных социальных факторов, обуславливает устойчивую тенденцию к росту заболеваемости во всех странах мира, в том числе в России [1-8].
Патогенез МКБ весьма сложен и включает ряд универсальных механизмов, в равной степени реализующихся при развитии таких актуальных заболеваний, как сахарный диабет, метаболический синдром, ожирение и артериальная гипертензия. Картину социальной значимости уролитиаза дополняют статистические данные, согласно которым наиболее подвержены заболеванию люди трудоспособного возраста в диапазоне от 20 до 45 лет [1,9-12].
Начало XXI века ознаменовалось радикальными изменениями в лечении МКБ на фоне повсеместного внедрения в урологическую практику высокоинформативных методов диагностики и малотравматичных, щадящих методик удаления конкрементов. Однако хирургические успехи не снизили актуальности и социальной значимости этого заболевания [7]. В настоящее время пациенты с МКБ составляют до 40% всего контингента урологических стационаров [13].
Современный комплексный подход к лечению МКБ характеризуется многообразием хирургических техник и вариантов медикаментозного воздействия, которые, как правило, используются совместно в различных сочетаниях.
Трансуретральная уретеро- и нефролитотрипсия, перкутанная литотрипсия и дистанционная литотрипсия (ДЛТ) составляют основу хирургии МКБ. Однако ни один из вышеназванных методов не позволяет во всех случаях добиваться одномоментного полного устранения конкремента и его фрагментов из мочевой системы [13,14]. В тех случаях, когда так называемый эффект «полного освобождения от камней» («stone free rate») все же достигается, следует понимать, что это ни в коей мере не решает проблемы МКБ как системного заболевания. Хорошо известно, что в ближайшее десятилетие после оперативного вмешательства (спонтанного отхождения конкремента) риск повторного камнеобразования достигает 30-40%, сохраняясь на уровне 5-15% в течение всей последующей жизни [15].
Таким образом, с учетом проблемы резидуальных камней и риска рецидивирования, конечный результат лечения пациента в немалой степени определяется сопутствующей медикаментозной терапией и вторичной профилактикой.
В этом комплексе медикаментозного сопровождения больных с МКБ важное место занимает литокинетическая (камнеизгоняющая) терапия. Это один из наиболее старых способов лечения мочекаменной болезни, представляющий в настоящее время современную методику с развитой системой показаний и противопоказаний.
Литокинетическая терапия может иметь как самостоятельное значение при выявлении исходно небольших конкрементов почки и мочеточника, так и включаться в комплекс мероприятий по борьбе с резидуальными конкрементами после различных хирургических пособий.
Литокинетическая терапия, включающая спазмолитики, анальгетики, мочегонные средства и физиотерапевтические воздействия, в урологии традиционно и с немалым успехом дополняется использованием растительных препаратов. Именно это направление фитотерапии востребовано в урологии в наибольшей степени [2,16-20].
Исторически в первую очередь был подмечен положительный эффект эфирных масел, применение которых способствовало самостоятельному отхождению конкрементов. Эфирные масла представляют собой легко испаряющиеся жидкости с характерным запахом, состоящие из органических веществ растительного происхождения. Количество компонентов, входящих в состав эфирных масел, может достигать одной тысячи, что делает весьма затруднительным детальное описание их качественного и количественного состава.
И хотя препараты на основе непосредственно эфирных масел используются по настоящее время, важным шагом вперед стали идентификация и выделение из сложной смеси органически соединений определенных химических субстанций, с которыми непосредственно связаны востребованные эффекты.
Этими веществами оказались терпены (от латинского Oleum Terebinthinae – скипидар). Именно терпены демонстрируют яркий литокинетический потенциал, складывающийся как совокупность спазмолитического и диуретического эффектов и стимулирующего воздействия на почечную гемодинамику. Кроме этого, некоторые терпены обладают противовоспалительным и умеренным антибактериальным действием, что дополнительно повышает ценность этих веществ для урологической практики [21].
Основу терпенов составляет непредельный углеводород диенового ряда, имеющий брутто-формулу С5Н8 (2-метилбута-1,3-диен) и известный как изопрен. Соединяясь строго определенным образом, молекулы изопрена формируют огромный спектр соединений, свойства которых прямо зависят от количества объединенных молекул, то есть от степени полимеризации. В зависимости от числа изопреновых фрагментов выделяют монотерпены, сесквитерпены, дитерпены (2, 3, 4 изопреновых фрагмента, соответственно) и т.д. Высокополимеризованные соединения изопрена носят название политерпенов и известны как гуттаперча и природный каучук [22,23].
Терпены эфирных масел имеют небольшую степень полимеризации и, соответственно, небольшую массу, что обуславливает их характерные физические свойства – высокую летучесть и специфический аромат. С увеличением степени полимеризации растет масса молекулы и параллельно снижается летучесть, изменяется агрегатное состояние и характер запаха химического вещества.
В окружающей природе помимо собственно терпенов в еще большем количестве представлены их разнообразные кислородсодержащие производные, известные как терпеноиды. Группа терпеноидов выделена в первую очередь по фитохимическому признаку, так как с точки зрения органической химии эти соединения принадлежат к классам кетонов, альдегидов, одно- и многоатомных спиртов, простых и сложных эфиров, карбоновых кислот. В настоящее время известно более 10000 терпеноидов, крайне разнообразных по своим физическим, химическим, фармакологическим свойствам [21-23].
Успехи органической химии и фармацевтической промышленности позволили создавать лекарственные препараты, содержащие только выделенные и очищенные терпены и терпеноиды, а не весь огромный набор соединений растительных веществ, точный состав и соотношения которых до конца не известны.
Растительные препараты, имеющие строго определенный и постоянный состав очевидно предпочтительнее, так как сочетают предсказуемую фармакодинамику и метаболизм, свойственные синтетическим лекарственным средствам, с широтой терапевтического эффекта и высоким уровнем безопасности, характерными для фитопрепаратов [21].
В настоящее время заслуживает внимания новый фитокомплекс на основе терпенов – Ренотинекс® (производитель ООО «Полярис», дистрибьютор АО «Мединторг»), отличающийся от аналогов в том числе значительной экономической привлекательностью.
Ренотинекс® выпускается в виде капсул с кишечнорастворимым покрытием по 300 мг (табл. 1).
Таблица 1. Качественный и количественный состав капсулы Ренотинекс®
Table 1. Qualitative and quantitative composition of Renotinex® capsules
| Пинен [смесь изомеров α+β], C10H16 Pinene [mixture of α + β isomers], C10H16 |
15,45 мг (mg) |
| Камфен, C10H16 Camphen, C10H16 |
7,50 мг (mg) |
| Цинеол, C10H16O Cineol, C10H18O |
1,51 мг (mg) |
| Фенхол, C10H16O Fenchol, C10H16O |
2,01 мг (mg) |
| Борнеол, C10H18O Borneol, C10H18O |
4,97 мг (mg) |
| Анетол, C10H12O Anethol, C10H12O |
2,01 мг (mg) |
| Витамин Е Vitamin E |
1,67 мг (mg) |
Пинен и камфен являются монотерпенами с циклической структурой, а цинеол, фенхол, борнеол и анетол входят в группу терпеноидов, с химической точки зрения относясь к классам кетонов, спиртов и ароматических эфиров. В состав Ренотинекс® дополнительно включен масляный раствор витамина Е, основной механизм действия которого ассоциируется со стабилизацией белково-липидных связей клеточных мембран, что обуславливает протективный эффект в отношении свободных радикалов.
Целью данного исследования было изучение эффективности и безопасности клинического применения комплекса терпенов Ренотинекс® при проведении литокинетической терапии у больных с МКБ.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование были включены 142 пациента, находившихся на лечении в урологической клинике ФГБОУ ВО «Астраханский государственный медицинский университет» на базе ГБУЗ АО «Александро-Мариинская областная клиническая больница» в течение 2019 г.
У 38 пациентов исходно диагностировались конкременты небольших размеров (до 5 мм), и существовал комплекс условий, позволяющих проводить литокинетическую терапию. У 104 пациентов резидуальные камни почек и мочеточников размером не более 5 мм были выявлены после выполнения различных вариантов литотрипсии (рис. 1).
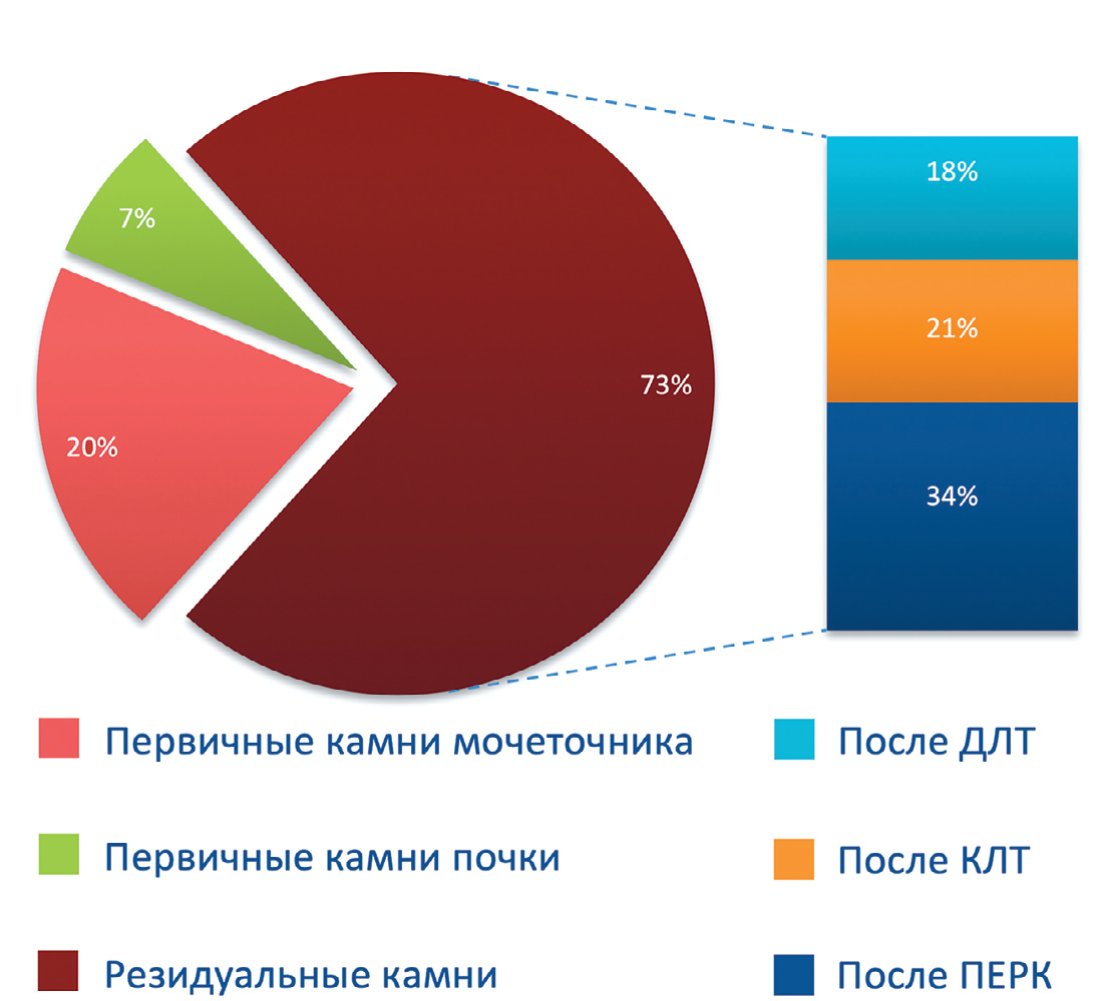
Рис.1. Варианты мочекаменной болезни у пациентов, включенных в исследование
Fig. 1. Options for urolithiasis in patients included in the study
Группа пациентов состояла из 65 мужчин (средний возраст 41,7 ± 15,6 года) и 77 женщин (средний возраст 40,8 ± 16,4 года).
Диагностика и выработка тактики лечения основывались на комплексном обследовании, выполнявшемся пациентам при поступлении в стационар. Помимо выяснения жалоб больных, сбора анамнеза и оценки объективного статуса, выполнялись ультразвуковое исследование мочевыделительной системы, компьютерная томография (КТ), обзорная и экскреторная урография (при отсутствии противопоказаний). Лабораторный блок исследований включал общий анализ крови (ОАК) и мочи (ОАМ), основные биохимические показатели крови (мочевина, креатинин, электролиты), а также бактериологическое исследование мочи с определением чувствительности микроорганизмов к антибактериальным препаратам. Также лабораторно верифицировался химический состав удаленных или самостоятельно отошедших конкрементов и их фрагментов.
С целью объективизации выраженности болевых ощущений использовалась 10- балльная числовая рейтинговая шкала для боли (Numeric rating Scale for pain, NRS).
Пациенты, у которых выявлялись первичные или резидуальные конкременты, размеры и локализация которых делали проведение литокинетической терапии заведомо бесперспективным, в исследование не включались. Также в качестве критериев исключения рассматривались: анурия, гнойные поражения почек, беременность и лактация.
Пациенты, включенные в исследование, были разделены на две равные группы, сопоставимые по основным клинико-диагностическим критериям. Пациенты I (основной) группы получали стандартную литокинетическую терапию и фитокомплекс Ренотинекс® по 2 капсулы (600 мг) 3 раза в день с момента установления диагноза и до окончания стационарного лечений. Пациентам II (контрольной) группы Ренотинекс® не назначался.
В динамике оценивались результаты комплексного лечения пациентов обеих групп по следующим критериям:
- субъективная оценка общего состояния пациента и выраженности болевых ощущений при изгнании камней, частота развития почечных колик;
- сроки и полнота самостоятельного отхождения конкрементов;
- результаты ультразвукового, рентгенологического и КТ контроля состояния мочевых путей;
- характер изменений в анализах крови и мочи (лейкоцитоз, степень лейкоцитурии, pH мочи, содержание минеральных веществ) и степень бактериурии при микробиологическом исследовании мочи;
- число сеансов ДЛТ и количества импульсов в каждом из сеансов дробления.
Статистическая обработка полученных данных проводилась по методу Стьюдента, различия в показателях считали достоверными при p<0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Частота почечных колик и степень выраженности болевого синдрома в процессе литокинетической терапии оценивались во время ежедневных обходов при помощи рейтинговой шкалы для боли (от 0 до 10 баллов).
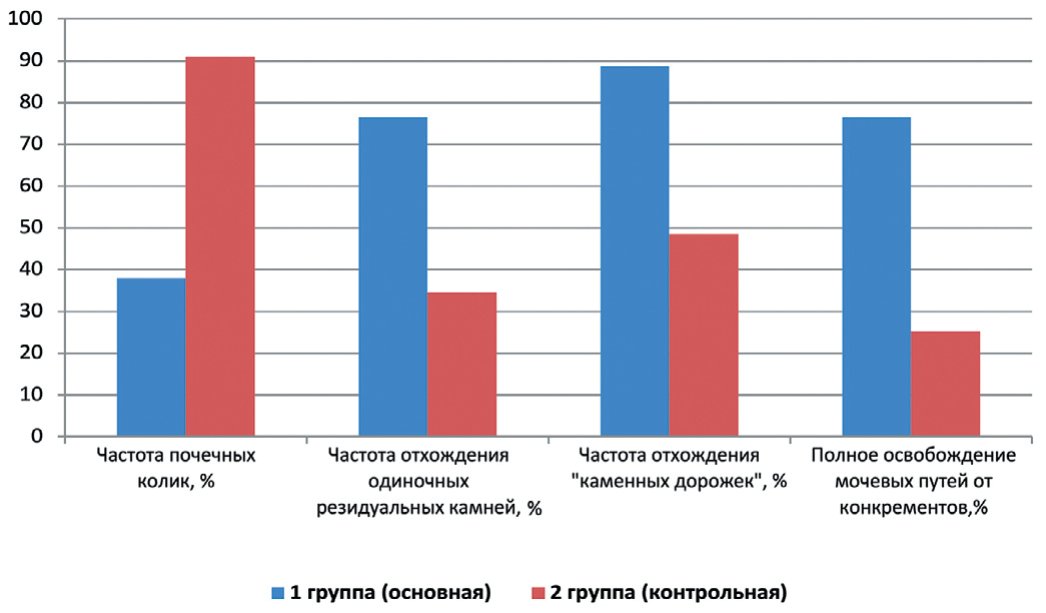
У пациентов I группы почечные колики регистрировались в 38% наблюдений. При этом развившийся болевой приступ достаточно легко купировался дополнительным назначением спазмолитиков и анальгетиков и редко возникал повторно. Среди пациентов контрольной группы почечные колики возникали в 91% случаев и, как правило, носили рецидивирующий характер и хуже купировались. Интенсивность болевых ощущений пациенты первой группы оценивали в среднем в 4,88 ± 2,1 баллов, в контрольной группе эта величина достигала 7,80 ± 2,2 баллов.
Таким образом, применение Ренотинекс® объективно снижало фармакологическую нагрузку на пациентов за счет сокращения использования спазмолитических и анальгетических препаратов. Пациенты, получавшие фитокомплекс, отмечали лучшее субъективное самочувствие в процессе лечения и хорошую его переносимость.
У пациентов, получавших Ренотинекс®, самостоятельное отхождение конкрементов отмечено в 76,4% случаев, в контрольной группе подобный эффект констатирован лишь в 34,6% наблюдений. Особо необходимо отметить результат применения фитокомплекса у пациентов с камнями и «каменными дорожками» нижней трети мочеточника. Частота самостоятельного отхождения конкрементов в этом случае достигала 88,7%, в то время как стандартная литокинетическая терапия оказывалась эффективной лишь 48,6% случаев.
Применение Ренотинекс® оказывало положительное влияние не только на частоту, но и на сроки самостоятельного отхождения конкрементов – они были на 51,2% меньше в основной группе.
Наиболее оптимальный результат – полное освобождение мочевых путей от конкрементов – достигнут в 76,4% случаев в первой группе и в 25,3% – в контрольной (рис. 2).
Рис. 2. Результаты применения фитокомплекса Ренотинекс®. Спазмолитический и литокинетический эффекты
Fig. 2. The results of the use of the Renotinex® phytocomplex. Antispasmodic and lithokinetic effects
Эффективность дистанционной литотрипсии (ДЛТ) в обеих группах оценивали по количеству пособий ДЛТ и числу импульсов в каждом из сеансов дробления.
Для дезинтеграции камня у пациентов, которым назначался Ренотинекс®, требовалось суммарно 1970 ± 140 импульсов, на фоне стандартной терапии эта величина составляла 2580 ± 214, причем разница имела статистически достоверный характер.
Риск развития острого пиелонефрита на фоне литокинетической терапии обусловлен сохраняющейся частичной обструкцией мочевых путей, а в случае предшествовавших оперативных пособий, направленных на фрагментацию конкремента, также и выходом микроорганизмов из внутренних слоев разрушенного конкремента в просвет мочевыводящих путей. Мы оценивали влияние фитокомплекса на степень лейкоцитурии и бактериурии. При исходном обследовании лейкоцитурия в ОАМ была выявлена у 81,8% пациентов, бактериурия в диагностически значимом титре (105 КОЕ/мл для кишечной палочки) – у 49,3 % пациентов – все они получали антибактериальную терапию в соответствии с результатами бактериологического исследования мочи. При лабораторном обследовании в динамике не было выявлено существенного влияния комплекса Ренотинекс® на результаты посева мочи и на уровень азотистых шлаков в биохимическом анализе крови. Вместе с тем отмечены достоверные (р < 0,05) изменения в общем анализе мочи, выражавшиеся в уменьшении степени лейкоцитурии и возросшей экскреции минеральных солей. Другой эффект, ассоциированный с приемом фитокомплекса, заключался в увеличении диуреза у пациентов I группы на 38,7% по сравнению с пациентами контрольной группы и параллельном снижение удельного веса мочи при неизменных значениях pH. У пациентов контрольной группы эти показатели не претерпевали значимых изменений в процессе лечения (табл. 2).
Каких-либо нежелательных эффектов, напрямую связанных с применением фитокомплекса Ренотинекс®, отмечено не было.
Таким образом, проведенное исследование позволяет придти к следующему заключению:
- включение Ренотинекс® в комплексную литокинетическую терапию положительно сказывается на субъективном состояние пациентов за счет уменьшения частоты и выраженности болевого синдрома;
- использование Ренотинекс® позволяет в большинстве случаев добиться быстрого и полного освобождения мочевых путей от мелких конкрементов;
- использование Ренотинекс® способствует увеличению диуреза, снижению удельного веса мочи и стимуляции выведения минеральных солей. При этом важным моментом терапевтического эффекта является отсутствие влияния фитокомплекса на электролитный баланс крови и pH мочи;
- Ренотинекс® также проявляет противовоспалительный эффект, что в сочетании с антибактериальной терапией благоприятно сказывается на течении осложняющих МКБ воспалительных процессов;
- Ренотинекс® хорошо переносится пациентами и не вызывает побочных эффектов.
ВЫВОДЫ
Проведенное исследование демонстрирует высокую эффективность применения отечественного продукта Ренотинекс® для целей литокинетической терапии в случае первичных или резидуальных камней почек и мочеточников независимо от их химического состава. Применение данного фитокомплекса особенно оправдано при формировании «каменных дорожек» после ДЛТ, так как более быстрое и полное отхождение фрагментов конкрементов в этом случае сопровождается лишь умеренно выраженными болевыми ощущениями
Ренотинекс® обладает также диуретическими, спазмолитическими, противовоспалительными и антибактериальными свойствами и в составе комплексной терапии эффективно способствует устранению инфекционно-воспалительных осложнений мочекаменной болезни.
Комплекс терпенов Ренотинекс® отличается хорошей переносимостью и не имеет побочных эффектов.
Таблица 2. Динамика некоторых лабораторных показателей в процессе лечения
Table 2. The dynamics of some laboratory parameters in the treatment process
| Исходные показатели по выборке пациентов на момент включения в исследование Baseline patient sampling at time of enrollment |
Результаты контрольного обследования через 2 недели от начала терапии The results of the control examination after 2 weeks from the start of therapy |
||
|---|---|---|---|
| I группа (основная) I group (main) |
II группа (контрольная) II group (control) |
||
| ОАМ | |||
| Лейкоцитурия, % Leukocyturia,% | 81,8 | 27,9 | 37,2 |
| рН мочи Urine pH | 5,8±1,1 | 5,6±1,8 | 5,5±1,9 |
| Удельный вес мочи Urine specific gravity | 1016,4±2,9 | 1011,13±2,1 | 1015,8±3,1 |
| Биохимические показатели мочи Biochemical indicators of urine |
|||
| Экскреция фосфатов, ммоль/л Phosphate Excretion, mmol / L | 11,18 ± 4,65 | 15,19 ± 3,77 | 11,09 ± 4,74 |
| Экскреция уратов, ммоль/л Urinary excretion mmol / L | 1,39 ± 0,51 | 2,66 ± 0,79 | 1,45±0,6 |
| Экскреция оксалатов, ммоль/л Oxalate Excretion, mmol / L | 1,88 ± 1,1 | 2,4±1,2 | 1,97+1,0 |
| Бактериологическое исследование мочи Bacteriological urinalysis |
|||
| Бактериурия в диагностически значимом титре (105 КОЕ/мл),% Bacteriuria in a diagnostically significant titer (105 CFU / ml),% |
49,3 | 10,5 | 10,8 |
| Биохимические показатели крови Biochemical blood counts |
|||
| Мочевина крови (ммоль\л) Blood Urea (mmol / L) | 7,1±2,4 | 6,8±2,3 | 6,9±2,1 |
| Креатинин крови (мкмоль\л) Blood creatinine (μmol / L) | 88±7,6 | 83±8,0 | 82±7,8 |
ЛИТЕРАТУРА
- Черепанова Е.В., Дзеранов Н.К. Метафилактика мочекаменной болезни в амбулаторных условиях. Экспериментальная и клиническая урология 2013;3:33-39. [Cherepanova E.V., Dzeranov N.K. Metaphylaxis of urolithiasis on an outpatient basis. Eksperimental'naya i klinicheskaya urologiya=Experimental and clinical urology 2013;3:33-39. (In Russian)]
- Гайбуллаев А.А., Кариев С.С., Турсунов Б.Ш. Применение комбинированных растительных мочегонных препаратов при уролитиазе. Экспериментальная и клиническая урология 2013;4:76-81. [Gaybullaev A.A., Kariev S.S., Tursunov B.Sh. The use of combined herbal diuretics for urolithiasis. Eksperimental'naya i klinicheskaya urologiya 2013;4:76-81. (In Russian)]
- Константинова О.В., Яненко Э.К., Шадеркина В.А. Метафилактика мочекислых камней почек. Экспериментальная и клиническая урология 2016;3:116-118. [Konstantinova O.V., Yanenko E.K., Shaderkina V.A. Metaphylaxis of uric acid kidney stones. Eksperimental'naya i klinicheskaya urologiya=Experimental and clinical urology 2016;3:116-118. (In Russian.)]
- Beltrami P, Ruggera L, Guttilla A, Iannetti A, Zattoni F, Gigli F, et al. Endourological treatment of renal matrix stones. Urol Int, 2014;93(4):394-8. 4.
- Sánchez-Martin FM, Millán Rodriguez F, Esquena Fernández S, Segarra Tomás J, Rousaud Barón F, Martínez-Rodríguez R, et al. Incidence and prevalence of published studies about urolithiasis in Spain. A review. Actas Urol Esp 2007;31(5):511-20. DOI: 10.1016/s0210-4806(07)73675-6
- Yasui T, Ando R, Okada A, Tozawa K, Iguchi M, Kohri K. Epidemiology of urolithiasis for improving clinical practic. Hinyokika Kiyo 2012;58(12):697-701.
- Яненко Э.К., Меринов Д.С., Константинова О.В. Епишов В.А., Калиниченко Д.Н. Современные тенденции в эпидемиологии, диагностике и лечении мочекаменной болезни. Экспериментальная и клиническая урология 2012;3:19-24. [Yanenko E.K., Merinov D.S., Konstantinova O.V. Epishov V.A., Kalinichenko D.N. Current trends in epidemiology, diagnosis and treatment of urolithiasis. Eksperimental'naya i klinicheskaya urologiya=Experimental and clinical urology 2012;3:19-24. (In Russian)]
- Каприн А.Д., Аполихин О.И., Сивков А.В., Москалева Н.Г., Солнцева Т.В., Комарова В.А. Анализ уронефрологической заболеваемости и смертности в Российской Федерации за 2003-2013 гг. Экспериментальная и клиническая урология 2015;2:4-12. [Kaprin A.D., Apolihin O.I., Sivkov A.V., Moskaleva N.G., Solntseva T.V., Komarova V.A. Analysis of the neurophrological morbidity and mortality in the Russian Federation for 2003-2013. Eksperimental'naya i klinicheskaya urologiya=Experimental and clinical urology 2015;2:4-12. (In Russian)]
- Cho ST, Jung SI, Myung SC, Kim TH. Correlation of metabolic syndrome with urinary stone composition. Int J Urol 2013;2(20):208-213. doi: 10.1111/j.1442-2042.2012.03131.x.
- Константинова О.В., Шадеркина В.А. Опыт медикаментозного лечения пациентов с мочекислой формой мочекаменной болезни. Экспериментальная и клиническая урология 2015;1:78-80. [Konstantinova O.V., Shaderkina V.A. The experience of drug treatment of patients with urate form of urolithiasis. Eksperimental'naya i klinicheskaya urologiya=Experimental and clinical urology 2015;1:78-80. (In Russian)]
- Сивков А.В., Черепанова Е.В., Шадеркина В.А. Применение фитопрепаратов на основе терпенов при мочекаменной болезни. Экспериментальная и клиническая урология 2011;1:69-72. [Sivkov A.V., Cherepanova Ye.V., Shaderkina V.A. The use of phytopreparations based on terpenes in urolithiasis. Eksperimental'naya i klinicheskaya urologiya=Experimental and clinical urology 2011;1:69-72. (In Russian)]
- Авдошин В.П., Андрюхин М.И., Исрафилов М.Н. Комплексное лечение и метафилактика уратного и смешанного уролитиаза: метод. пособие для врачей. – М.: Спецкнига, 2013. [Avdoshin VP, Andrukhin MI, Israfilov MN. Complex treatment and metaphylaxis of urate and mixed urolithiasis: method. manual for doctors. Moscow: Spetskniga; 2013. (In Russian]
- Шестаев А.Ю., Протощак В.В., Паронников М.В., Киселев А.О. Комбинированный (цитратный и растительный) препарат уриклар в дистанционной литотрипсии и метафилактике мочекаменной болезни. Урологические ведомости 2018;8(1):19-25. DOI: 10.17816/uroved8119-25. [Shestayev A.YU., Protoshchak V.V., Paronnikov M.V., Kiselev A.O. The combined (citrate and herbal) drug uriclar in remote lithotripsy and metaphylaxis of urolithiasis. Urologicheskiye vedomosti=Urological statements 2018;8(1):19-25. DOI: 10.17816/uroved8119-25. (In Russian)]/
- Мартов А.Г., Гордиенко А.Ю., Москаленко С.А., Пенюкова И.В. Дистанционная и контактная уретеролитотрипсия в лечении крупных камней верхней трети мочеточника. Экспериментальная и клиническая урология 2013;2:82-85. [Martov A.G., Gordiyenko A.YU., Moskalenko S.A., Penyukova I.V. Remote and contact ureterolithotripsy in the treatment of large stones of the upper third of the ureter. Eksperimental'naya i klinicheskaya urologiya=Experimental and clinical urology 2013;2:82-85. (In Russian)]
- Вощула В.И. Мочекаменная болезнь: этиотропное и патогенетическое лечение, профилактика. Минск: ВЭВЭР, 2006. [Voshchula V.I. Urolithiasis: etiotropic and pathogenetic treatment, prevention. Minsk: VEVER, 2006. (In Russian)]
- Блюмберг Б.И., Основин Р.Н., Фомкин Р.Н. Фитотерапия уратного нефролитиаза. Клиническая нефрология 2013;1:71-72. [Blyumberg B.I., Osnovin R.N., Fomkin R.N. Herbal medicine of urate nephrolithiasis. Klinicheskaya nefrologiya=Clinical nephrology 2013;1:71-72. (In Russian)]
- Дзеранов Н.К., Константинова О.В., Москаленко С.А., Бешлиев Д.А., Бутин П.С., Дрозжева В.В., Конькова Т.А. Роль фитотерапии в до- и послеоперационном периоде у пациентов с мочекаменной болезнью. Урология 2005;2:18-20. [Dzeranov N.K., Konstantinova O.V., Moskalenko S.A., Beshliyev D.A., Butin P.S., Drozzheva V.V., Kon'kova T.A. The role of herbal medicine in the pre- and postoperative period in patients with urolithiasis. Urologiya=Urology 2005;2:18-20. (In Russian)]
- Сивков А.В., Дзеранов Н.К., Черепанова Е.В., Константинова О.В., Голованов С.А., Шадеркина В.А. Результаты применения препарата Роватинекс у больных, страдающих уролитиазом. Экспериментальная и клиническая урология 2011;4:38-45. [Sivkov A.V., Dzeranov N.K., Cherepanova Ye.V., Konstantinova O.V., Golovanov S.A., Shaderkina V.A. The results of the use of the drug Rovatinex in patients suffering from urolithiasis. Eksperimental'naya i klinicheskaya urologiya=Experimental and clinical urology 2011;4:38-45. (In Russian)]
- Türk C, Knoll T, Petrik A, Sarica K, Skolarikos A, Straub M, et al. Guidelines on Urolithiasis. European Association of Urology 2015. Available from: http://uroweb.org/wpcontent/uploads/22-Urolithiasis_LR_full.pdf
- Анафин Т.Г., Досхожаев Б.К., Шалекенов С.Б. Опыт применения препарата уриклар в комплексном лечении хронического пиелонефрита. Вестник казахского национального медицинского университета 2016;3:61-67. [Anafin T.G., Doskhozhayev B.K., Shalekenov S.B. The experience of using the drug uriklar in the complex treatment of chronic pyelonephritis. Vestnik kazakhskogo natsional'nogo meditsinskogo universiteta=Bulletin of the Kazakh national medical university 2016;3:61-67. (In Russian)]
- Шадеркина В.А., Шадеркин И.А. Терпены и их применение в клинической практике. Экспериментальная и клиническая урология 2019;1:77-80. [Shaderkina V.A., Shaderkin I.A. Terpenes and their use in clinical practice. Eksperimental'naya i klinicheskaya urologiya=Experimental and clinical urology 2019;1:77-80. (In Russian)]
- Племенков В.В. Химия изопреноидов. Химия растительного сырья 2006;3:55-72. [Plemenkov V.V. Chemistry of plant raw materials. Khimiya rastitel'nogo syr'ya=Chemistry of plant raw materials 2006;3:55-72. (In Russian)]
- Пономарев Д.А., Федоров Э.И. Основы химии терпенов: учебное пособие. Сыктывкар: СЛИ, 2014. 56 с.. [Ponomarov D.A., Fedorov E.I. The basics of terpene chemistry: a tutorial. Syktyvkar: SLI, 2014. — 56. (In Russian)].