ВВЕДЕНИЕ
Проблема мочекаменной болезни (МКБ) сохраняет свою актуальность во всем мире, затрагивая преимущественно пациентов трудоспособного возраста. В различных странах показатели распространенности МКБ варьируют от 1 до 20 % [1]. Проведенный анализ заболеваемости на территории Российской Федерации с 2005 по 2016 гг. продемонстрировал, что частота МКБ среди популяции взрослого населения составляет примерно 0,7 % с тенденцией к увеличению [2]. Заболеваемость уролитиазом выше среди мужчин, чем среди женщин, что подтверждено на основании регистра NHANES (National Health and Nutrition Examination Survey), соотношение составляет 1,75:1 [3]. Для лечения пациентов МКБ применяют как консервативную терапию, так и различные методы оперативного лечения. Контактная уретеролитотрипсия ригидным или гибким уретероскопом выполняется при камнях любого отдела мочеточника, чаще при локализации в средней и нижней трети. Несмотря на возможность применения лазерной литотрипсии, независимо от состава камня не все фрагменты конкрементов извлекаются из мочеточника интраоперационно. Пациенты с резидуальными фрагментами конкремента в мочеточнике требуют продолжения литокинетической терапии для профилактики возникновения почечной колики, острого пиелонефрита, дренирования верхних мочевых путей, и чтобы избежать повторной госпитализации.
Перспективным направлением в улучшении результатов контактной уретеролитотрипсии может быть дополнение растительных препаратов к основной послеоперационной терапии. Одним из растительных препаратов является растительный комплекс Ренотинекс®. Имеющиеся данные о результатах применения Ренотинекс® указывают на то, что он способствует лучшему отхождению конкрементов по верхним мочевым путям, а его активно действующие вещества обладают нефропротективным эффектом [4].
Цель исследования: oценить клиническую эффективность применения Ренотинекс® после оперативного вмешательства в объеме контактной уретеролитотрипсии у пациентов с мочекаменной болезнью.
МАТЕРИАЛЫ И МЕТОДЫ
В университетской клинике урологии РНИМУ им. Н.И. Пирогова в период с ноября 2019 г. по март 2020 г. проведено проспективное, одноцентровое, рандомизированное исследование. Критериями включения в исследование были мужчины и женщины в возрасте 18–75 лет с МКБ и наличием конкрементов средней и нижней трети мочеточника, подтвержденных данными ультразвукового исследования и рентгенологическими методами. Критерием исключения явилось наличие клинических и лабораторных признаков острого воспалительного процесса в органах мочеполовой системы. Всем пациентам была выполнена контактная уретеролитотрипсия. Пациенты были разделены на 2 группы: группа Ренотинекс® (основная) (n = 30) – пациенты, получавшие препарат растительного происхождения Ренотинекс® по 600 мг (2 капс.) х 3 раза в день с первого дня после операции (в течение 1 месяца) в дополнение к стандартной терапии; группа контрольная (n = 30) – пациенты, получавшие только стандартную послеоперационную терапию. В группе Ренотинекс® было 16 (60%) пациентов мужского и 14 (40%) женского пола, в контрольной – 14 (40%) и 16 (60%) пациентов, соответственно. Средний возраст пациентов в обеих группах достоверно не различался и составил 51,9 и 55,3 лет, соответственно (p>0,05). Следует обратить внимание на длительный анамнез мочекаменной болезни у всех пациентов с медианой в 4,5 года. Сопутствующие заболевания были диагностированы у 17 (57%) больных в основной группе: сахарный диабет – 3 (10%) и гипертоническая болезнь – 14 (46,7%), в контрольной группе – в 19 (63,3%) случаях: сахарный диабет – 4 (13,3%) и гипертоническая болезнь – 14 (46,7%). Все пациенты были компенсированы относительно сопутствующих заболеваний до проведения оперативного вмешательства. Длительный стаж курения чаще встречался среди пациентов основной группы и составил 56,7% (17 пациентов), в то время как в контрольной группе – 40% (12 пациентов). Среди пациентов основной группы до операции у 24 (80%) больных функционировал внутренний мочеточниковый стент, у 2 (6,7 %) – нефростомический дренаж и в 4 (13,3 %) случаях дренажи отсутствовали. В группе контроля до операции у 18 (60%) был установлен внутренний мочеточниковый стент, у 2 (6,7 %) – нефростомический дренаж и у 10 (30%) пациентов отсутствовал какой-либо дренаж. С учетом стратификации риска, в соответствии с результатами посева мочи, была назначена антибактериальная терапия у 5 (16,7%), в каждой группе. Всем пациентам была выполнена мультиспиральная компьютерная томография. Конкременты имели следующую локализацию для основной и контрольной групп: в в/3 – у 8 (26,7%) и 5 (16,7%) пациентов соответственно; в ср/3 – в 9 (30%) и в 5 (16,7%) случаях, в н/3 – 12 (40%) и в 17 (56,7%) случаях, и в интрамуральном отделе мочеточника – в 1 (3,3%) и в 3 (10%) случаях соответственно. Минимальный размер конкремента составил 4 мм для обеих групп, максимальный размер в основной группе – 21 мм и в группе контроля – 17 мм. После выполнения контактной уретеролитотрипсии 16 (53,3%) пациентам из основной группы и 10 (33,3%) пациентам из контрольной группы потребовалась установка внутреннего мочеточникового стента. Последний удалялся через месяц после операции. Наружный мочеточниковый катетер был установлен на сутки после операции в 10 (30%) и 16 (53,3%) случаях, соответственно.
В обеих группах (по 4 (13,3%) пациента в каждой) оперативное вмешательство закончилось без какоголибо дренажа.
В послеоперационном периоде антибактериальная терапия была дополнительно назначена в связи с признаками системной воспалительной реакции у 1 (3,3%) пациента основной группы и у 3 (10%) пациентов контрольной. Сравнительная характеристика групп представлена в таблице 1.
Таблица 1. Основные показатели обеих групп до начала оперативного лечения
Table 1. Main characteristics of both groups before treatment
| Показатель Characteristic |
Основная группа Ренотинекс® (визит 0) n (%) Primary group Renotinex® (visit 0) |
Контрольная группа (визит 0) n (%) |
|---|---|---|
| Количество мужчин Number of men Количество женщин Number of women |
16 (53,3) 14 (46,7) |
15 (50) 15 (50) |
| Возраст (лет) Age (years) | 51,9 | 55,3 |
| МКБ в анамнезе (медиана) / (лет) Urolithiasis anamnesis (median) / (years) | 4 | 5 |
Наличие дренажа перед операцией: Preoperative drainage
|
4 (13,3) 24 (80) 2 (6,7) |
10(33,3) 18 (60) 2 (6,7) |
Наличие сопутствующей патологии: Co-morbidity
|
3 (10) 14 (46,7) |
3 (13,3) 14 (46,7) |
| Курение в анамнезе > 10 лет Smoking more over 10 years | 17 (56,7) | 12 (40) |
| ИМП в анамнезе Urinary tract infections | 27(90) | 17(56,7) |
| Антибактериальная терапия в предоперационном периоде Antimicrobial therapy in the preoperative period |
5 (16,7) | 5 (16,7) |
| Лейкоцитурия в ОАМ до операции Leukocyturia in simple urine test | 11 (36,7) | 5 (16,7) |
| Рост патогенной микрофлоры по данным посева мочи Pathogenic flora in urine culture |
4 (13,3) | 5 (16,7) |
| Повышение показателей азотистого баланса (мочевины/креатинина) до операции Increasing of the nitrogen balance (urea nitrogen / creatinine) before treatment |
8 (26,7) | 7 (23,3) |
КУЛТ (контактная уретеролитотрипсия) Ureterolithotripsy
|
8 (26,7) 9 (30) 12 (40) 1 (3,3) |
5 (16,7) 5 (16,7) 17 (56,7) 3 (10) |
| Размер конкремента при КУЛТ (минимальный/максимальный) The size of calculus during ureterolithotripsy (minimal / maximal) |
4 мм/21 мм | 4 мм/17 мм |
Установка дренажей в конце операции Postoperative drainage
|
16 (53,3) 10 (33,3) 4 (13,3) |
10 (33,3) 16 (53,3) 4 (13,3) |
| Дополнительно антибактериальная терапия в послеоперационном периоде по поводу СВР Antimicrobial therapy in the postoperative period |
1 (3,3) | 3 (10) |
Статистическая обработка данных выполнена на индивидуальном компьютере с помощью электронных таблиц Microsoft Excel и пакета программы «Prism 8 for Windows» (GraphPad Software, Inc). Все полученные анамнестические, клинические, лабораторные и инструментальные данные вносились в базу данных Microsoft Excel, разработанную автором, и были обработаны методом вариационной статистики. Для каждого количественного параметра были определены среднее значение (М), среднеквадратическое отклонение (δ), ошибка среднего (m), медиана (Ме), 95 % доверительный интервал, для качественных данных — частоты (%). Для сравнения числовых данных (после проверки количественных данных на нормальное распределение) использовали t-критерий Стъюдента. Для сравнения непараметрических данных применяли попарное сравнение осуществляли с помощью критерия Манна-Уитни (для 2-х групп) для несвязанных совокупностей. Статистически значимыми считались отличия при p<0,05 (95%-й уровень значимости).
РЕЗУЛЬТАТЫ
За обеих групп осуществлялся непрерывный контроль спустя 1 (Визит 2) и 3 месяца (Визит 3) после начала терапии. Пациентам проводили сбор жалоб, общий осмотр, оценивали результаты клинического обследования (общеклинический анализ крови, общеклинический анализ мочи, биохимический анализ крови, посев мочи на флору с определением чувствительности к антибиотикам) и данные ультразвукового исследования мочевых путей, а также интерпретировали данные нативной компьютерной томографии. Для основной группы пациентов также проводили оценку побочных явлений применения Ренотинекс®.
Повторная госпитализация в стационар в связи с атакой пиелонефрита в послеоперационном периоде в основной группе не потребовалась, в контрольной группе – по 1 (3,3%) пациенту до Визита 1 и Визита 2.
Спустя месяц болевой синдром в поясничной области беспокоил в основной группе и контрольной 5 (16,7%) и 8 (26,7%) пациентов соответственно (p<0,05). Спустя 3 месяца после операции только в контрольной группе у 3 (10%) пациентов сохранялся болевой синдром, тогда как в основной группе к 3 месяцам – болевой синдром полностью исчез.
В первый месяц наблюдения субфебрильное повышение температуры тела (37,1–37,9°С) отмечено у 1 (3,3%) пациента основной группы и у 7 (23,3%) пациентов контрольной группы (p<0,05). В обеих группах температура нормализовалась до окончания срока наблюдения.
Частота повышения показателей азотистого обмена была сопоставима в основной группе и в группе контроля спустя 1 месяц наблюдения после операции (5/16,7% и 6/20% соответственно, p>0,05). Но к 3 месяцам активного наблюдения была отмечена достоверная разница: показатели креатинина и мочевины были в норме у всех пациентов основной группы, но оставались выше нормы у 4 (13,3%) пациентов контрольной группы (p<0,05).
Рост патогенной микрофлоры, согласно посеву мочи, был зафиксирован по 1 (3,3%) случаю в каждой группе спустя 1 и 3 месяца (p>0,05).
Показатели лейкоцитурии и эритроцитурии спустя 1 месяц превалировали в основной группе и наблюдались в 6 (20%) случаях, когда в контрольной – у 2 (6,7%) пациентов (p<0,05). Такая разница обусловлена тем, что у пациентов в основной группе чаще после операции устанавливался внутренний мочеточниковый стент из-за более частой локализации конкремента в верхней и средней трети мочеточника. Удаление мочеточникового стента проводилось спустя 1 месяц после операции, что почти всегда совпадало с визитом 1. Одинаковая частота бактериурии в группах на первом визите исключает воспаление мочевых путей как причину эритроцит- и лейкоцитурии. К 3 месяцам одинаково в каждой группе по 1 (3,3%) пациенту сохранялась лейкоцитурия.
При использовании инструментальных методов визуализации критериями наличия мочекаменной болезни являлись конкременты > 5 мм по данным ультразвукового исследования и > 3 мм по данным мультиспиральной компьютерной томографии (МСКТ). У пациентов, получающих дополнительно Ренотинекс®, спустя 1 месяц активного наблюдения конкременты визуализированы в 3 (10%) случаях , и у 1 (3,3%) пациента – к 3 месяцам наблюдения. В контрольной группе данный показатель составил – 6 (20%) и 3 (10%), больных соответственно (p<0,05). Надо отметить, что частота выполнения МСКТ превалировала в основной группе.
За весь период наблюдения только у 1 (3,3%) пациента наблюдалась диарея, которая самостоятельно прекратилась после окончания курса терапии. В таблице 2 приведено сравнение основных показателей обеих групп спустя 1 и 3 месяца активного наблюдения.
Таблица 2. Сравнение основных показателей обеих групп спустя 1 и 3 месяца активного наблюдения
Table 2. Compression of both groups after 1 and 3 months active monitoring
| Показатель Characteristic |
Основная группа Ренотинекс® Primary group Renotinex® |
Контрольная группа Control group |
||
|---|---|---|---|---|
|
визит 1 |
визит 2 (3 месяца после операции) n (%) |
визит 1 (1 месяц после операции) n (%) |
визит 2 (3 месяца после операции) n (%) |
|
Необходимость повторной госпитализации Demand of Re-hospitalization
|
– – |
1 (3,3) – |
1 (3,3) 1 (3,3) |
– 1 (3,3) |
| Болевой синдром в поясничной области (на стороне выполнения оперативного вмешательства) Pain syndrome in the lumbar region (on the side of the surgical intervention) |
5 (16,7) | – | 8 (26,7) | 3(10) |
| Гипертермия (37.1-37.9С) Hyperthermy | 1 (3,3) | – | 7 (23,3) | – |
| Лейкоцитурия / Эритроцитурия в ОАМ в послеоперационном периоде (Эритроциты > 3-х в поле зрения; Лейкоцитурия > 5 в поле зрения) Leukocyturia / Erythrocyturia in simple urine test |
6 (20) | 1 (3,3) | 2 (6,7) | 2 (6,7) |
| Повышение показателей азотистого баланса (мочевины/креатинина) после операции Increasing of the nitrogen balance (urea nitrogen / creatinine) after treatment |
5 (16,7) | – | 6 (20) | 4 (13,3) |
| Рост патогенной микрофлоры по данным посева мочи Pathogenic flora in urine culture |
1 (3,3) | 1 (3,3) | 1 (3,3) | 1 (3,3) |
| Количество пациентов с подтвержденной МКБ по данным УЗИ / МСКТ. (Критерии оценки конкремента: УЗИ > 6 мм, МСКТ > 4 мм.) Number of patients with confirmed urolithiasis disease according to ultrasound / computer tomography |
3(10) | 1 (3,3) | 6 (20) | 3(10) |
ОБСУЖДЕНИЕ
В настоящее время под англоязычным термином «stone-free» следует понимать отсутствие конкрементов после проведенного лечения, которое не должно включать группу пациентов с бессимптомными, клинически незначимыми резидуальными конкрементами размером менее 4 мм [5, 6]. Риск рецидива МКБ в ближайшие 5-10 лет после первого эпизода составляет 30-50% [7]. Несмотря на вышеуказанные данные и развитую систему медицинского страхования, в западных странах примерно 3% пациентов проводятся метафилактические мероприятия [8]. Препараты растительного происхождения занимают значимое место в лечении и профилактике МКБ. В 2013 г. M.E. Chua и соавт. продемонстрировали литокинетический эффект лекарственных средств на основе терпенов [9]. Согласно данным НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина, вероятность самостоятельного отхождения конкремента, на фоне проводимой комплексной терапии, включающей трепены, составляет 73% [10]. Терапевтическое применение растительного комплекса Ренотинекс® способствует улучшению функции почек, уменьшению болевого синдрома, выведению мелких конкрементов из почек и снижению риска повторного камнеобразования.
Ренотинекс® зарегистрирован 25.04.2018 г. в качестве биологически активной добавки к пище (регистрационный номер – KZ.16.01.95.003.E.000294.04.18), представляет собой комбинацию из масляного раствора витамина Е и встречающихся в природе терпенов и эфирных масел. Спазмолитический и противовоспалительный эффект действия препарата обусловлен свойствами пинена (α+β). Камфен способствует улучшению тканевого кровотока и имеет антибактериальное и спазмолитическое действие. Борнеол обладает антибактериальным, обезболивающим, спазмолитическим и сосудорасширяющим действиями. Основными свойствами атенола являются мочегонный и антибактериальный эффекты, а фенхона и цинеола – антисептический и спазмолитический эффекты. Входящий в состав комплекса Ренотинекс® помимо шести монотерпенов витамин Е (α-токоферола ацетат) способствует быстрейшей регенерации почечной ткани после литотрипсии. Витамин Е обеспечивает стабильность белково-липидных связей в мембранах клеток почек и эритроцитов, способствуя защите организма от вредоносного воздействия свободных радикалов.
Анальгетический эффект терпенов соизмерим со среднетерапевтическими дозами индометацина [11]. В.Л. Медведев и соавт. оценили уменьшение выраженности боли по визуальной аналоговой шкале (ВАШ), оказалось, что в группе пациентов, принимавших Ренотинекс®, отмечено значительное снижение данного показателя [12]. С уменьшением выраженности боли пациенты быстрее возвращаются к привычному ритму жизни. Обсуждая литокинетический эффект, следует отметить успешное использование отечественного продукта Ренотинекс® в исследовании В.А. Круглова и соавт., где применение фитокомплекса особенно оправдано после проведения дистанционной литотрипсии (ДЛТ) [13]. Процесс самостоятельного отхождения фрагментов конкремента на фоне терапии после сеанса ДЛТ обусловлен достоверным увеличением диуреза, что подтверждается публикациями В.А. Шадеркиной и соавт., В.М. Попковым и соавт. и соответствует полученным нами данными в ходе проведения исследования [14, 15].
Клиническое преимущество применения растительного комплекса Ренотинекс® в нашем исследовании заключалось в статистически достоверном уменьшении выраженности болевого синдрома в первые три месяца после операции, нормализации температурной кривой и отсутствии субфебрилитета в первый месяц после контактной уретеролитотрипсии (рис. 1). Также в нашей работе продемонстрировано, что на фоне терапии с использованием комплекса Ренотинекс® происходит достоверно более быстрая нормализация показателей азотистого обмена крови (креатинин и мочевина) в раннем послеоперационном периоде, ниже частота повторных госпитализаций по поводу атаки острого пиелонефрита и быстрая нормализация общего анализа мочи после удаления внутреннего мочеточникового стента, что указывает на противовоспалительный эффект растительного комплекса.
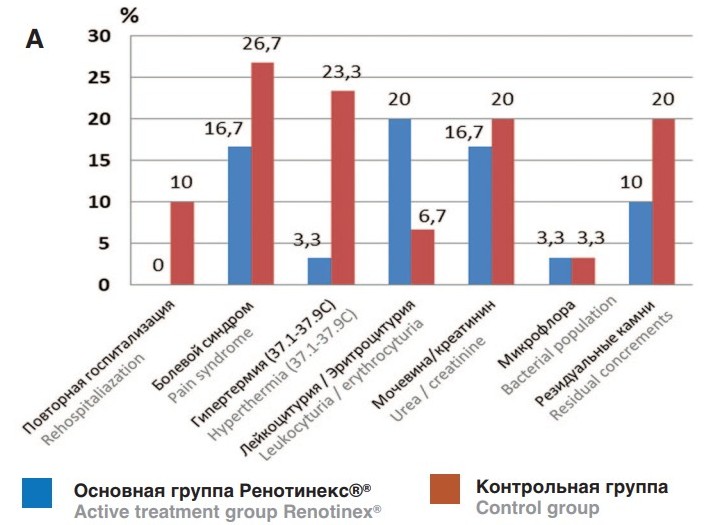
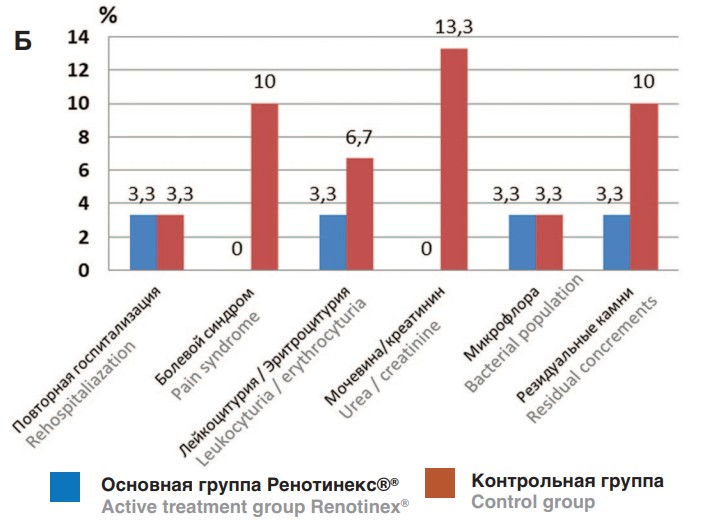
Рис. 1. А. Визит 2 (через 1 мес. после операции)
Б. Визит 3 (через 3 мес. после операции)
Fig. 1. А. Visit 2 (1 month after surgery)
Б. Visit 3 (3 month after surgery)
В группе применения Ренотинекс® за весь период наблюдения нежелательные реакции и побочные явления отсутствовали. Также в основной группе частота определения резидуальных фрагментов камня была достоверно ниже как спустя 1 месяц, так и спустя 3 месяца после операции, что указывает на увеличение процента отхождения конкрементов после выполнения контактной уретеролитотрипсии на фоне приема растительного комплекса.
ВЫВОДЫ
Проведенное исследование показало обоснованность применения Ренотинекс® в комплексном лечении пациентов с МКБ в послеоперационном периоде после контактной уретеролитотрипсии. Ренотинекс® обладает литокинетическим эффектом за счет спазмолитического, диуретического и противовоспалительного действия натуральных терпенов. Применение данного растительного комплекса способствует лучшему отхождению конкрементов, а активно действующие вещества – профилактике инфекционно-воспалительных осложнений МКБ.
ЛИТЕРАТУРА
- Trinchieri A. Epidemiology, In: Stone Disease, edited by Segura J, Conort P, Khoury S, Paris, France, ICUD, Distributed by Editions 21, 2003.
- Аполихин О.И., Сивков А.В., Комарова В.А., Просянников М.Ю., Голованов С.А., Казаченко А.В., et al. Заболеваемость мочекаменной болезнью в Российской Федерации (2005-2016 годы). Экспериментальная и клиническая урология 2018;4:4-14. [Apolikhin OI, Sivkov AV, Komarova VA, Prosyannikov M.Yu., Golovanov SA, Kazachenko AV, et al. The incidence of urolithiasis in the Russian Federation (2005-2016). Eksperimental'naya i klinicheskaya urologiya = Experimental and Clinical Urology 2018;4:4-14. (In Russian)].
- Stamatelou KK, Francis ME, Jones CA, Nyberg LM, Curhan GC. Time trends in reported prevalence of kidney stones in the United States: 1976-1994. Kidney Int 2003; 63(5):1817-23.
- Chen J, Hou XF, Wang G, Zhong QX, Liu Y, Qiu HH, et al. Terpene glycoside component from Moutan Cortex ameliorates diabetic nephropathy by regulating endoplasmic reticulum stress-related inflammatory response. J Ethnopharmacol 2016;193:433-444.
- Galvin DJ, Pearle MS. The contemporary management of renal and ureteric calculi. BJU Int 2006;98:1283–1288.
- Tan YH, Wong M. How significant are clinically insignificant residual fragments following lithotripsy? Curr Opin Urol 2005;15:127–131.
- Trinchieri A, Ostini F, Nespoli R, Rovera F, Montanari E, et al. A prospective study of recurrence rate and risk factors for recurrence after a first renal stone. J Urol 1999; 162 (1):27-30.https://doi.org/10.1097/00005392-199907000-00007.
- Rule AD, Lieske JC, Li X, Melton LJ 3rd, Krambeck AE, Bergstralh EJ. The ROKS nomogram for predicting a second symptomatic stone episode. J Am Soc Nephrol 2014;25(12): 2878–2886. https://doi.org/10.1681/ASN.2013091011.
- Chua ME, Park JH, Castillo JC, Morales ML. Terpene compound drug as medical expulsive therapy for ureterolithiasis: a meta-analysis. Urolithiasis 2013; 41(2):143-51.
- Сивков А.В., Черепанова Е.В., Шадеркина В.А. Применение фитопрепаратов на основе терпенов при мочекаменной болезни. Экспериментальная и клиническая урология 2011;(1):69-72. [Sivkov A.V., CHerepanova E.V., SHaderkina V.A. Application of phytopreparations based on terpenes for urolithiasis. Eksperimental'naya i klinicheskaya urologiya = Experimental and Clinical Urology 2011;(1):69-72. (In Russian)].
- Lee CB, Ha US, Lee SJ, Kim SW, Cho YH. Preliminary experience with a terpene mixture versus ibuprofen for treatment of category III chronic prostatitis/chronic pelvic pain syndrome. World J Urol 2006;24(1):55-60.
- Медведев В.Л., Михайлов И.В., Розенкранц А.М., Ефремов М.Е., Муратов К.У., Буданов А.А. Применение растительной добавки на основе терпенов Ренотинекс® в комплексной терапии пациентов с мочекаменной болезнью. Урология 2020;1:00–00. [Medvedev V.L., Mihajlov I.V., Rozenkranc A.M., Efremov M.E., Muratov K.U., Budanov A.A. The use of herbal supplements based on terpenes Renotinex in the complex therapy of patients with urolithiasis. Urologiya = Urology 2020; 1: 00–00. (In Russian)]. https://doi.org/10.18565/urology.2020.1.00-00
- Круглов В.А., Асфандияров Ф.Р., Выборнов С.В., Сеидов К.С., Калашников Е.С., Ляшенко В.В. Литокинетическая терапия пациентов с мочекаменной болезнью. Экспериментальная и клиническая урология 2020;(2):105-111. [Kruglov V.A., Asfandiyarov F.R., Vybornov S.V., Seidov K.S., Kalashnikov E.S., Lyashenko V.V. Litokinetic therapy of patients with urolithiasis. Eksperimental'naya i klinicheskaya urologiya = Experimental and Clinical Urology 2020;(2):105-111. (In Russian)].
- Шадеркина В.А., Шадеркин И.А. Терпены и их применение в клинической практике. Экспериментальная и клиническая урология 2019;(1):75-78. [SHaderkina V.A., SHaderkin I.A. Terpenes and their use in clinical practice. Eksperimental'naya i klinicheskaya urologiya = Experimental and Clinical Urology 2019;(1):75-78. (In Russian)].
- Попков В.М., Основин О.В., Фомкина О.А. Результаты применения препарата на основе терпенов Ренотинекс® у пациентов с уролитиазом после дистанционной ударно-волновой литотрипсии. Урологические ведомости 2020; 10 (1): 39–42. [Popkov V.M., Osnovin O.V., Fomkina O.A. Results of using the drug based on terpenes Renotinex in patients with urolithiasis after extracorporeal shock wave lithotripsy. Urologicheskie vedomosti = Urological statements 2020;10(1):39–42. (In Russian)]. https://doi.org/10.17816/uroved10139-42







