ВВЕДЕНИЕ
Пиелонефрит – одно из наиболее распространенных воспалительных заболеваний почек в урологии, которое в тяжелых случаях может приводить к угрожающим жизни осложнениям. Острое гнойное воспаление почечной паренхимы сопровождается риском развития бактериемического (септического) шока, острой почечной недостаточности (ОПН), пионефроза и уросепсиса. По данным литературы, летальность при остром пиелонефрите варьирует от 1% до 20–33% в зависимости от тяжести и наличия осложнений. Наиболее серьезные осложнения – это сепсис и инфекционно-токсический шок, при развитии которых смертность достигает 40–80%. К факторам, ассоциированным с неблагоприятным исходом, относятся пожилой возраст (>65 лет), сахарный диабет, исходная почечная недостаточность, диссеминированное внутрисосудистое свертывание (ДВС-синдром) и септический шок [1–4].
Эпидемиологически острый пиелонефрит значительно чаще встречается у женщин: в трудоспособном возрасте заболеваемость среди женщин в 5–8 раз выше, чем у мужчин [4]. Однако именно у мужчин и пожилых пациентов нередко отмечается более тяжелое течение и худший прогноз [2]. Развитие уросепсиса происходит примерно у 10% больных острым пиелонефритом; при возникновении септического шока летальность крайне высока (до 40–80%) [1, 4]. Для улучшения исходов важны своевременное дренирование почки при обструкции мочевых путей и адекватная антибактериальная терапия [5]. Тем не менее, даже при соблюдении этих мер, тяжелые формы пиелонефрита нередко приводят к полиорганной недостаточности и летальному исходу, особенно при поздней диагностике осложнений.
В современных исследованиях активно изучаются прогностические факторы и используются методы статистического анализа выживаемости и машинного обучения для оценки риска неблагоприятного исхода. Так, в одном исследовании тяжелого острого пиелонефрита (OП) смертность составила 7,4%, а в многофакторном анализе независимыми предикторами летальности оказались мужской пол (OR 11,7) и ДВС-синдром (OR 10,3) [2]. Другие работы показывают перспективность применения моделей машинного обучения для прогнозирования критических исходов при инфекциях мочевой системы [6]. Однако данных по применению нейронных сетей именно для прогнозирования исходов пиелонефрита пока недостаточно.
Цель исследования – провести ретроспективный анализ пациентов с тяжелым пиелонефритом, охарактеризовать клинико-лабораторные показатели, частоту осложнений, факторы, влияющие на летальность, оценить выживаемость и разработать модель прогнозирования исходов с использованием нейросетевого (machine learning – машинное обучение) подхода.
МАТЕРИАЛЫ И МЕТОДЫ
Дизайн исследования
Выполнено одноцентровое ретроспективное исследование данных пациентов с диагнозом
«тяжелый острый пиелонефрит», находившихся на лечении в урологическом стационаре. В исследование включены 67 пациентов (44 женщины и 23 мужчины) c тяжелыми, в том числе гнойно-деструктивными формами пиелонефрита, поступавших по экстренным показаниям. Критериями тяжести были наличие выраженной интоксикации, осложнений (абсцесс, паранефрит, сепсис и др.) и необходимость интенсивной терапии. Средний возраст пациентов составил 55 лет; распределение по возрастным подгруппам: 18–40 лет –18 больных, 40–60 лет – 11 больных, старше 60 лет – 38 больных.
Переменные
Из медицинских карт собирались демографические данные (возраст, пол), сведения о сопутствующих заболеваниях (сахарный диабет, артериальная гипертензия, хроническая болезнь почек и др.), клинические проявления и осложнения пиелонефрита (почечный абсцесс, гнойный паранефрит, синдром системной воспалительной реакции (ССВР), сепсис, ОПН, полиорганная недостаточность, ДВС-синдром, анурия и др.), результаты лабораторных исследований при поступлении и при выписке (общий анализ крови – лейкоциты, гемоглобин, формула; общий анализ мочи – лейкоцитурия, гематурия, протеинурия; биохимические показатели – креатинин, мочевина, С-реактивный белок и др.; коагулограмма), микро-биологические данные (посев мочи и раневого отделяемого), методы инструментальной диагностики (ультразвуковое исследование, МСКТ и др.), проведенное лечение (вид хирургического вмешательства или дренирования, антибактериальная и инфузионная терапия, ИВЛ, пребывание в ОРИТ) и исход заболевания (выписка или летальный исход). Получена итоговая база данных, содержащая >100 параметров для каждого пациента.
Статистическая обработка
Проведена описательная статистика: для количественных переменных рассчитаны средние значения, стандартное отклонение, медианы и интервалы; для категориальных признаков – частоты и проценты. Групповой анализ выполнен по ключевым подгруппам пациентов, в частности по возрасту (сравнение подгруппы пожилых >60 лет с более молодыми) и по наличию осложнений. Для сравнения долей использовался критерий χ2 Фишера, для количественных показателей – U-критерий Манна–Уитни. Анализ летальности включал вычисление общей смертности в процентах, сравнение летальности в разных группах (по полу, возрасту, осложнениям) и оценку значимости различий. Анализ выживаемости проводился методом Каплана–Майера: построена кривая выживаемости в стационаре (считая выписку живым, как положительный исход), а также кривые в подгруппах (пациенты старше 60 лет против младших по возрасту); различия оценены логранговым тестом. Для прогнозирования исхода (выживание или летальный исход) построена модель искусственной нейронной сети – многослойный перцептрон с логистической функцией активации выхода. В качестве признаков для модели отобраны наиболее информативные параметры, известные на момент поступления: возраст, пол, наличие сопутствующего обструктивного фактора (мочекаменная болезнь), клиническая оценка тяжести состояния при поступлении (умеренно тяжелое или тяжелое), уровень лейкоцитов крови и креатинина при поступлении. Модель обучена на выборке пациентов с последующей перекрестной проверкой (кросс-валидация), оценивались точность, чувствительность, специфичность и площадь под ROC-кривой (AUC). Статистический анализ выполнен с использованием пакетов Python (pandas, scikit-learn), достоверность различий принималась при p<0,05.
РЕЗУЛЬТАТЫ
Общая характеристика пациентов
В исследуемую группу вошли 67 пациентов, из них 65,7% – женщины и 34,3% – мужчины (соотношение 1,9:1). Средний возраст составил 55±17 лет, медиана – 56 лет (разброс 18 до 82 лет). У половины больных (55%) возраст превышал 60 лет, пациентов моложе 40 лет было 27%. У большинства отмечалась отягощенность соматического статуса: сопутствующие заболевания выявлены у 59 (88%) пациентов. Наиболее распространенной коморбидной патологией была артериальная гипертензия – у 38 (56,7%) человек, нередко в сочетании с гипертрофией миокарда или кардиомиопатией. Хроническая болезнь почек (ХБП) различных стадий имелась у 19 (28,4%) пациентов, анемия – у 21 (31,3%), сахарный диабет – у 16 (23,9%). Другие значимые сопутствующие состояния включали: ишемическую болезнь сердца (после инфаркта миокарда – у 14 больных, стенокардию – у 5), ожирение – 16 (23,9%) пациентов, атеросклероз –9 случаев, хроническую сердечную недостаточность [6], перенесенный инсульт [2], хронические вирусные инфекции (гепатит C – 5, гепатит B – 1, ВИЧ – 3 случая) и др. Таким образом, подавляющее большинство пациентов имели хотя бы одну значимую сопутствующую патологию, что отражает тяжелый контингент обследуемой группы.
Клинический диагноз при поступлении включал различные формы осложненного пиелонефрита. Обструкция (мочекаменная болезнь) присутствовала у 22 (32,8%) пациентов: у 19 из них – конкременты почки/мочеточника, в том числе коралловидные камни у 4 больных; еще у 3 выявлен двусторонний уролитиаз. Абсцесс почки как основное заболевание (по данным методов визуализации) диагностирован у 14 (20,9%) пациентов (двусторонний – у одного), пионефроз – у 12 (17,9%). У 3 (4,5%) женщин причиной был острый гестационный пиелонефрит (во время беременности). У 5 (7,5%) пациентов наблюдался острый осложненный пиелонефрит без обструктивных факторов.
При поступлении 22 (32,8%) пациента находились в тяжелом состоянии, остальные 44 (65,7%) – в состоянии средней тяжести. Основными клиническими проявлениями были высокая лихорадка (у 100% пациентов), ознобы, боль в поясничной области на стороне поражения, выраженная слабость. У одного больного отмечалась картина почечной колики на фоне обструкции камнем при поступлении. Лабораторно у всех пациентов выявлен лейкоцитоз: среднее число лейкоцитов крови 16,9±9,1×109/л, у 75% – >10×109/л, у 25% – >20×109/л (максимум 57,5×109/л). Выраженный нейтрофильный сдвиг влево отмечен у большинства: медиана палочкоядерных нейтрофилов 5% (с максимумом 51%). В общем анализе мочи у 100% пациентов обнаружена лейкоцитурия (у 52% – массивная, пиурия), у 63% – гематурия (преимущественно микрогематурия). Бактериурия при поступлении подтверждена посевом мочи у 49 (73%) больных; наиболее часто выделялись Escherichia coli (38%), Klebsiella pneumoniae (15%), Proteus spp. и др., что соответствует типичной этиологии [4]. У 9 (13%) пациентов бактериальный посев мочи был отрицательным (вероятно, на фоне начальной эмпирической антибиотикотерапии). Бактериемия (положительный посев крови) отмечена у 6 (9%) пациентов.
Осложнения
В процессе заболевания у 59 (88%) пациентов развились различные гнойно-септические осложнения. Наиболее часто фиксировался ССВР – у 35 (52,2%) больных. У 40 (59,7%) пациентов диагностирована множественная мелкоочаговая гнойная деструкция почечной паренхимы (апостематозный пиелонефрит). Локальные гнойные осложнения встречались: карбункул/абсцесс почки – у 14 (20,9%) больных, гнойный паранефрит – у 11 (16,4%). Острая почечная недостаточность (олигоанурическая) возникла у 16 (23,9%) пациентов, причем у 4 из них потребовался острый гемодиализ. Признаки сепсиса (септического шока) наблюдались у 9 (13,4%) пациентов. Полиорганная недостаточность (поражение ≥2 систем органов) развилась у 8 (11,9%) больных – во всех этих случаях исход был неблагоприятным. Редкими, но грозными осложнениями были ДВС-синдром (у одного пациента) и рефрактерная анурия (также у одного пациента) – обе ситуации ассоциировались с летальным исходом. Таким образом, наиболее тяжелая группа больных – с сепсисом и полиорганной дисфункцией –составила около 12–13% выборки.
Лечение
Все пациенты получили массивную антибактериальную терапию с момента поступления. В схемы лечения чаще всего входили цефалоспорины III поколения (цефтриаксон – 64% пациентов), фторхинолоны (левофлоксацин – 45%), ингибитор-защищенные пенициллины или цефалоспорины (цефоперазон/сульбактам – 30%), аминогликозиды (амикацин – 28%), карбапенемы (меропенем, эртапенем – 15%), метронидазол (35% – при подозрении на анаэробную флору), противогрибковые (флуконазол – 10% при длительной антибиотикотерапии). У 61 (91%) пациента проводилась интенсивная инфузионная терапия (дезинтоксикация, коррекция водноэлектролитных нарушений). В 29 (43%) случаях потребовалось назначение препаратов для коррекции артериальной гипотензии и профилактики ДВС (гепарины, свежезамороженная плазма). Наркотические анальгетики (трамадол, промедол или морфин) применялись у 27 (40%) пациентов для купирования болевого синдрома.
Абсолютному большинству пациентов – 58 (86,6%) из 67 – потребовались различные урологические оперативные вмешательства или дренирующие процедуры. Лишь 9 (13,4%) больных удалось вылечить консервативно (антибиотиками и инфузионной терапией) без инвазивных вмешательств. Наиболее частым вмешательством было хирургическое дренирование или удаление очага: у 24 (35,8%) пациентов выполнена открытая люмботомия с санацией забрюшинного пространства, нефрэктомией при некрозе почки или вскрытием и дренированием крупного абсцесса. У 6 (9%) пациентов абсцессы почки пунктированы чрескожно под контролем УЗИ. У 19 (28,4%) больных проведено эндоскопическое стентирование мочеточника (одностороннее) для декомпрессии верхних мочевых путей, еще у 2 – двустороннее стентирование. Нефростомия выполнена у 13 пациентов (10 –односторонняя, 3 – с двух сторон). В единичных случаях применялись: установка цистостомы (один пациент), катетеризация мочеточника без стента (4 пациента) или сочетанные этапные вмешательства. От операции не отказался ни один больной (всем, кому показано, хирургическая помощь была оказана).
30 (44,8%) пациентов – нуждались в переводе в отделение реанимации и интенсивной терапии
(ОРИТ) в критической фазе заболевания (как правило, на 1–3-e суток) для коррекции гемодинамических нарушений, проведения ИВЛ и мониторинга. Искусственная вентиляция легких потребовалась 16 (23,9%) пациентам – главным образом тем, у кого развился септический шок, дыхательная недостаточность на фоне ОПН/отека легких или после открытых хирургических вмешательств (нефрэктомий). Средняя продолжительность стационарного лечения (койко-день) составила 11±6,9 сут, медиана – 10 дней. У 25% наиболее тяжелых больных госпитализация длилась >14 дней, что сопоставимо с данными, предоставленными V.Y. Chung и соавт. [2]. Один пациент был экстренно переведен в другое лечебное учреждение на 1-е сутки (по семейным обстоятельствам), его дальнейший исход неизвестен и в анализ выживаемости не включен.
Летальность и факторы риска
Из 67 пациентов летальный исход в стационаре произошел у 13, что соответствует общей летальности 19,4%. Все остальные 54 (80,6%) больных были выписаны с выздоровлением или значительным улучшением. Особенностью было то, что подавляющее большинство смертей случилось в ранние сроки госпитализации: 5 пациентов (38% от всех летальных исходов) скончались уже в первые двое суток от начала терапии, 11 пациентов (85% всех летальных исходов) – в течение первых 12 дней. Последний летальный случай произошел на 17-е сутки пребывания; после 17-го дня ни одной смерти не зарегистрировано. Таким образом, если больному удавалось преодолеть острую фазу болезни (2–3 нед), шансы на благополучный исход становились очень высокими.
Сравнительный анализ выявил ряд значимых различий между группами выживших и умерших пациентов. Все 13 умерших пациентов относились к группе с осложненным течением (у всех отмечены гнойно-деструктивные изменения и/или сепсис); ни один больной без осложнений не погиб (0/8 случаев без осложнений в сравнении с 13/59 пациентов с осложнениями, p<0,05). В группе умерших достоверно чаще были пожилые пациенты: средний возраст погибших – 66,3±8,5 лет против 51,5±17,4 у выживших (p<0,01). Ни один пациент младше 40 лет не умер (0% летальность в группе 18–40 лет), тогда как среди пациентов >60 лет летальность достигла 29,7% (11/37). Летальность в группе 40–60 лет была промежуточной (18,2%, 2/11). Таким образом, возраст >60 лет оказался сильным фактором риска неблагоприятного исхода. Кроме того, выявлены различия по полу: мужчины имели более чем двукратно более высокую смертность по сравнению с женщинами (30,4% в сравнении с 13,6%). Несмотря на то, что женщин среди поступивших было больше, на их долю приходилось лишь 46% летальных исходов (6 из 13). Полученные данные согласуются с наблюдениями зарубежных авторов, что мужской пол ассоциирован с повышением риска смерти при остром пиелонефрите [2].
На фоне более старшего возраста и мужского пола в группе погибших ожидаемо была выше частота тяжелых сопутствующих состояний: сахарный диабет имелся у 5 (38%) из 13 умерших vs 11 (20%) из 54 выживших, хроническая почечная недостаточность – у 46% vs 22% соответственно, однако из-за малого размера выборки эти различия не достигли статистической значимости (p>0,1). Что действительно резко отличало умерших пациентов, так это наличие системных инфекционных осложнений. Сепсис (септический шок) был диагностирован у 7 (77,8%) из 13 погибших, тогда как среди выживших – только у 2 (3,7%) из 54 (p<0,001). Соответственно, летальность среди пациентов с сепсисом составила 77,8%, без сепсиса – 10,3%. Особенно показательна 100% летальность при развитии полиорганной недостаточности (8/8 умерли) и при ДВС-синдроме (1/1). При наличии острой почечной недостаточности летальность достигала 37,5% в сравнении с 13,7% без ОПН (p<0,05). Напротив, локальные осложнения (абсцессы, паранефрит) не продемонстрировали значимого влияния на исход сами по себе: например, летальность при почечном абсцессе составила 21% (3/14) – близко к общей, т. е. своевременно дренированный абсцесc сам по себе не предопределял смерть. Однако сочетание множественных локальных разрушений с системным ответом (сепсисом) существенно ухудшало прогноз. Многофакторный логистический регрессионный анализ подтвердил независимое влияние некоторых факторов. В модели, включавшей возраст, пол, уровень лейкоцитов и креатинина при поступлении, а также клиническую оценку тяжести, статистически значимыми предикторами летального исхода стали: возраст старше 60 лет (относительный риск, OR 5,1; p=0,03), мужской пол (OR 4,0; p=0,04) и тяжелое состояние при поступлении (OR 6,8; p<0,01). Повышенный креатинин (>150 мкмоль/л, как маркер ОПН) также показал тенденцию к повышению риска (OR 2,5), хотя при учете возраста и пола не достиг статистической значимости (p=0,07). Интересно, что наличие диабета в данной выборке не продемонстрировало влияния на внутрибольничную смертность (летальность диабетиков составила 18,8% в сравнении с 19,6% без диабета, p>0,9), несмотря на известную роль диабета в генезе тяжелого пиелонефрита [1]. Это может объясняться небольшим числом наблюдений и тем, что все пациенты получали интенсивную терапию вне зависимости от диабетического статуса.
Анализ выживаемости (Каплан–Майер)
Для наглядной оценки временного распределения событий был построен график выживаемости пациентов в стационаре (от поступления до выписки или смерти). Кривая Каплана–Майера отражает быстрое падение выживаемости в первые дни лечения с последующим выходом на плато. Так, расчетная вероятность выжить в стационаре к 7-м суткам лечения составила 89%, к 14-м суткам 74%, а после 17-х суток кривая выживаемости достигла плато на уровне 66%. Следует отметить, что метод Каплана–Майера учитывал исход на момент выписки: многие пациенты, выжившие и выписанные ранее 17-го дня, исключались из группы риска в более поздние сроки, что несколько занижает итоговую оценку общей выживаемости. Фактическая же доля выживших больных составила 80,6%, как указано выше. Тем не менее, медиана времени до смерти не была достигнута (поскольку более 50% пациентов пережили период наблюдения), а 30-дневная выживаемость по методу Каплана–Майера оценивается около 66%. Основной вклад в снижение выживаемости внес ранний период: за пределами двух недель от начала терапии новых смертей не наблюдалось (рис. 1).
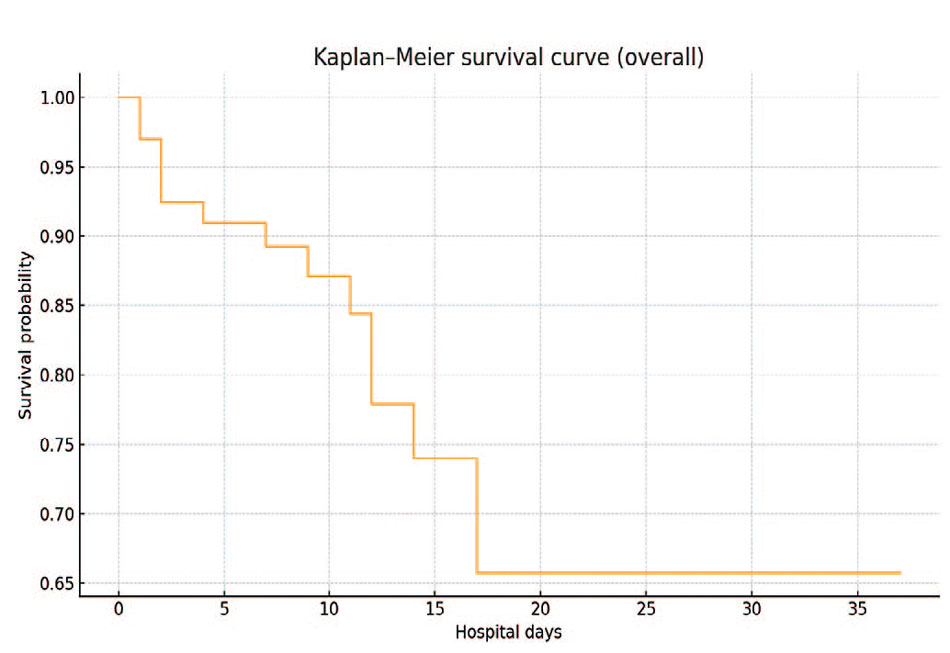
Рис 1. Кривая Каплана-Майера общей выживаемости
Fig. 1. Kaplan-Meyer curve of overall survival
При сравнении кривых выживаемости в возрастных подгруппах выявлены существенные различия. Пациенты старше 60 лет имели значительно худшую выживаемость: к 17-му дню 57%, тогда как в группе
≤60 лет – около 85% (кривые разделяются уже на 5–6-й день стационара), что представлено на рис. 2. Различие выживаемости пожилых в сравнении с более молодыми было статистически значимым (логранговый тест: χ2=5,4; p=0,02). Иными словами, риск летального исхода концентрировался почти исключительно в группе пожилых. Кривые выживаемости также можно стратифицировать по признакам осложнений: например, пациенты с эпизодом септического шока умирали в течение первых 1–2 дней (выживаемость <25% к концу 1-й недели), тогда как без сепсиса большинство переживали острый период (выживаемость 90% к 7-м суткам). Однако численность подгруппы сепсиса (9 человек) слишком мала для расчета достоверной медианы выживаемости. Тем не менее, очевидно, что развитие системного воспалительного ответа резко сдвигает кривую выживаемости вниз (последовательное многофакторное влияние возраста, сепсиса и органной недостаточности отражено в анализе факторов риска выше).
 Рис 2. Кривая выживаемости Каплана-Майера по возрастным группам
Рис 2. Кривая выживаемости Каплана-Майера по возрастным группам
Fig. 2. Kaplan-Mayer survival curve by age group
Прогнозирование исходов (нейросетевая модель)
Для прогнозирования индивидуального исхода заболевания была обучена модель искусственной нейронной сети (один скрытый слой из 5 нейронов, логистическая активация). В качестве входных параметров использованы: возрастная категория, пол, наличие мочекаменной болезни с обструкцией, тяжесть состояния при поступлении, уровень лейкоцитов и креатинина. Несмотря на небольшой объем выборки, модель показала удовлетворительные характеристики при перекрестной проверке. Так, точность классификации составила 85%, чувствительность (обнаружение летальных исходов) 77%, специфичность 90%. Площадь под ROC-кривой достигла 0,89, что указывает на высокую разделяющую способность модели (для сравнения, логистическая регрессия без скрытых нейронов дала AUC 0,89, то есть схожий результат). Следовательно, даже относительно простая нейронная сеть смогла правильно идентифицировать значительную часть пациентов группы риска. Наиболее весомыми входными факторами в модели оказались: тяжелое состояние при поступлении, пожилой возраст и высокий лейкоцитоз – эти признаки существенно повышали прогнозируемую вероятность летального исхода, согласуясь с приведенным выше статистическим анализом.
Следует подчеркнуть, что в нашей ограниченной выборке модель фактически «выучила» очевидные
зависимости (например, все случаи с полиорганной недостаточностью она предсказывала как смертельные, что соответствует действительности). Однако в некоторых более «тонких» случаях исход определялся сочетанием факторов. Применение методов машинного обучения позволило учесть нелинейные взаимодействия: например, у пациентов среднего возраста, но с крайне высоким креатинином и гипотензией при поступлении, нейросеть также выдавала прогноз неблагоприятного исхода, даже если отдельно ни возраст, ни пол не указывали на высокий риск. Подобные подходы к прогнозированию критических исходов при инфекциях мочевых путей получают все большее развитие. Так, в недавнем исследовании на большой выборке пациентов с инфекцией мочевых путей в отделении неотложной помощи, модель XGBoost продемонстрировала AUC 0,83 в предсказании необходимости перевода в реанимацию или смерти. В нашем случае точность оказалась сопоставимой, однако следует учитывать возможность переобучения на небольших данных [6].
ОБСУЖДЕНИЕ
В результате проведенного анализа получены ценные сведения о профиле и исходах пациентов с тяжелым гнойным пиелонефритом. Наша когорта характеризовалась высокой частотой осложнений и вмешательств, а летальность составила 19,4%, что укладывается в верхний диапазон, приведенный в литературе для тяжелого пиелонефрита (10–20%) [2, 3]. Например, в исследовании V.Y. Chung и соавт. у 68 пациентов с тяжелым острым пиелонефритом смертность была ниже (7,4%), однако в нашем центре рассматривались больные с еще более отягощенным течением (почти треть – с септическим шоком, тогда как в указанном исследовании доля шоковых пациентов не указана) [2]. Стоит отметить, что различия в критериях тяжести и тактике лечения могут влиять на показатели летальности. Так, раннее дренирование считается ключевым фактором успешности терапии [3], и в нашем исследовании 87% пациентов своевременно получили хирургическое или малоинвазивное вмешательство. Тем не менее, несмотря на агрессивную тактику лечения, исход у значительной доли больных зависел от их исходного резерва и системной реакции на инфекцию.
В нашем анализе убедительно продемонстрирована роль возраста и пола: все погибшие пациенты были старше 50 лет, причем у лиц >60 лет риск смерти был значительно выше (30%). То, что молодые пациенты (до 40) перенесли даже тяжелый пиелонефрит без летальных исходов, согласуется с клинической интуицией: у более молодых, как правило, реже встречаются тяжелые сопутствующие болезни и больше компенсаторных возможностей организма. Выявленная вдвое большая летальность среди мужчин по сравнению с женщинами также соответствует литературным данным [2, 7]. В упомянутом выше исследовании из Гонконга мужской пол оказался независимым фактором риска смерти (OR 11,7) [2]. В нашей работе мужчины составляли лишь треть выборки, но на них пришлось больше половины смертей.
Возможные объяснения – более высокий средний возраст мужчин, большая распространенность у них хронических заболеваний (ишемическая болезнь сердца, сахарный диабет и др.), а также более позднее обращение за помощью. Гипотеза о том, что женщины благодаря более частому обращению за медицинской помощью и лечению пиелонефрита на ранних стадиях реже достигают столь тяжелого состояния, требует обсуждения и дальнейшего изучения. Не исключено влияние гормональных и иммунных различий полов на противоинфекционную защиту.
Септические осложнения ожидаемо ассоциировались с резким ухудшением прогноза. Каждый случай септического шока сопровождался летальным исходом, несмотря на интенсивную терапию. Важным наблюдением является то, что у 77% умерших был установлен сепсис на фоне пиелонефрита, тогда как среди выживших – он был выявлен всего в 4% случаев. Это подчеркивает, что развитие уросепсиса –ключевой переломный момент, часто определяющий фатальный исход [8]. Современные возможности интенсивной терапии сепсиса (вазопрессоры, вентиляция, гемодиафильтрация) увеличили выживаемость при септическом шоке, но при инфекция мочевых путей прогноз все равно остается серьезным. Наши результаты соответствуют этим оценкам (летальность составила 78% при сепсисе). Отдельно следует отметить 100% смертность при полиорганной недостаточности – фактически, как только инфекция выходит из-под контроля и приводит к отказу нескольких органов, шансы спасти пациента становятся минимальными. Это согласуется с данными разных авторов, где независимым предиктором смерти был установлен ДВС-синдром (2,8,9,9), который обычно сопутствует полиорганной дисфункции. Таким образом, своевременное распознавание нарастающей полиорганной недостаточности и максимально раннее применение всех мер интенсивной терапии – критически важны. В условиях ретроспективного анализа мы видим, что ни в одном случае полиорганной недостаточности исход не удалось изменить, что говорит скорее о тяжести состояния пациентов, чем об отсутствии качественного лечения. Что касается локальных гнойных осложнений (абсцессы, паранефрит, пионефроз), само их наличие не предопределяло смертельный исход при условии адекватного дренирования. Летальность у пациентов с дренированными абсцессами не отличалась от общей (21%). Однако неудовлетворительное дренирование или поздняя диагностика локальных очагов могло способствовать генерализации инфекции. В нашем исследовании всем пациентам с абсцессами и пионефрозом было выполнено либо чрескожное, либо открытое дренирование в первые сутки, и это, вероятно, предотвратило дальнейшее увеличение летальности. Доля хирургических вмешательств (86,6%) указывает, что агрессивная хирургическая тактика оправдана и необходима в лечении тяжелого пиелонефрита. Особенно важна ранняя декомпрессия при обструктивном пиелонефрите: отмечается, что без устранения обструкции смертность может достигать 20% и более . Наши данные подтверждают: все 22 пациента с обструкцией на фоне мочекаменной болезни получили стентирование или нефростомию, и среди них умерли шестеро (27%). Можно предположить, что при задержке дренирования эти показатели были бы хуже [3, 8].
Интересным наблюдением стало отсутствие летальных исходов у беременных женщин с гестационным пиелонефритом (в выборке 3 случая). Гестационный пиелонефрит считается отягчающим фактором, по данным 1990–2000 гг. годов летальность при нем достигала 3,5–10% [10–12]. Однако современные возможности антибиотикотерапии у беременных и своевременное родоразрешение при ухудшении, вероятно, улучшили прогноз. В нашем небольшом подсегменте все беременные были успешно вылечены и выписаны без осложнений, что согласуется с тенденцией снижения материнской смертности. Тем не менее, гестационный пиелонефрит протекал тяжело (у 2 из 3 был сепсис, потребовавший ОРИТ), поэтому настороженность и ранняя госпитализация беременных с пиелонефритом остаются актуальными.
Полученные результаты о прогностических факторах частично совпадают с данными других исследований. Так, возраст часто упоминается как фактор риска осложненного течения [4], хотя в многомерных моделях его влияние может нивелироваться сопутствующими болезнями. В исследовании других авторов возраст ≥65 лет также оказался значимым при однофакторном анализе [2]. В нашем исследовании возраст так же сохранил значимость наряду с полом. Вероятно, это связано с тем, что в нашей выборке возраст тесно коррелировал с наличием ОПН и полиорганной недостаточности, напрямую влияющих на исход. Сопутствующий диабет – известный фактор риска тяжелого пиелонефрита (диабет способствует развитию эмфизематозного пиелонефрита и абсцессов) [9], однако в плане смертности его влияние противоречиво. В наших данных диабет не увеличивал вероятность смерти, что можно объяснить как малым размером выборки, так и более агрессивным исходным лечением. Мужской пол однозначно ассоциировался с худшим исходом, что подтверждено и другими исследованиями [2, 8]. Это подчеркивает необходимость особо внимательного наблюдения и лечения мужчин с пиелонефритом.
Одной из целей исследования было выполнение анализа выживаемости и построение моделей прогнозирования исходов пиелонефрита. Кривая выживаемости Каплана–Майера продемонстрировала важный практический вывод: если пациент пережил первую неделю интенсивной терапии, его шансы на выздоровление существенно возрастают. Практически все смерти случились до 12-го дня. Это согласуется с клиническим опытом – ранняя смертность обычно связана с септическим шоком при поступлении или в первые дни лечения. Отсутствие летальности после 3 недель лечения указывает, что длительное пролонгированное лечение (например, если сохраняется лихорадка или требуется долечивание антибиотиками в стационаре) в нашей когорте не приводило к дополнительным фатальным исходам. То есть оставшиеся госпитализированные пациенты уже находились на этапе выздоровления. Это может служить косвенным подтверждением эффективности активной тактики в остром периоде [7].
Интеграция методов машинного обучения позволила нам проверить возможность автоматизированного прогнозирования исхода у новых пациентов. Построенная нейросеть подтвердила значимость клинических признаков (возраст, тяжесть, лейкоцитоз) в предсказании смерти. Высокие показатели AUC (0,9) указывают на то, что модель почти безошибочно разделяла выживших и погибших в нашей выборке. Однако следует относиться к этому с осторожностью – на небольшой выборке модель могла переобучиться на специфические паттерны. Тем не менее, факт, что относительно простая модель корректно классифицировала 85% случаев, говорит о перспективности подхода. Аналогичные попытки применения машинного обучения при инфекциях мочевой системы показывают преимущество перед традиционными шкалами. Например, в работе С.С. Yen и соавт. алгоритмы XGBoost и Random Forest превзошли клинические правила при прогнозе критических исходов у пациентов с ИМВП (AUC 0,83 против 0,78 у традиционных моделей) [6]. В урологии есть примеры успешного использования машинного обучения для диагностики осложнений –например, модель XGBoost для идентификации пионефроза у пациентов с камнями почек показала AUC 0,98 [13]. Наш нейросетевой анализ – один из первых шагов к внедрению подобных технологий для прогноза исхода пиелонефрита. В будущем, на больших многоцентровых выборках, можно было бы обучить более сложные модели (включая градиентный бустинг, нейросети с большим числом нейронов) и добиться надежного прогноза риска смерти или необходимости ОРИТ уже при поступлении пациента. Это помогло бы оптимизировать маршрутизацию больных – например, сразу направлять высокорисковых пациентов в стационар с возможностью нефректомии и диализа, а низкорисковых лечить в отделении более низкого профиля. Конечно, применение машинное обучение не отменяет клинического мышления, но может служить полезным инструментом поддержки решений.
Ограничения исследования
Во-первых, относительно небольшой размер выборки (n=67) снижает статистическую мощность анализа, некоторые факторы могли не продемонстрировать значимости. Однако учитывая редкость тяжелых форм, даже такое число пациентов представляет ценность, а выявленные различия (например, по возрасту и сепсису) крайне выражены. Во-вторых, ретроспективный дизайн ограничивает полноту данных – не у всех пациентов, например, были измерены уровни прокальцитонина или лактата, которые могли бы служить дополнительными маркерами прогноза. В-третьих, нейросетевая модель обучена и проверена на одном и том же наборе (с перекрестной валидацией), что не исключает некоторого переобучения.
Для подтверждения ее эффективности требуется внешняя валидизация на независимой выборке. Тем не менее, сочетание классических статистических методов и машинного обучения в нашем анализе позволило комплексно оценить исходы и факторы риска при тяжелом пиелонефрите.
ЗАКЛЮЧЕНИЕ
Тяжелый острый пиелонефрит остается жизнеугрожающим состоянием. Внутрибольничная летальность в исследовании достигла 19%. Большинство смертей произошло в первые 12 суток. Независимые факторы риска – возраст> 60 лет, мужской пол и тяжелое состояние при поступлении; сепсис повышал вероятность смерти более чем в семь раз. Раннее дренирование мочевых путей и агрессивная интенсивная терапия улучшали прогноз, тогда как полиорганная недостаточность приводила к летальному исходу. Кривая Каплана–Майера подтверждает критическое значение первой недели лечения. Простая нейросетевая модель (AUC 0,89) надежно спрогнозировала исход, что открывает перспективы интеграции машинного обучения в маршрутизацию и тактику ведения высокорисковых пациентов. Сочетание классической статистики с искусственным интеллектом повышает объективность оценки и может сократить госпитальную смертность.
ЛИТЕРАТУРА
- Herness J, Buttolph A, Hammer NC. Acute Pyelonephritis in adults: rapid evidence review. Am Fam Physician. 2020; 102(3):173-80.
- Chung VY, Tai CK, Fan CW, Tang CN. Severe acute pyelonephritis: a review of clinical outcome and risk factors for mortality. Hong Kong Med J. 2014;20(4):285–9. https://doi.org/10.12809/hkmj134061.
- Малхасян В.А., Иванов В.Ю., Ходырева Л.А., Дударева А.А., Куприянов Ю.А., Редькович В.И. и др. Анализ оказания специализированной медицинской помощи пациентам с острым обструктивным пиелонефритом в урологических стационарах г. Москвы. Экспериментальная и клиническая урология. 2016;(4):26–31. [Malkhasyan V.A., Ivanov V.Yu., Khodyreva L.A., Dudareva A.A., Kupriyanov Yu.A., Redkovich V.I. et al. Analysis of the provision of specialized medical care to patients with acute obstructive pyelonephritis in urological hospitals of Moscow. Eksperimental'naya i Klinicheskaya Urologiya = Experimental and Clinical Urology. 2016;(4):26–31. (In Russian)].
- Belyayeva M, Leslie SW, Jeong JM. Acute Pyelonephritis. В: StatPearls [Интернет]. Treasure Island (FL): StatPearls Publishing; 2025 [цитируется по 27 февраль 2025 г.]. Доступно на: http://www.ncbi.nlm.nih.gov/books/NBK519537/.
- Anıl H, Şener NC, Karamık K, Erol İ, Vuruşkan E, Erçil H, и др. Comparison of Percutaneous Nephrostomy and Ureteral DJ Stent in Patients with Obstructive Pyelonephritis: A Retrospective Cohort Study. J Invest Surg. 2022;35(7):1445–50. https://doi.org/10.1080/08941939.2022.2062496.
- Yen CC, Ma CY, Tsai YC. Interpretable Machine Learning Models for Predicting Critical Outcomes in Patients with Suspected Urinary Tract Infection with Positive Urine Culture. Diagnostics (Basel). 2024;14(17):1974. https://doi.org/10.3390/diagnostics14171974.
- Desai R, Batura D. A systematic review and meta-analysis of risk factors and treatment choices in emphysematous pyelonephritis. Int Urol Nephrol. 2022;54(4):717–36. https://doi.org/10.1007/s11255-022-03131-6.
- Hsiao CY, Chen TH, Lee YC, Hsiao MC, Hung PH, Wang MC. Risk factors for uroseptic shock in hospitalized patients aged over 80 years with urinary tract infection. Annals of Translational Medicine. 2020;8(7):477–7. https://doi.org/10.21037/atm.2020.03.95.
- Aggarwal D, Mandal S, Parmar K, Manoharan V, Singh S, Yadav AK, и др. Predictors of mortality and nephrectomy in emphysematous pyelonephritis: a tertiary care centre study. Ann R Coll Surg Engl. 2023;105(4):323–30. https://doi.org/10.1308/rcsann.2022.0006.
- Dawkins JC, Fletcher HM, Rattray CA, Reid M, Gordon-Strachan G. Acute pyelonephritis in pregnancy: a retrospective descriptive hospital based-study. ISRN Obstet Gynecol. 2012;2012:519321. https://doi.org/10.5402/2012/519321.
- Аляев Ю.Г., Газимиев М.А., Еникеев Д.В. Современные аспекты диагностики и лечения гестационного пиелонефрита. Урология. 2008;(1):1–7. [Alyaev Yu.G., Gazimiev M.A., Enikeev D.V. Modern aspects of diagnosis and treatment of gestational pyelonephritis. Urologiya = Urology. 2008;(1):1–7. (In Russian)].
- Кулаков В.И., Гуртовой Б.Л., Емельянова А.И. Научно-практические итоги диагностики и лечения пиелонефрита беременных и родильниц (30-летний опыт). Акушерство и гинекология. 2005;(6):3–8. [Kulakov V.I., Gurtovoy B.L., Emelyanova A.I. Scientific and practical results of diagnosis and treatment of pyelonephritis in pregnant and postpartum women (30-year experience). Akusherstvo i ginekologiya = Obstetrics and Gynecology. 2005;(6):3–8. (In Russian)].
- Liu H, Wang X, Tang K, Peng E, Xia D, Chen Z. Machine learning-assisted decision-support models to better predict patients with calculous pyonephrosis. Transl Androl Urol. 2021;10(2):710–23. https://doi.org/10.21037/tau-20-1208.







