ВВЕДЕНИЕ
Стриктура женской уретры в качестве причины инфравезикальной обструкции встречается достаточно редко. Различные авторы оценивают порог сужения уретры при калибровке от 12 до 20 Ш и большинство специалистов рассматривают диаметр уретры, равный 14 шкалам Шарьера, как диагностический критерий наличия стриктуры у женщин [1]. Диагностика данного патологического состояния ввиду отсутствия характерных специфических жалоб и четкого алгоритма диагностики, а также вследствие небольшого количества наблюдений затруднена. Тем не менее инфравезикальная обструкция уретры при отсутствии коррекции может приводить не только к появлению и прогрессированию симптомов нарушения функции нижних мочевыводящих путей (СНМП) и ухудшению качества жизни, но и к таким осложнениям, как хроническая задержка мочеиспускания, хроническая рецидивирующая инфекция нижних мочевыводящих путей, дивертикулы мочевого пузыря, камнеобразование, нарушение функции почек [2]. Также нет единого мнения по поводу оптимального метода лечения стриктуры уретры у женщин, применяется дилатация уретры, эндоскопические методы и пластика уретры.
МАТЕРИАЛЫ И МЕТОДЫ
Клинический случай
В Санкт-Петербургское государственное учреждение здравоохранения «Городская клиническая больница №31» обратилась пациентка 34 лет с жалобами на дискомфорт в области мочеиспускательного канала, учащение мочеиспускания, разбрызгивание струи мочи, необходимость натуживания для совершения мочеиспускания, повторные эпизоды инфекций нижних мочевыводящих путей. Из анамнеза установлено, что в 2023 году пациентке было выполнено оперативное вмешательство по иссечению парауретральной кисты. Спустя 6 месяцев после проведенного оперативного вмешательства появились вышеуказанные жалобы. С течением времени интенсивность их увеличилась. По данным объективного исследования сужения наружного отверстия уретры выявлено не было, женские наружные половые органы без патологических изменений. В акушерско-гинекологическом анамнезе 2 беременности и родоразрешение путем кесарева сечения. При оценке тонуса тазовых мышц по Оксфордской шкале выявлен нормотонус. По данным ультрасонографии нарушений уродинамики верхних мочевых путей (ВМП) не выявлено, остаточная моча не определялась. По данным урофлоуметрии выявлены максимальная скорость потока на уровне 21,7 мл/с, средняя – 8,4 мл/с (рис. 1).
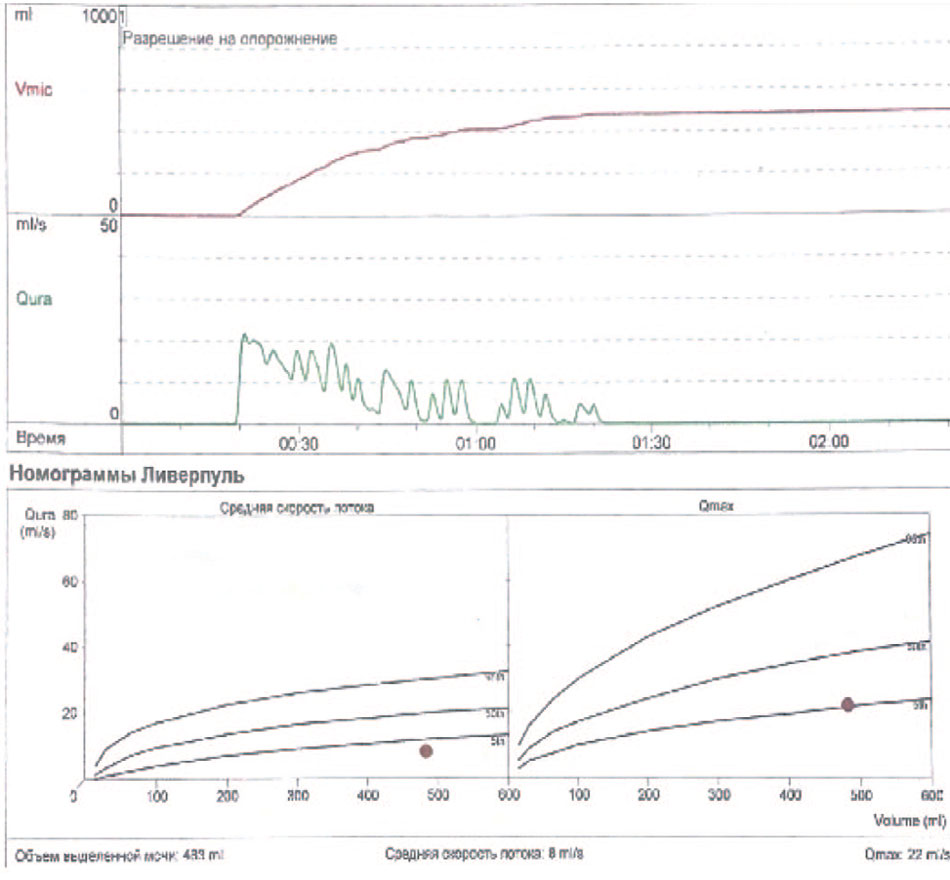
Рис. 1. Урофлоуметрия до оперативного лечения
Fig. 1. Uroflowmetry before surgical treatment
При выполнении микционной цистографии выявлено сужение просвета дистальной уретры протяженностью до 1,5 см (рис. 2).

Рис. 2. Микционная цистоуретрография до оперативного лечения
Fig. 2. Voiding cystourethrography before surgical treatment
Оперативное вмешательство выполнено под спинномозговой анестезией, оно состояло из двух этапов – забор трансплантата и его непосредственно уретропластика. Первый этап был выполнен под местной анестезией и заключался в заборе участка слизистой оболочки щеки размерами 1,5×3,0 см, отступая от отверстия выводного протока околоушной железы на 1,5 см. Затем в мочевой пузырь с техническими трудностями был проведен катетер Фоли СН 18. Далее выполнен полулунный разрез выше меатуса.
Произведена диссекция пространства между телом клитора и дорсальной частью уретры (рис. 3). Дорсальная уретры рассечена до появления здоровой слизистой. Слизистая трансплантата размещена в сторону просвета уретры (рис. 4). Края трансплантата фиксированы к краям рассеченной уретры узловыми швами vicryl 3-0. Края дистальной части трансплантата анастомозированы с краями супрамеатального разреза (рис. 5).
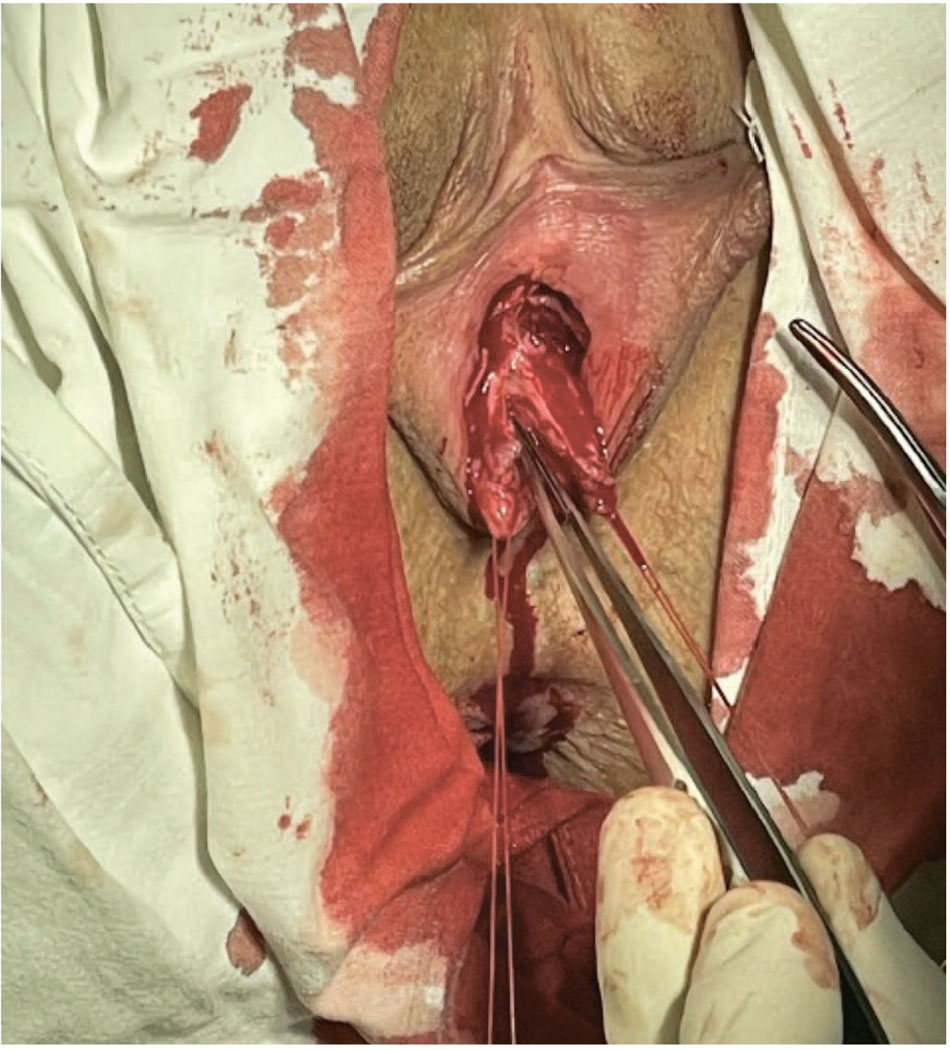
Рис. 3. Выделение уретры
Fig. 3. Urethral dissection
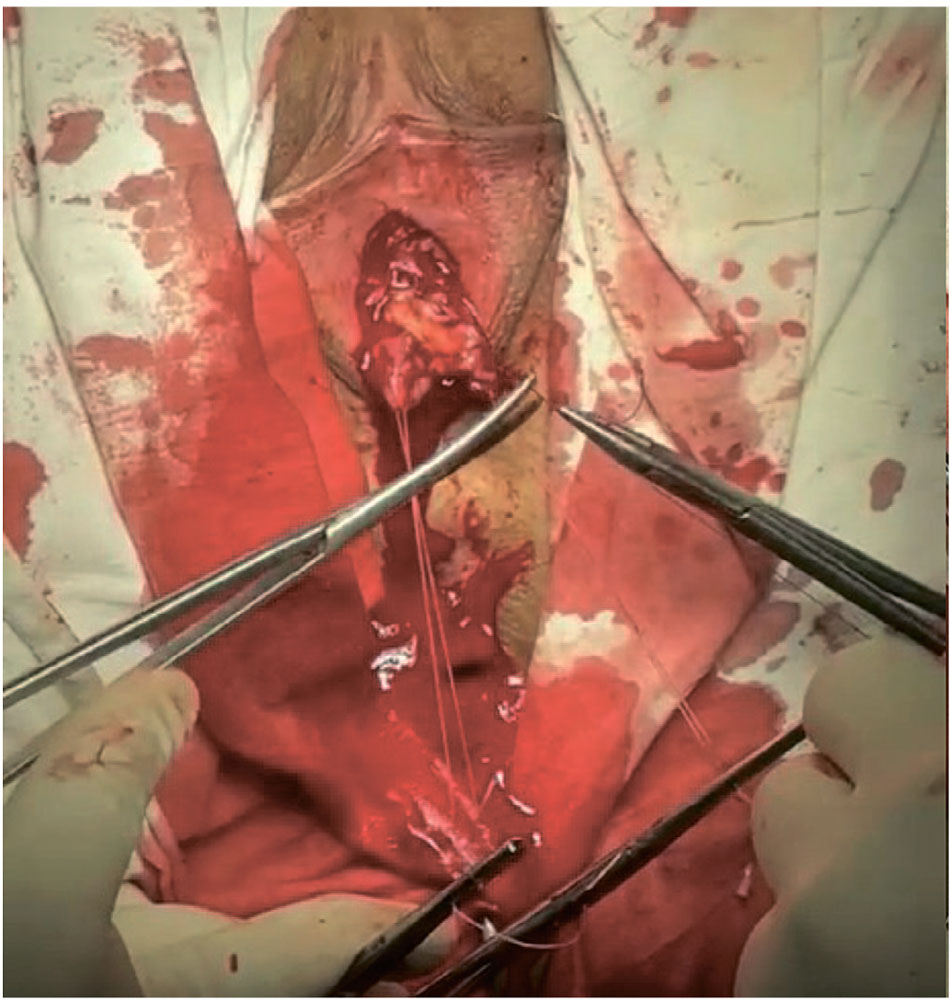
Рис. 4. Фиксация трансплантата
Fig. 4. Buccal graft fixation
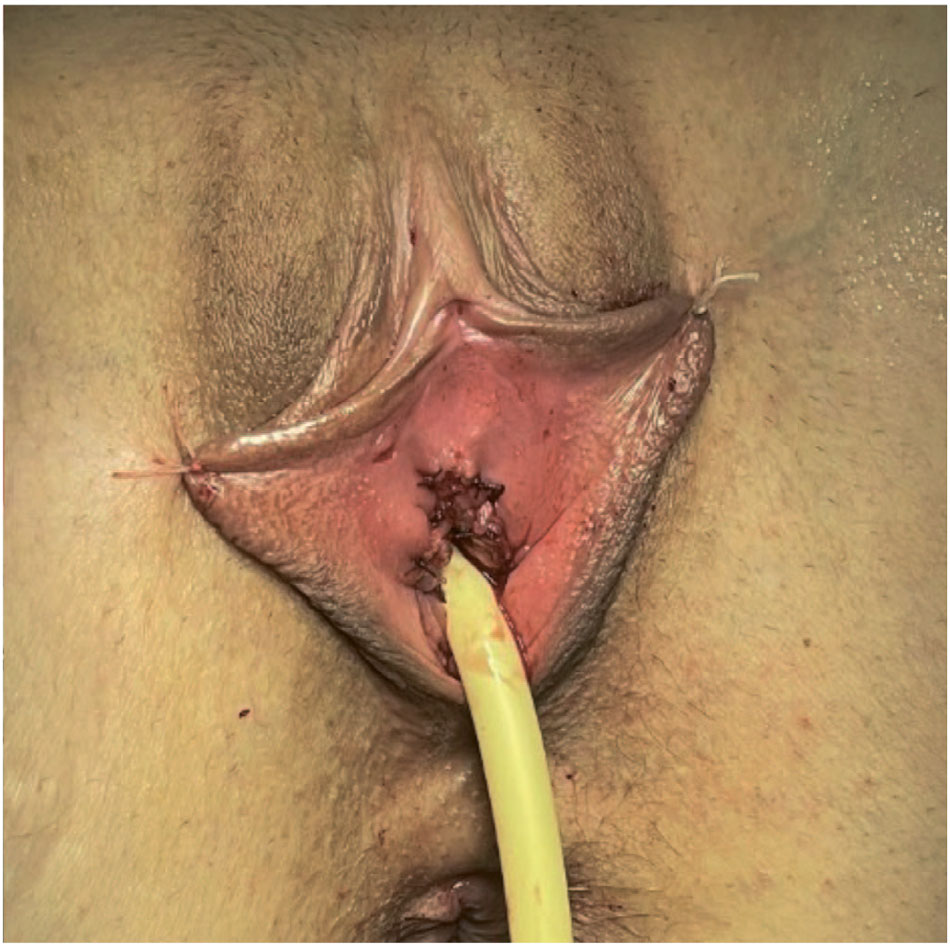
Рис. 5. Окончание операции.
Fig. 5. End of surgery
Послеоперационный период протекал гладко, осложнений отмечено не было. Проводилась рутинная антибактериальная, симптоматическая терапия. Уретральный катетер был удален на 5-е сутки. После восстановления самостоятельного мочеиспускания было выполнено ультразвукковое исследование (УЗИ) мочевого пузыря, резидуальной мочи выявлено не было.
Контрольное обследование было проведено через 3 и 6 месяцев после операции. Оно включало в себя выполнение урофлоуметрии, микционной цистоуретрографии, оценку количества остаточной мочи, субъективную оценку симптомов на основании заполнения опросника IPSS (International Prostate Symptom Score – Международная система оценки симптомов заболеваний предстательной железы) и шкалы UDI 6 (Urinary Distress Inventory – Шкала оценки расстройств мочеиспускания). Сумма баллов по опроснику IPSS составила 4, по шкале UDI 6 – 3 балла. Остаточной мочи при проведении ультрасонографии мочевого пузыря не отмечено. По данным урофлоуметрии объем опорожнения – 260 мл, максимальная скорость потока (Qmax) – 26,2 ml/с, средняя скорость потока (Qave) – 15,5 ml\с, тип кривой куполообразный (рис. 6).
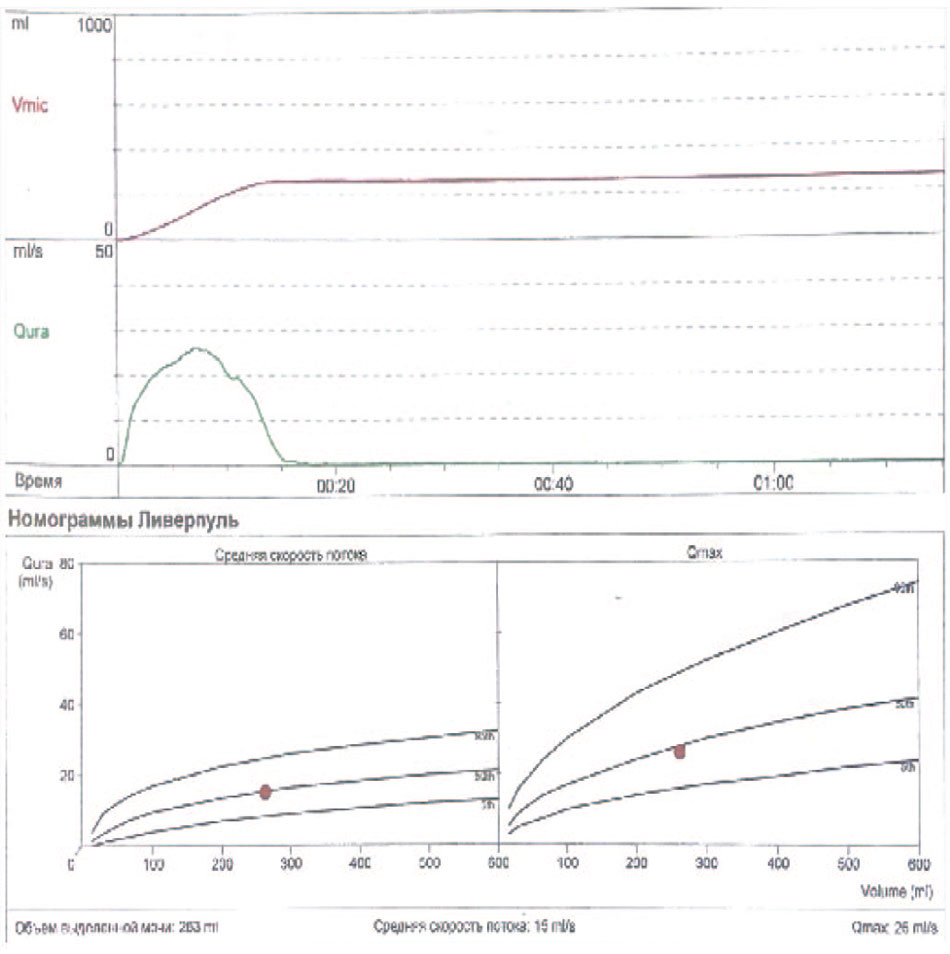
Рис. 6. Урофлоуметрия после оперативного лечения
Fig. 6. Uroflowmetry after surgical treatment
Микционная цистоуретрография – без особенностей, признаков стриктуры уретры не определяется (рис. 7).
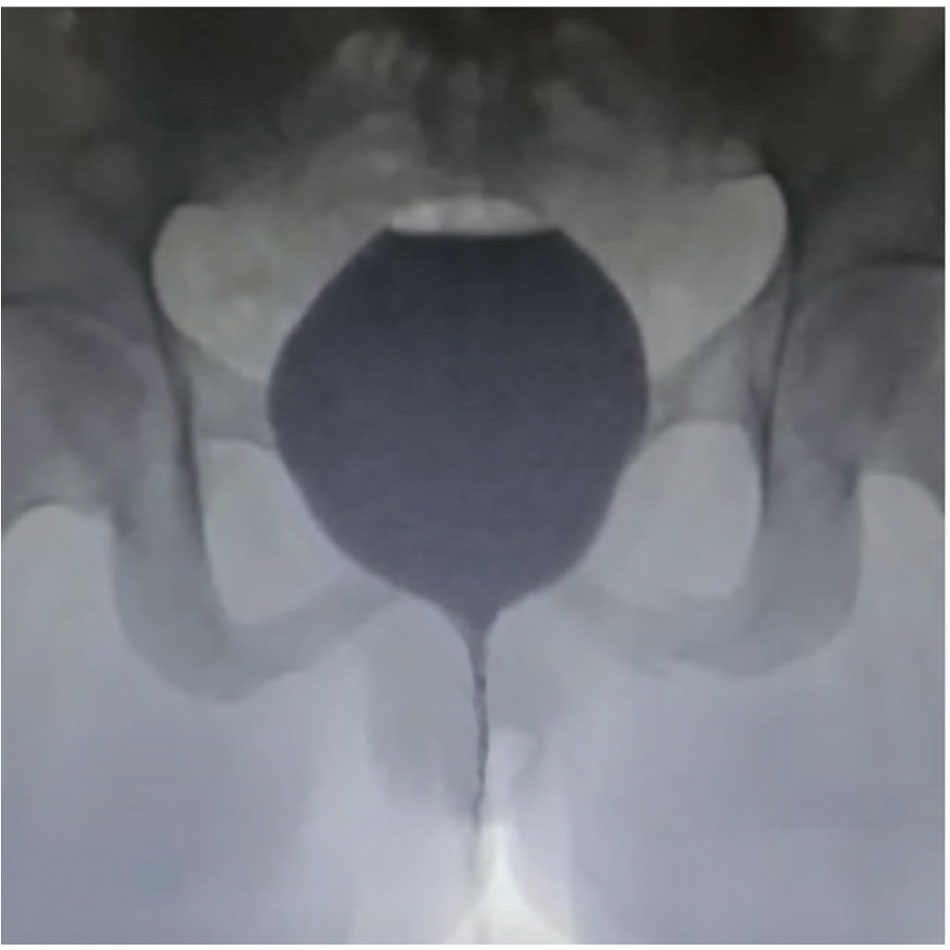
Микционная цистоуретрография после оперативного лечения
Fig. 7. Voiding cystourethrography after surgical treatment
ОБСУЖДЕНИЕ
Стриктура мочеиспускательного канала у женщин является относительно редкой причиной инфравезикальной обструкции. По данным литературы обструктивное мочеиспускание встречается в среднем у 3–8% женщин с СНМП и только в 4-13% случаев они вызваны сужением мочеиспускательного канала [3 – 7]. Отсутствие единого алгоритма диагностики, отсутствие специфичности предъявляемых пациентками жалоб существенно затрудняют постановку диагноза женской стриктурной болезни уретры (СБУ). Чаще всего стриктура мочеиспускательного канала у женщин носит ятрогенный характер: вследствие перенесенной дилатации уретры, травматичной катетеризации, оперативных вмешательств на мочеиспускательном канале – иссечения дивертикула уретры, удаления уретрального карункула, ушивания уретровлагалищного свища, имплантации субуретрального слинга по поводу стрессовой инконтиненции, а также в результате проведения лучевой терапии в области таза [3, 5, 8]. Также встречаются упоминания о стриктуре уретры в результате осложнений специфического воспалительного (туберкулезного) процесса, прогрессирования склеро-атрофического лихена, карциномы и фиброэпителиальных полипов уретры, лейомиомы уретры, осложнений трансуретральной резекции опухоли мочевого пузыря, крестцово-копчиковой тератомы или операций по смене пола [3, 5].
На данным момент нет единого мнения и четких клинических рекомендаций в аспекте диагностики СБУ у женщин. Диагноз стриктуры уретры невозможно поставить на основании только одних лишь жалоб. Прежде всего потому, что СНМП неспецифичны, а обструкция уретры у женщин может быть многофакторной и носить как анатомический, так и функциональный характер [4]. У пациенток отмечаются частые позывы на мочеиспускание, затруднение мочеиспускание, чувство неполного опорожнения мочевого пузыря. Нередко имеет место рецидивирующая инфекция мочевыводящих путей. Хроническая задержка мочеиспускания, формирование дивертикулов мочевого пузыря, развитие гидронефроза, хронического пиелонефрита и почечной недостаточности являются следствием клинически значимой СБУ у женщин [2].
Спектр обследования включает в себя УЗИ мочевого пузыря с определением остаточной мочи, урофлоуметрию, уретроцистоскопию, микционную цистоуретрографию, исследование «давление-поток». Основная задача такого исследования – оценка типа нарушения мочеиспускания, контрактильности детрузора и уровня обструкции.
В повседневной клинической практике инициальным методом лечения женской СБУ является дилатация уретры. Частота успешного результата при данной методики составляет в среднем около 51%, при повторной дилатации уретры процент успеха ниже и составляет около 27% [9]. Каждая последующая процедура приводит к более выраженному формированию периуретрального фиброза и ухудшает результаты дальнейшего лечения. Мы рекомендуем использовать этот метод лечения с осторожностью и при неэффективности первичного бужирования уретры в качестве следующего этапа рассматривать пластику мочеиспускательного канала.
В литературе описаны следующие методы оперативного лечения СБУ у женщин: меатопластика, уретропластика лоскутом передней стенки влагалища (Blandy), боковой стенкой влагалища (Orandi), вестибулярным лоскутом (Montorsi), уретропластика свободным трансплантатом в дорсальном или вентральном исполнении. Данных за преимущество какого из вышеперечисленных методов в настоящее время не представлено. Отчасти это связано с достаточно низкой частотой встречаемости данной патологии. Выбор тактики оперативного вмешательства основан на локализации стриктуры уретры, ее протяженности и навыках хирурга.
Учитывая жалобы пациентки, анамнез, данные обследования в качестве первичного метода лечения была выбрана уретропластика буккальным трансплантатом с дорсальным доступом. Аргументом против дорсального доступа при уретропластике может быть возможного повреждения сосудисто-нервного пучка, ведущего к клитору, однако анатомически он располагается далеко от зоны диссекции [10]. Преимуществами такого вида доступа в том, что ткани влагалища остаются интактными, что позволяет избежать таких послеоперационных осложнений, как уретровагинальный свищ и мешковидная деформация трансплантата [8].
ВЫВОДЫ
Стриктура уретры у женщин является достаточно редкой формой женской инфравезикальной обструкции. При выборе тактики лечения следует опираться на опыт хирурга, локализацию и протяженность стриктуры. Дорсальный доступ характеризуется более низким риском развития уретровагинальной фистулы, он более предпочтителен при планируемой установке субуретрального слинга. Данный клинический случай показывает эффективность уретропластики при стриктуре женской уретры.
ЛИТЕРАТУРА
- Osman NI, Mangera A, Chapple CR. A systematic review of surgical techniques used in the treatment of female urethral stricture. Eur urol 2013;64(6):965-73. https://doi.org/10.1016/j.eururo.2013.07.038.
- Romero Pérez P, Mira Llinares A. Complicaciones renales y ureterales de la estenosis uretral [Renal and ureteral complications of urethral stenosis. Actas Urol Esp 1995;19(6):432-40 (In Spanish)].
- Ackerman AL, Blaivas J, Anger JT. Female urethral reconstruction. Curr Bladder Dysfunct Rep 2010;5(4):225-232. https://doi.org/10.1007/s11884-010-0071-6
- Agochukwu-Mmonu N, Srirangapatanam S, Cohen A, Breyer B. Female urethral strictures: Review of diagnosis, etiology, and management. Curr Urol Rep 2019;20(11):74. https://doi.org/10.1007/s11934-019-0933-1
- Keegan KA, Nanigian DK, Stone AR. Female urethral stricture disease. Curr Urol Rep 2008;9(5):419-23. https://doi.org/10.1007/s11934-008-0071-7
- Nitti VW, Tu LM, Gitlin J. Diagnosing bladder outlet obstruction in women. J Urol 1999;161(5):1535-40.
- Önol FF, Antar B, Köse O, Erdem MR, Önol ŞY. Techniques and results of urethroplasty for female urethral strictures: our experience with 17 patients. Urology 2011;77(6):1318-24. https://doi.org/10.1016/j.urology.2011.01.017
- Hoag N, Chee J. Surgical management of female urethral strictures. Transl Androl Urol 2017;6(Suppl 2):S76-S80. https://doi.org/10.21037/tau.2017.01.20
- Romman AN, Alhalabi F, Zimmern PE. Distal intramural urethral pathology in women. J Urol 2012;188(4):1218-23. https://doi.org/10.1016/j.juro.2012.06.016
- Migliari R, Leone P, Berdondini E, De Angelis M, Barbagli G, Palminteri E. Dorsal buccal mucosa graft urethroplasty for female urethral strictures. J Urology 2006;176(4 Pt 1):1473-76. https://doi.org/10.1016/j.juro.2006.06.043







