ВВЕДЕНИЕ
Доброкачественная гиперплазия предстательной железы (ДГПЖ) является одним из самых распространенных заболеваний органов мочеполовой системы у мужчин [1, 2]. Средний возраст появления симптомов заболевания – 60 лет. Распространенность данного процесса увеличивается с возрастом [3, 4]. ДГПЖ встречается у 11,3% мужчин в возрасте 40-49 лет, у 81,4% – в 80 лет, у 95,5% мужчин – после 80 лет [5, 6]. По мнению С.J. Girman правильнее было бы называть ДГПЖ не заболеванием, а возрастным состоянием, связанным с естественным изменением уровня гормонов и процессами старения [7].
Выраженные симптомы нарушения функции нижних мочевых путей (СНМП), развивающиеся при ДГПЖ, влияют на качество жизни, причем даже сильнее, чем такие хронические заболевания как диабет, гипертония, стенокардия, подагра, а также рак предстательной железы (ПЖ), при этом качество жизни пациентов снижается по мере развития тяжести симптомов [8-10]. Поэтому страх развития СНМП и связанного с ними ухудшения качества жизни — это основная причина обращения пациентов с ДГПЖ к врачу в странах, где ключевым вопросом для мужчин является качество жизни [11]. Безусловно, качество жизни пациента — один из важнейших аспектов, которые надо учитывать при принятии решения о профилактике, прогрессии и развитии осложнений гиперплазии ПЖ. К сожалению, в России, как правило, к урологу обращаются мужчины с весьма выраженными симптомами нарушенного мочеиспускания, с гиперплазией ПЖ больших объемов, и, нередко, с осложнениями, вызванными ДГПЖ (острая или хроническая задержка мочи, хроническая почечная недостаточность и др.). Иными словами, специалист видит пациента тогда, когда речь идет не о профилактике, а об остановке прогрессии ДГПЖ и контроле над симптомами [3]. По данным эпидемиологического исследования, проведенным И.А. Корнеевым и соавт., в России СНМП фиксируются среди мужчин любого возраста, они снижают качество жизни, тесно связаны с сопутствующими метаболическимим нарушениями и эректильной дисфункцией. Авторы делают вывод о том, что мужчинам с расстройствами мочеиспускания показано комплексное обследование и лечение с учетом междисциплинарных аспектов проблемы [12].
К факторам риска прогрессирования заболевания относятся: возраст пациента старше 45 лет, выраженность симптомов по шкале International Prostate Symptom Score (IPSS) не менее 8 баллов, максимальная скорость мочеиспускания менее 15 мл/с, объем остаточной мочи более 50 мл, объем ПЖ более 30 см3, уровень простатспецифического антигена (ПСА) более 1,4 нг/мл [13]. Для выявления этих факторов риска необходимо включение в алгоритм профилактических осмотров обязательного заполнения мужчинами старше 40 лет опросника IPSS для оценки выраженности СНМП. Именно благодаря профосмотрам появляется возможность своевременного выявления и контроля над симптомами.
Все перечисленное, доказывает актуальность вопроса своевременного выявления симптомов и начала профилактики прогрессии и лечения ДГПЖ.
Все подходы к терапии ДГПЖ можно разделить на консервативные (немедикаментозное и медикаментозное лечение) и хирургические варианты. К консервативному немедикаментозному лечению относят динамическое наблюдение и поведенческую терапию. Динамическое наблюдение рекомендуется пациентам с неосложненными СНМП легкой/умеренной степени, которые не обеспокоены своими симптомами. Поведенческая терапия включает обеспечение пациента необходимым объемом знаний о заболевании и изменении образа жизни, способного привести к улучшению клинической картины заболевания. Поведенческая терапия может служить дополнением к лечению всех пациентов с ДГПЖ, которым предполагается проведение любого нехирургического вмешательства. К основным недостаткам поведенческой терапии можно отнести невозможность адекватного контроля над выполнением соответствующих рекомендаций и отсутствие патогенетического эффекта в отношении прогрессии гиперплазии ПЖ, поскольку эти рекомендации влияют исключительно на уменьшение симптоматических проявлений.
Однако большая часть пациентов (80-95%), страдающих ДГПЖ, подвергается медикаментозному лечению, которое подразумевает под собой различные варианты моно– или комбинированной терапии имеющимися в арсенале уролога лекарственными препаратами [14].
Цели медикаментозной терапии у пациентов с СНМП на фоне ДГПЖ можно разделить на долгосрочные и краткосрочные. К краткосрочным целям относятся устранение СНМП, увеличение скорости мочеиспускания, улучшение качества жизни, например, до выполнения хирургического лечения. К долгосрочным целям – длительное улучшение симптоматики, профилактика прогрессирования заболевания, увеличение скорости мочеиспускания, уменьшение объема ПЖ, а также снижение риска острой задержки мочи и необходимости оперативного вмешательства [15]. Длительная, пожизненная консервативная терапия ДГПЖ обусловлена этиологией и патогенезом заболевания, а также ее тенденцией к прогрессированию [16].
Арсенал медикаментозной терапии крайне разнообразен и включает как комбинированное назначение препаратов из нескольких фармакологических групп, так и монотерапию. Согласно рекомендациям Российского общества урологов, Европейской и Американской ассоциации урологов к методам медикаментозного лечения ДГПЖ, продемонстрировавшим эффективность, относятся α1-адреноблокаторы, ингибиторы 5α-редуктазы, антагонисты мускариновых рецепторов, ингибиторы фосфодиэстеразы 5 типа, β3-агонисты, комбинированная терапия (α1-адреноблокаторы + антагонисты мускариновых рецепторов, α1-адреноблокаторы + ингибиторы 5α-редуктазы) и др. [17-19]. Выбор группы препарата основан на преобладании и степени выраженности симптомов фазы опорожнения или накопления и может иметь различия при той или иной ситуации [17]. Большой выбор вариантов медикаментозной терапии ДГПЖ позволяет урологу индивидуально подходить к лечению каждого пациента [20].
Одним из вариантов своевременного контроля над ДГПЖ, предложенным Л.Г. Спиваком, были растительные экстракты [21]. Для раннего контроля над СНМП могут быть использованы биорегуляторные пептиды – биологически активный экстракт ПЖ бычков. Наиболее полный анализ отечественных фундаментальных и клинических исследований биорегуляторных пептидов представлен в мета-анализе И.А. Корнеева [22].
Разработки российских ученых и создание новых групп лекарственных препаратов для лечения пациентов с гиперплазией ПЖ требуют проведения дальнейших исследований, которые позволят оценить их эффективность и определить те категории пациентов, которым данная терапия наиболее целесообразна.
Целью настоящей работы явилась оценка эффективности ранней диагностики и приверженности к медикаментозной профилактике развития и прогрессии ДГПЖ с применением различных методов, в том числе и биорегуляторных пептидов.
МАТЕРИАЛЫ И МЕТОДЫ
Нами были проанализированы данные диспансеризации и периодических медосмотров мужчин, прикрепленных к ООО «Семейная поликлиника №4» по страховке или приходящих на так называемые «чекапы» по собственной инициативе. Мы применили программу «Комплекс мер по увеличению эффективности ранней диагностики ДГПЖ и повышению приверженности к медикаментозной профилактике развития и прогрессии ДГПЖ», разработанную и инициированную авторами статьи в 2017 году в регионе работы учреждения.
Программа состояла из двух этапов – эпидемиологического и клинического неинтервенционного.
Основная идея первого этапа программы состояла в определении профиля мужчины, имеющего необходимость в начале терапии СНМП, но при этом не обращавшегося к врачу.
Все мужчины осматривались профпатологом, кардиологом, урологом и другими специалистами. В случае выявления нарушений мочеиспускания врачуролог предлагал пройти пациенту более углубленное обследование и, при отсутствии критериев исключения, принять участие во втором неинтервенционном этапе. Дизайн исследования представлен на рисунке 1.
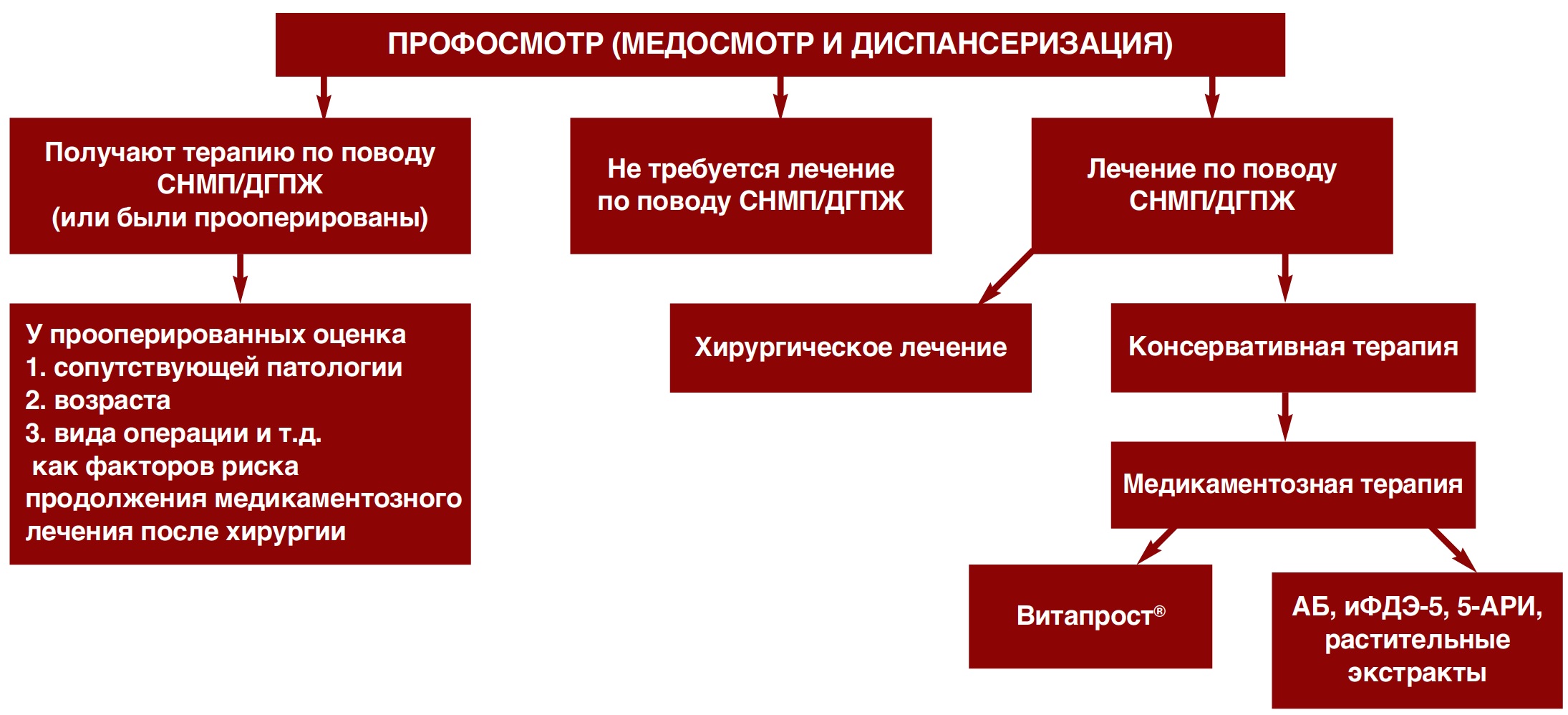
Рис. 1. Дизайн региональной программы
Fig. 1. Regional program design
Врач-уролог на приеме проводил сбор анамнеза, выполнял трансректальное ультразвуковое исследование (ТРУЗИ) ПЖ, ультразвуковое исследование мочевого пузыря до и после мочеиспускания, урофлоуметрию и другие обследования при необходимости. Далее специалист, исходя из результатов обследования, предлагал возможные варианты лечения. В зависимости от показаний пациентам рекомендовалось хирургическое или консервативное лечение – медикаментозное (α1-адреноблокаторы + антагонисты мускариновых рецепторов, α1-адреноблокаторы + ингибиторы 5α-редуктазы) или препараты линейки Витапрост® или немедикаментозное лечение (поведенческая терапия).
Эффективность и безопасность применения биорегуляторных пептидов у больных с ДГПЖ и СНМП сравнивалась с результатами лечения пациентов, выбравших поведенческую терапию (активное наблюдение).
Критерии включения в исследование:
• мужчины старше 40 лет;
• диагноз ДГПЖ, установленный в результате рутинного обследования пациента.
Критерии невключения:
• непереносимость препаратов Витапрост® Форте и Витапрост® в таблетках;
• обострение хронического простатита;
• медикаментозная или немедикаментозная терапия СНМП, обусловленных ДГПЖ;
• злоупотребление алкоголем, наркотиками.
Критерии исключения:
• желание пациента прекратить участие в программе на любом этапе ее проведения;
• решение исследователя, что продолжение участия в исследовании противоречит интересам пациента.
Критерии прекращения терапии:
• возникновение серьезных нежелательных реакций.
Регистрация нежелательных явлений проводилась с момента включения в исследование и до завершения исследования у всех пациентов на основании жалоб, физикального обследования, и при необходимости измерения артериального давления, частоты сердечных сокращений, частоты дыхания, температуры и анализа лабораторных результатов и инструментальных исследований.
В случае назначения медикаментозного лечения с использованием биорегуляторных пептидов (Витапрост®), больному давались рекомендации по курсовому применению этого лекарственного средства:
• суппозитории ректальные Витапрост® Форте – по 1 свече 1 раз в день;
• таблетки Витапрост®, покрытые кишечнорастворимой оболочкой внутрь, по 1 таблетке 2 раза в день;
• длительность курса лечения препаратами линейки Витапрост® при ДГПЖ – не менее 30 дней;
• курсы рекомендовалось повторять через 3-6 месяцев.
В случае если пациенту предлагалось немедикаментозное лечение (поведенческая терапия), то врачуролог давал подробные инструкции по ее проведению. Контрольное обследование предлагалось проходить не реже одного раза в год.
РЕЗУЛЬТАТЫ
Старт региональной программы произошел в 2017 году, сроки наблюдения за пациентами в группе, получавшей терапию препаратами Витапрост® Форте и Витапрост® в таблетках, а также пациентов, выбравших поведенческую терапию, составили 4 года.
Анализу подверглись данные, полученные в ходе профосмотров 1675 мужчин, проходивших обследование с 2017 по 2021 гг. Поведенческая терапия использована у 221 пациента с легкой и умеренной симптоматикой, 312 больным назначены препараты линейки Витапрост® (табл. 1).
Таблица 1. Распределение пациентов по группам
Table 1. Distribution of patients by group
| Группа / Group | Количество пациентов, n (%) Number of patients, n (%) |
|---|---|
| Не требуется лечение / No treatment required | 214 (13) |
| Уже на терапии / Already in therapy | 288 (17) |
| Уже прооперированы / Already operated | 69 (4) |
| Нуждается в операции / Needs surgery | 36 (2) |
| Активное наблюдение (поведенческая терапия) / Active monitoring (behavioral therapy | 221 (13) |
| Витапрост® Форте и Витапрост® в таблетках / itaprost®Forte and Vitaprost® tablets | 312 (19) |
| АБ, иФДЭ-5, 5-АРИ, фитопрепараты Adrenoblockers, PDE5, 5-ARI, phytotherapy | 535 (32) |
Возраст
Возраст мужчин, вошедших в региональную программу, колебался от 40 до 67 лет. По результатам анализа демографических показателей, мужчин до 50 лет было 685 человек, что составило практически 40% всех участников исследования. Еще 823 мужчины были в возрасте до 55 лет, что составило около 50% и оставшиеся 167 человек (10%) были старше 55 лет (табл. 2).
Таблица 2. Распределение мужчин по возрасту
Table 2. Distribution of men by age
| Возрастной диапазон (лет) Age range (years) |
Количество пациентов, n (%) Number of patients, n (%) |
|---|---|
| 40-44 | 224 (13,4) |
| 45-49 | 461 (27,5) |
| 50-54 | 823 (49,1) |
| 55-59 | 101 (6) |
| 60-67 | 66 (4) |
Обращает на себя внимание, что активное наблюдение относительно чаще (129 против 95 мужчин) выбирали пациенты из самой молодой группы – возрастной диапазон 40-44 года, в то время как мужчины в возрастном диапазоне 45-49 и 50-54 лет выбирали медикаментозную терапию. Этих мужчин было практически в два раза больше в диапазоне 45-49 и более чем в четыре раза – в диапазоне 50-54 лет (рис. 2).
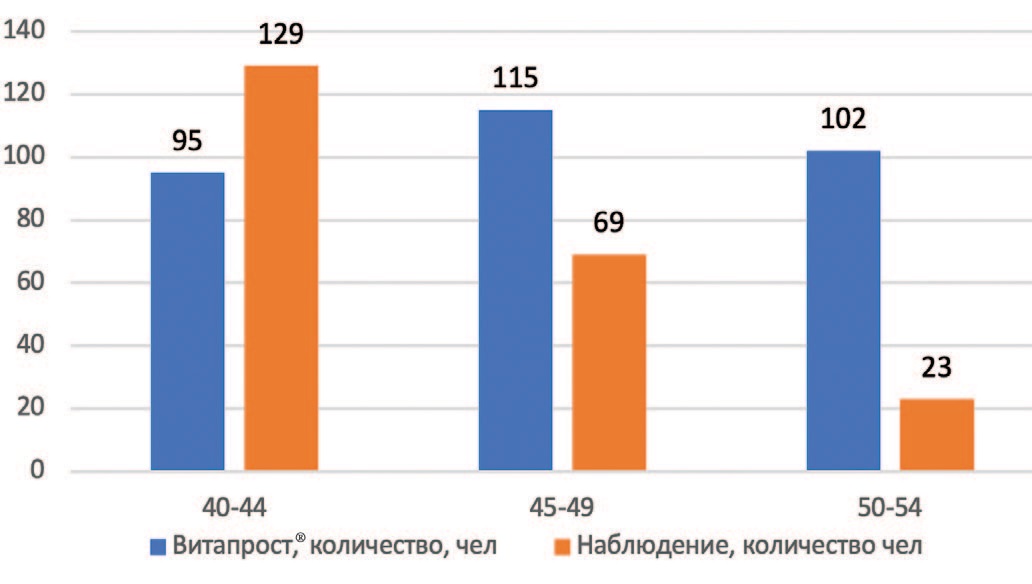
Рис. 2. Распределение пациентов по возрасту в зависимости от метода лечения (Витапрост® и активное наблюдение)
Fig. 2. Distribution of patients by age depending on the method of treatment (Vitaprost® and active monitoring)
Изменение субъективной оценки мочеиспускания при помощи опросника IPSS
В рамках программы на всех визитах в центр на приеме у врача-уролога пациенты самостоятельно заполняли опросник IPSS. Результаты представляются нам наиболее важными именно в отношении поставленных перед региональной программой задачами и целью.
Исходно, выраженность симптоматики в обеих группах была примерно одинаковой – 7-8 баллов. В группе немедикаментозной терапии (активное наблюдение) можно было наблюдать некоторое улучшение симптоматики в первые два года наблюдения – снижение баллов до 6, однако в последующем мы отметили ухудшение и усиление выраженности жалоб, согласно опроснику до 10-11 баллов. В группе пациентов, выбравших в качестве терапии курсы биорегуляторных пептидов (Витапрост® Форте и Витапрост® в таблетках), на протяжении всего времени наблюдения происходило снижение выраженности СНМП по шкале IPSS c 7 до 5 баллов (рис. 3).
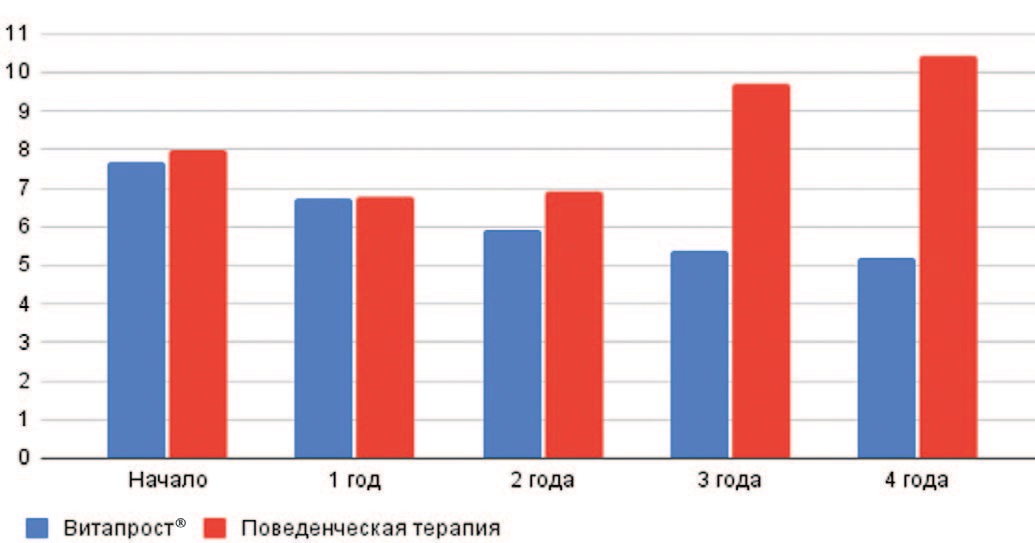
Рис. 3. Динамика IPSS в зависимости от метода лечения (Витапрост® и активное наблюдение)
Fig. 3. Dynamics of IPSS depending on the method of treatment (Vitaprost® and active monitoring)
Изменение объективной оценки мочеиспускания при помощи урофлоуметрии и измерения объема остаточной мочи
Максимальная скорость мочеиспускания (Qmax) и объем остаточной мочи у пациентов обеих групп изучались при помощи урофлоуметрии с последующим исследованием объема остаточной мочи при помощи УЗ-сканирования мочевого пузыря после мочеиспускания.
Обращает на себя внимание динамика показателей максимальной скорости мочеиспускания в группе пациентов, получавших курсы терапии препаратами Витапрост® Форте и Витапрост® в таблетках. В отличие от группы, выбравшей для себя поведенческую терапию, пациенты из группы медикаментозной терапии демонстрируют положительную динамику Qmax – увеличение показателей с 15 до 20 мл/сек. В группе поведенческой терапии за 4 года наблюдения скорость мочеиспускания не только не улучшилась, но несколько снизилась (рис. 4).
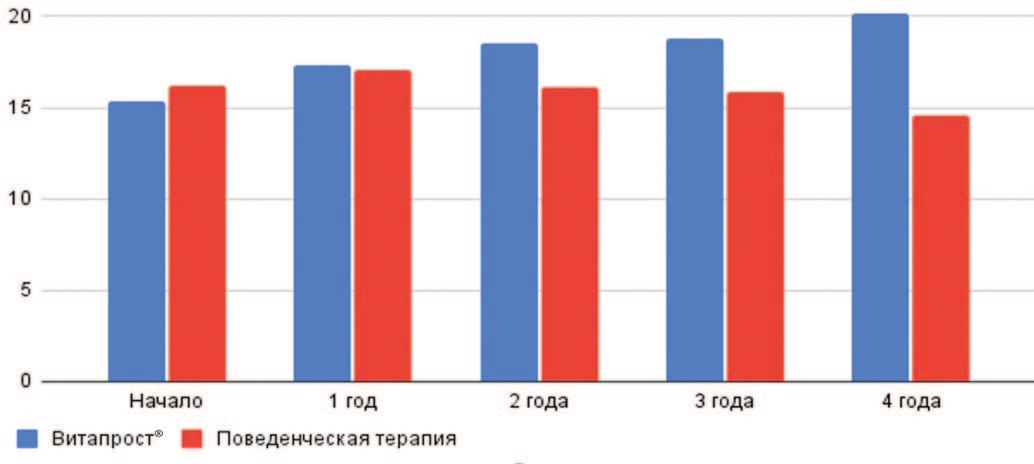
Рис. 4. Динамика Qmax в зависимости от метода лечения (Витапрост® и активное наблюдение)
Fig. 4. Dynamics of Qmax depending on the method of treatment (Vitaprost® and active monitoring)
Показатели остаточной мочи в обеих группах исходно были в пределах нормы, поскольку у мужчин не было выраженных нарушений мочеиспускания, а, следовательно, признаков ухудшения состояния детрузора тоже не было. В динамике мы также наблюдаем неплохие показатели объема остаточной мочи в обеих группах (рис. 5).
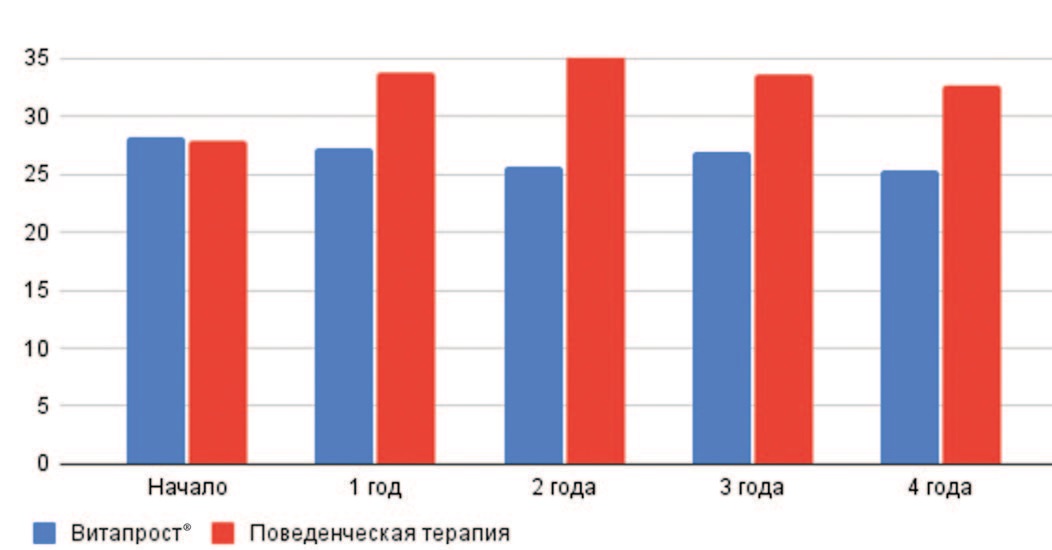
Риc. 5. Динамика объема остаточной мочи в зависимости от метода лечения (Витапрост® и активное наблюдение)
Fig. 5. Dynamics of the volume of residual urine depending on the method of treatment (Vitaprost® and active monitoring)
Изменение объема предстательной железы в ходе наблюдательной программы
Несмотря на то, что исходно в группе пациентов, выбравших Витапрост® Форте и Витапрост® в таблетках, объем ПЖ был несколько больше, чем в группе выбравших немедикаментозное лечение, за время наблюдения ситуация изменилась. Как видно из диаграммы, за 4 года объем ПЖ в группе пациентов, выбравших регуляторные пептиды в качестве патогенетической медикаментозной терапии, уменьшился с 35 см3 до 30 см3. В то же время, у пациентов, выбравших немедикаментозный путь контроля над симптомами мочеиспускания, объем предстательной железы прогрессивно увеличивался с 33 см3 до 40 см3 (рис. 6).
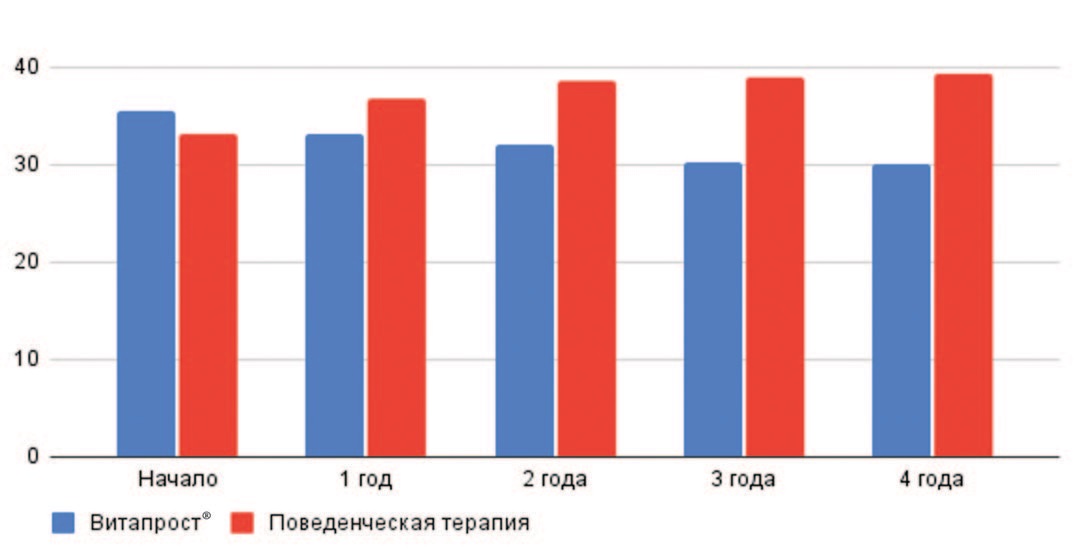
Риc. 6. Динамика объема ПЖ в зависимости от метода лечения (Витапрост® и активное наблюдение)
Fig. 6. Dynamics of prostate volume depending on the method of treatment (Vitaprost® and active monitoring)
Отмечен благоприятный профиль безопасности применения курсов Витапрост® Форте и Витапрост® в таблетках – никаких нежелательных явлений (НЯ), связанных с применением данного лекарственного средства, у пациентов не возникло. Количество НЯ в обеих группах было сопоставимо.
ОБСУЖДЕНИЕ
У больных с ДГПЖ и СНМП наиболее важными являются вопросы своевременного контроля над симптомами. Они актуальны еще и потому, что зачастую, даже выполняемое по показаниям хирургическое лечение, не приносит должного результата и требует продолжения симптоматического и патогенетического медикаментозного лечения. В 2021 году был опубликован обзор под названием «Postoperative medical treatment of lower urinary tract symptoms after benign prostatic hyperplasia surgery. Are we underestimating the problem? » в которой представлены данные, свидетельствующие о необходимости раннего начала контроля над симптомами нарушения функции нижних мочевых путей [23]. Нами показано, что, исходя из полученных данных, можно утверждать, что более, чем половине мужчин, пришедших на профосмотр, требовалось медикаментозное лечение, но при этом они его не получали и к урологу не обращались и никаких профилактических и лечебных мер ими не использовалось!
Одним из возможных препаратов для раннего контроля над СНМП являются биорегуляторные пептиды – биологически активный экстракт ПЖ бычков. Наиболее полный анализ отечественных фундаментальных и клинических исследований биорегуляторных пептидов представлен в метаанализе профессора И.А. Корнеева. Проанализировав результаты 9 исследований, проведенных российскими урологами, было сделано заключение, что полученные данные подтверждают эффективность применения препарата на основе ПЖ бычков при лечении пациентов с умеренно выраженными СНМП и инфравезикальной обструкцией, обусловленной ДГПЖ с целью снижения степени дизурии, повышения качества жизни и нормализации уродинамических показателей [22, 24]. При этом данные имеющихся клинических исследований доказали, что применение препарата Витапрост® уменьшает вероятность развития обострений хронического абактериального простатита, не вызывает изменений показателей клинического и биохимического анализа крови, общего анализа мочи. Витапрост® нормализует параметры секрета ПЖ и эякулята [24-27].
Результаты нашего исследования подтвердили эффективность и безопасность этого лекарственного препарата для контроля СНМП при ДГПЖ.
Оценка конечных точек была произведена и показала безусловное преимущество выбранной медикаментозной терапии в сравнении с поведенческой терапией. При применении линейки препаратов Витапрост® улучшились показатели по опроснику IPSS, увеличилась максимальная скорость мочеиспускания, уменьшился объем остаточной мочи и объем предстательной железы. Уровень ПСА на старте наблюдения у всех пациентов был в пределах нормы и оставался таковым до конца участия пациентов в региональной программе.
ВЫВОДЫ
Своевременное начало терапии препаратами Витапрост® Форте и Витапрост® в таблетках у пациентов с ДГПЖ обладает благоприятным профилем эффективности и безопасности. Объем данных, полученных в результате проведенной региональной программы, позволит в будущем более глубоко проанализировать отдельные ее аспекты и даст почву для размышления и обнадеживающих выводов.
ЛИТЕРАТУРА
1. Wei JT, Calhoun E, Jacobsen SJ. Urologic diseases in America project: benign prostatic hyperplasia. J Urol 2008;179(5Suppl):S75-80. https://doi.org/10.1016/j.juro.2008.03.141.
2. Launer BM, McVary KT, Ricke WA, Lloyd GL. The rising worldwide impact of benign prostatic hyperplasia. BJU Int 2021;127(6):722-8. https://doi.org/10.1111/bju.15286.
3. Trueman P, Hood SC, Nayak US, Mrazek MF. Prevalence of lower urinary tract symptoms and self-reported diagnosed ‘benign prostatic hyperplasia’, and their effect on quality of life in a community-based survey of men in the UK. BJU Int 1999;83(4):410–5. https://doi.org/10.1046/j.1464-410x.1999.00966.x.
4. Guess HA, Arrighi HM, Metter EJ, Fozard JL. Cumulative prevalence of prostatism matches the autopsy prevalence of benign prostatic hyperplasia. Prostate 1990;17(3):241-6. https://doi.org/10.1002/pros.2990170308.
5. Раснер П.И., Сивков А.В., Харчилава Р.Р. Доброкачественная гиперплазия предстательной железы. Клинические рекомендации. (Утверждены Министерством здравоохранения Российской Федерации 2020;54 с. [Rasner P.I., Sivkov A.V., Kharchilava R.R. Benign prostatic hyperplasia. Clinical recommendations. (Approved by the Ministry of Health of the Russian Federation 2020;54 p. (In Russian)].
6. Лопаткин Н.А. Урология. Национальное руководство. Гэотар-Медиа 2013;352-389 с. [Lopatkin N.A. Urology. National leadership. Geotar-Media 2013;352-389 p. (In Russian)].
7. Girman CJ. Population-based studies of the epidemiology of benign prostatic hyperplasia. Br J Urol 1998;82(Suppl.1):34-43. https://doi.org/10.1046/j.1464-410x.1998.0820s1034.x.
8. Welch G, Weinger K, Barry MJ. Quality-of-life impact of lower urinary tract symptom severity: results from the Health Professionals Follow-Up Study. Urology 2002;59(2):245–50. https://doi.org/10.1016/s0090-4295(01)01506-0.
9. Batista-Miranda JE, Molinuevo B, Pardo Y. Impact of lower urinary tract symptoms on quality of life using Functional Assessment Cancer Therapy scale. Urology 2007;69(2):285–8. https://doi.org/10.1016/j.urology.2006.09.054.
10. Girman CJ, Epstein RS, Jacobsen SJ, Guess HA, Panser LA, Oesterling JE, et al. Natural history of prostatism: impact of urinary symptoms on quality of life in 2115 randomly selected community men. Urology 1994;44(6):825-31. https://doi.org/10.1016/s0090-4295(94)80165-7.
11. Sells H, Donovan J, Ewings P, MacDonagh RP. The development and validation of a quality-of-life measure to assess partner morbidity in benign prostatic enlargement. BJU Int 2000;85(4):440–5. https://doi.org/10.1046/j.1464-410x.2000.00525.x.
12. Korneyev I., Alexeeva T., Al-Shukri S., Bernikov A., Erkovich A., Zhuravlev V., et al. Revalence of lower urinary tract symptoms among male population in Russian Federation: analysis of population study results. Georgian Medical News 2015;4(241):7–14.
13. Anderson JB, Roehrborn CG, Schalken JA, Emberton M. The progression of benign prostatic hyperplasia: examining the evidence and determining the risk. Eur Urol 2001;39(4):390- 9. https://doi.org/10.1159/000052475.
14. McConnell JD, Roehrborn CG, Bautista OM, Andriole GL Jr, Dixon CM, Kusek JW, et al. The long-term effect of doxazosin, finasteride, and combination therapy on the clinical progression of benign prostatic hyperplasia. N Engl J Med 2003;349(25):2387-98; https://doi.org/10.1056/NEJMoa030656.
15. Emberton M, Cornel EB, Bassi PF, Fourcade RO, Gómez JM, Castro R. Benign prostatic hyperplasia as a progressive disease: a guide to the risk factors and options for medical management. Int J Clin Pract 2008;62(7):1076–1086. https://doi.org/10.1111/j.1742-1241.2008.01785.x.
16. McVary KT. A review of combination therapy in patients with benign prostatic hyperplasia. Clin Ther 2007;29(3):387-98. https://doi.org/10.1016/s0149-2918(07)80077-4.
17. Аляев Ю.Г. Российские клинические рекомендации. Урология. Симптомы нижних мочевых путей. Под ред. Ю.Г. Аляева, П.В. Глыбочко, Д.Ю. Пушкаря. Геотар-Медиа, 2015;15-38 с. [Alyaev Yu.G. Russian clinical guidelines. Urology. Symptoms of the lower urinary tract. Ed. Yu.G. Alyaev, P.V. Glybochko, D.Yu. Pushkar. Geotar-Media 2015;15-38 р. (In Russian)].
18. Gravas S, Cornu JN, Gacci M, Gratzke C, Herrmann TRW., Mamoulakis C, et al. European association of Urology. Guidlines on the management of male lower urinary tract symptoms (LUTS), including bening prostatic obstruction. UPDATE MARCH 2022. URL: www.uroweb.org.
19. Lerner LB, McVary KT, Barry MJ, Bixler BR, Dahm P, Das AK, et al. Management of Lower Urinary Tract Symptoms Attributed to Benign Prostatic Hyperplasia: AUA GUIDELINE PART I-Initial Work-up and Medical Management. J Urol 2021;206(4):806-17. https://doi.org/10.1097/JU.0000000000002183.
20. Винаров А.З. Медикаментозное лечение больных гиперплазией предстательной железы: автореф. дис. д.м.н. М., 1999;40 c. [Vinarov A.Z. Drug treatment of patients with prostatic hyperplasia. Dr. Med. Sci [thesis] M., 1999;40 p.]. URL: https://viewer.rsl.ru/ru/ rsl01000254417?page=39&rotate=0&theme=white.
21. Спивак Л.Г. Медикаментозная профилактика возникновения, прогрессирования и развития осложнений гиперплазии предстательной железы: автореф. дис. д.м.н. М., 2019; 40 с. [Spivak L.G. Drug prevention of the occurrence, progression and development of complications of prostatic hyperplasia. Dr. Med. Sci. [thesis] M., 2019; 40 p. (In Russian)]. URL: ttps://www.dissercat.com/content/medikamentoznaya-profilaktika-vozniknoveniyaprogressirovaniya-i-razvitiya-oslozhnenii-giper.
22. Корнеев И.А. Российский опыт применения суппозиториев Витапрост форте у больных с симптомами нижних мочевых путей и доброкачественной гиперплазией предстательной железы: сравнительный анализ исследований. Урология 2017;(3):138- 44. [Korneev I.A. Russian experience with Vitaprost forte suppositories in patients with lower urinary tract symptoms and benign prostatic hyperplasia: comparative analysis of studies. Urologiya = Urologiia 2017;(3):138-44. (In Russian)].
23. Spivak L, Morozov A, Shpikina A, Enikeev D, Rapoport L. Postoperative medical treatment of lower urinary tract symptoms after benign prostatic hyperplasia surgery. Are we underestimating the problem? Curr Opin Urol 2021;31(5):451-5. https://doi.org/10.1097/MOU.0000000000000912.
24. Ергаков Д.В., Мартов А.Г., Аслиев К.А. Клиническое использование цитомединов у пациентов с заболеваниями предстательной железы. Экспериментальная и клиническая урология 2021;14(3):136-140; [D.V. Ergakov, A.G. Martov, K.A. Asliev. Clinical use of cytomedin in patients with prostate diseases. Eksperimental'naya i klinicheskaya urologiya = Experimental and Clinical Urology 2021;14(3):136-140]. https://doi.org/10.29188/2222- 8543-2021-14-3-136-140.
25. Haghpanah A, Masjedi F, Salehipour M, Hosseinpour A, Roozbeh J, Dehghani A. Is COVID-19 a risk factor for progression of benign prostatic hyperplasia and exacerbation of its related symptoms?: a systematic review. Prostate Cancer Prostatic Dis 2022;25(1):27-38. https://doi.org/10.1038/s41391-021-00388-3.
26. Nabeeh H, Ibrahim A, Taha D-E,Talaat M, Abdelbaky TM. Impact of COVID-19 pandemic onlower urinary tract symptoms in patients with benign prostatic hyperplasia and predictors of urine retention in such patients. Low Urin Tract Symptoms 2022;14(1):41-6. https://doi.org/10.1111/luts.12407.
27. Ткачук В.Н., Ткачук И.Н., Боровец С.Ю. Результаты 12-летнего исследования эффективности витапроста у больных хроническим простатитом. Урологические ведомости 2016;6(4):5-9. https://doi.org/10.17816/uroved645-9. [Tkachuk V.N., Tkachuk I.N., Borovets S.Yu. The results of 12-year study of the efficacy of Vitaprostin patients with chronic prostatitis. Urologicheskie vedomosti = Urology reports 2016;6(4):5-9. (In Russian)].







