ВВЕДЕНИЕ
Нарушение мочеиспускания является распространенной проблемой, и возможными причинами данных нарушений являются стриктуры уретры и стенозы шейки мочевого пузыря. Существующие методы лечения не всегда обеспечивают желаемый результат. В связи с этим ведется разработка новых методов лечения данных заболеваний. Одним из таких методов является установка уретрального стента. Впервые данный метод был применен более 30 лет назад. В настоящее время отсутствуют четкие рекомендации относительно установки стентов и продолжительности их использования. Применение этого метода привлекательно простотой установки, однако из-за высокого риска осложнений, достигающего 49%, его использование ограничено [1]. В настоящее время фирмы производители предлагают различные модели стентов, различающееся по конструкции и материалам, из которых они сделаны [2].
Согласно литературным данным, одной из самых распространенных причин стриктуры или стеноза уретры является ятрогенная, которая может встречаться в 34% случаев [3, 4]. В данную категорию попадают стенозы цистоуретроанастомоза (СЦУА) после радикальных простатэктомий по поводу рака предстательной железы (РПЖ), который входит в число самых распространенных злокачественных опухолей. В структуре онкологической заболеваемости и смертности РПЖ занимает соответственно 2-e и 6-e места среди мужского населения [5]. Радикальная простатэктомия является показанием для лечения пациентов на стадии T1-T3aN0M0 [6]. Однако после хирургических методов лечения у 1-8% пациентов возникает СЦУА [7]. Несмотря на постоянное совершенствование методик наложения цистоуретроанастомоза при радикальной простатэктомии, данное осложнение может возникнуть в течение первых 2 лет после операции [8]. Анализ литературных данных показал, что первой линией лечения СЦУА является внутренняя оптическая уретротомия (ВОУТ). При данном методе лечения степень успеха варьирует от 0 до 90% [9-11]. Для улучшения результатов лечения СЦУА было предложена установка уретральных стентов в зону цистоуретроанастомоза после ВОУТ, но и после этого результаты лечения оставались также скромны и составляли 4760% [12-14].
Хирургические реконструкции СЦУА могут быть осуществлены трансперинеально, позадилонно или абдоменоперинеально. У каждого хирургического способа есть свои отрицательные стороны, при позадилонном доступе отмечается трудность доступа из-за выраженного фиброза в позадилонном пространстве, что затрудняет визуализацию и приводит к формированию короткой культи уретры. Преимуществом этого доступа является возможность сохранить поперечнополосатый сфинктер. Степень успеха при этом доступе составила 60%, а впервые возникшее недержание мочи – около 30% [15]. Абдоменоперинеальный доступ позволяет восстановить проходимость мочеиспускательного канала в 83% [16]. Наиболее широко используется промежностный доступ ввиду его малоинвазивности и возможности широко мобилизовать уретру. Эффективность данной операции составляет 67-91%. Отрицательной стороной данного доступа является повреждение поперечнополосатого сфинктера мочеиспускательного канала, ведущее к тотальному недержанию мочи, что может потребовать имплантации искусственного мочевого сфинктера [17, 18].
Стеноз шейки мочевого пузыря требует несколько других подходов. Для его лечения применяются Y-, V-, T-образные реконструкции шейки мочевого пузыря с хорошими функциональными результатами [19]. В последнее время все чаще используется буккальный лоскут для реконструкции уретры. M.A. Avallone и соавт. предложили свой метод робот-ассистированной субтригональной буккальной пластики шейки мочевого пузыря при ее стенозе [20]. И.Э. Мамаев и соавт. сообщили об успешном лечении стеноза шейки мочевого пузыря путем трансуретрального удаления рубцовой ткани в области шейки с последующей фиксацией буккального лоскута внебрюшинным лапароскопическим доступом после раскрытия простатического отдела уретры на сформированную площадку [21].
Несмотря на существующие методы, мы предложили новый способ лечения стеноза шейки мочевого пузыря. Сущностью метода является трансуретральное рассечение стеноза шейки мочевого пузыря с последующей фиксацией буккального лоскута с помощью нитинолового уретрального стента.
КЛИНИЧЕСКИЕ СЛУЧАИ
В урологическом отделении ГБУЗ «Волгоградская областная клиническая больница №1» с 2021 по 2022 года проходили лечение 3 пациента с СЦУА, которым ранее была выполнена лапароскопическая простатэктомия по поводу рака предстательной железы. Пациенты были в возрасте 52, 66 и 76 лет. При предварительном обследовании у пациентов не был выявлен рецидив злокачественного новообразования. Через 5-7 месяцев после перенесенной операции пациенты отметили затрудненное мочеиспускание, и при дальнейшем обследовании у них выявлен СЦУА. При уретрографии нарушения проходимости в пенильном и бульбозном отделах не выявлено, в зоне цистоуретроанастомоза визуализировалось конусовидное сужение от 1 до 1,5 см с симптомом «фонтанчика». Все пациенты первым этапом подверглись ВОУТ холодным ножом с последующей катетеризаций мочевого пузыря силиконовым катетером на 5 суток. После его удаления отмечалось восстановление мочеиспускания. Но в течение последующих 3-5 месяцев у них возникал рецидив СЦУА с явлениями острой задержки мочи, по поводу чего им всем была наложена цистостома. Через 6 месяцев после проведения ВОУТ пациентам выполнена повторная ВОУТ холодным ножом с фиксацией буккального лоскута в шейке мочевого пузыря простатическим нитиноловым стентом.
Операция ВОУТ с фиксацией буккального лоскута в шейке мочевого пузыря простатическим нитиноловым стентом
Выполнение данной операции проводилось под двойным визуальным контролем со стороны мочеиспускательного канала и мочевого пузыря через цистостомический свищ.
Первым этапом при уретроскопии осматривалась уретра до зоны стеноза-облитерации. Затем по цистостомическому ходу в полость мочевого пузыря устанавливался буж Амплац для нефростомии № 30 Ch, а по нему проводили кожух Амплац. Полость мочевого пузыря осматривалась с помощью стандартного нефроскопа №26 Ch. Во всех 3 случаях отмечалась полная облитерация. Зону облитерации рассекали на свет. Для этого выключали освещение резектоскопа со стороны уретры, и в самом тонком месте зоны облитерации визуализировалось светлое пятно. Под двойным визуальным контролем со стороны мочевого пузыря и со стороны уретры выполняли рассечение рубцовой ткани прямым ножом уретротомом до нужного диаметра и появления признаков незначительного кровотечения (рис. 1). Уретротом извлекали. Далее в уретру вводили операционный цистоуретроскоп. Измеряли протяженность стенозаоблитерации и по рабочему каналу проводили систему для доставки нитинолового стента. Нитиноловый стент через цистостомический свищ по кожуху Амплац выводили на переднюю брюшную стенку. Выполняли стандартный забор буккального лоскута нужного размера и подготавливали его к трансплантации. Уретральный стент раскрывали и к нему фиксировали буккальный лоскут по окружности (рис. 2).
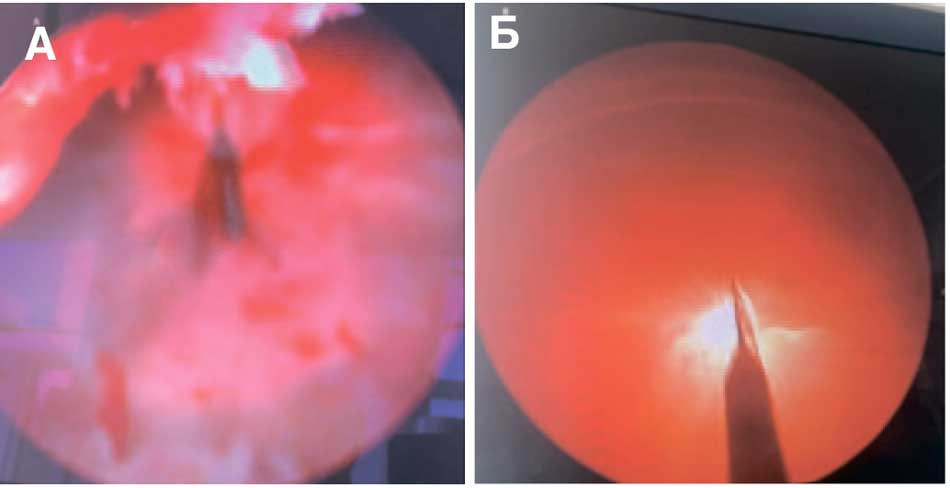
Рис. 1. Внутренняя оптическая уретротомия: А – вид со стороны мочевого пузыря; В – вид со стороны уретры.
Fig. 1. Direct visual optical urethrotomy: A – view from the bladder; B – view from the urethra
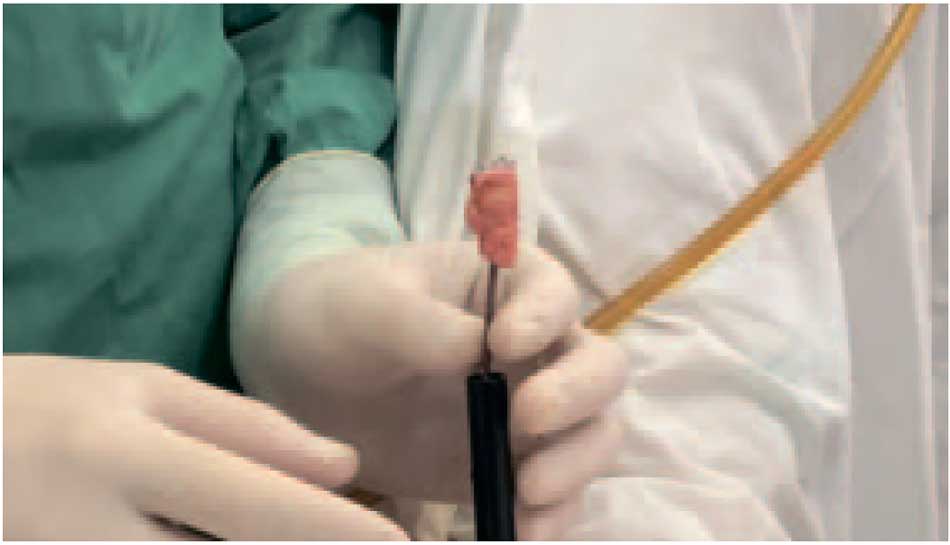
Рис. 2. Фиксация буккального лоскута по окружности уретрального стента
Fig. 2. Fixing the buccal graft surrounding the urethral stent
Затем стент с лоскутом доставляли к шейке, позиционировали на месте ложа и раскрывали стент. Контроль установки стента выполняли как со стороны уретры, так и со стороны мочевого пузыря.
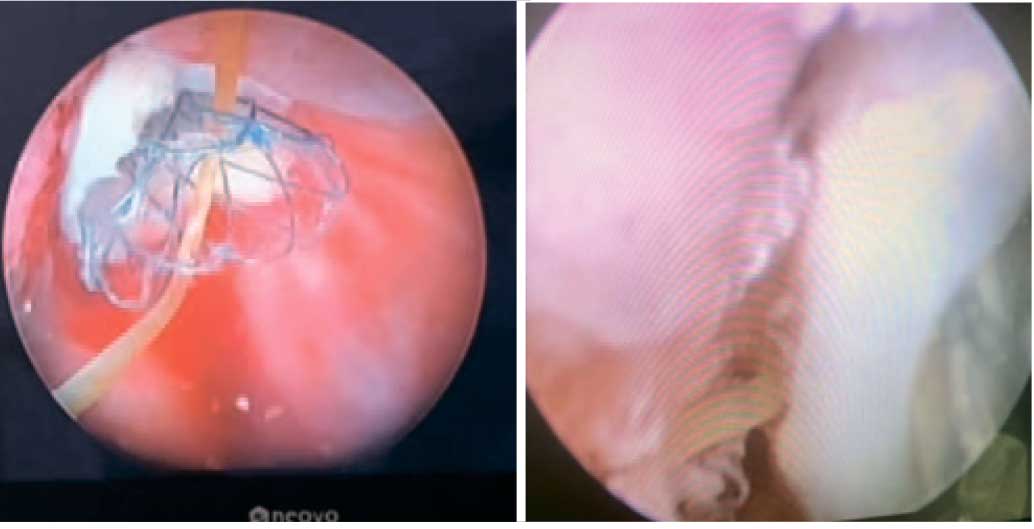
Рис. 3. Размещение уретрального стента с буккальным лоскутом в шейке мочевого пузыря
Fig. 3. Placement the urethral stent with buccal graft in the bladder neck
Стент устанавливали таким образом, чтобы пузырный конец стента выступал в просвет мочевого пузыря не более 2-3 мм для профилактики последующей миграции (рис. 3).
Для профилактики миграции стента использовали методику П.С. Кызласова. Для этого осуществляли промежностный доступ к уретре, затем ее выделяли и под оптическим визуальным контролем фиксировали стент к уретре полигликолидной нитью (ПГА) [22]. После восстановления мочеиспускания цистостому закрывали.
Результаты операции
У одного больного цистоуретроскоп с системой доставки и нефроскоп удалили и восстановили цистостому. Длительность стентирования в этом случае составила 2 месяца из-за плохой переносимости и наличия болевого синдрома (рис. 4). У двух других больных стент извлекали с помощью цистоскопа через 3 месяца.
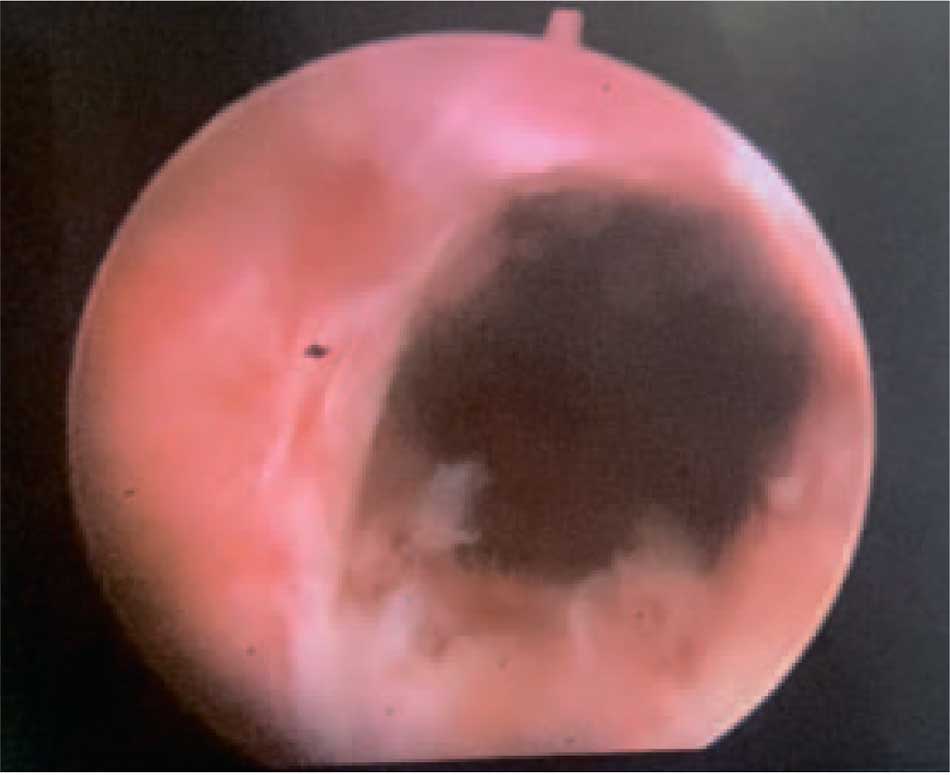
Рис. 4. Вид шейки мочевого пузыря через 2 месяца после установки уретрального стента
Fig.4. The view of bladder neck after 2 months after urethral stent placement
После восстановления мочеиспускания цистостому закрывали. При контрольной цистоскопии через 1,5 года определяется широкая шейка мочевого пузыря (рис. 5).
В послеоперационном периоде пациенты предъявляли жалобы на чувство инородного тела в промежности. В 2-х случаях после установки стента отмечались признаки легкой инконтиненции, что требовало использования 2-3 урологических прокладок в день. У одного пациента через 2 месяца, а у другого через 3 месяца отметили появление болевого синдрома в промежности, что потребовало выполнения уретроцистоскопии, где отмечались признаки незначительной инкрустации стента, что потребовало их удаления. После удаления стентов признаки недержания мочи исчезли. В одном случае у пациента уретральный стент не вызывал дискомфорта. Стент удален через 3 месяца.
Рис. 5. Вид шейки мочевого пузыря через 1,5 года после операции
Fig. 5. The view of bladder neck after 1.5 years after placement urethral stent
После удаления стента у всех пациентов восстановилось самостоятельное мочеиспускание. Цистостома закрыта. При контрольном обследовании через 6 месяцев после удаления стента все пациенты заполняли опросник IPSS (International Prostate Symptom Score – Международная система суммарной оценки симптомов болезней предстательной железы в баллах), средний балл составил 6±1,5 балла; по опроснику, QoL (Quality of life – опросник качества жизни) средний бал был равен 2, средняя скорость мочеиспускания составила 17±3,2 мл/с. В одном случае оценили результат через 1,5 года: при заполнении опросника IPSS сумма баллов равна 7, QoL – 2 балла.
ОБСУЖДЕНИЕ
Радикальная простатэктомия является ведущим методом лечения рака предстательной железы. При данном методе лечения возникают два социально значимых осложнения: недержание мочи, ведущее к постоянному использованию адсорбирующего белья, или СЦУА, которое чаще всего приводит к отсутствию самостоятельного мочеиспускания и установке цистостомы, что, в свою очередь, значительно увеличивает риски инфекционных осложнений. Поэтому восстановление самостоятельного мочеиспускания является важной задачей. При использовании эндолюминальных методик лечения очень часто возникают рецидивы, достигающие, по разным литературным данным, от 0 до 90% [9, 11, 13]. Открытые оперативные вмешательства, в частности, при позадилонном доступе очень травматичны и затруднительны в связи с развитием массивного фиброзного процесса в ретциевом пространстве после предыдущего оперативного вмешательства [15]. При промежностном доступе возникает высокий риск недержания мочи [17, 18]. Имеющиеся единичные публикации с фиксацией буккального лоскута в шейке мочевого пузыря говорят о высокой эффективности данного метода лечения. Однако фиксация лоскута производится с помощью лапароскопической или робот-ассистирований техники, что иногда бывает затруднительно сделать [20, 21].
Предложенный нами способ сочетает малоинвазивность эндолюминальной техники и возможную высокую эффективность лапароскопической техники, что позволяет избежать вскрытия просвета мочевого пузыря. Отрицательной стороной данной методики является использование инородного тела в просвете мочевыводящих путей, что способствует поддержанию инфекционного процесса и возникновению инкрустации стента. Другим недостатком данной методики является невозможность контролировать степень компрессии буккального лоскута стентом для оптимального его приживления, чтобы не вызвать избыточного давления или, наоборот, отсутствия должного давления на лоскут, что может привести к его смещению и невозможности питания из подлежащих тканей. Поэтому необходимо выполнять контролируемую инцизию шейки мочевого пузыря, чтобы диаметр шейки мочевого пузыря был сопоставим с диаметром уретрального стента. Для профилактики смещения стента необходима фиксация стента в уретре путем его прошивания под оптическим контролем или с помощью специальных приспособлений. Ранее удаление стента через 2-3 месяца после его имплантации позволит избежать серьезных осложнений, таких как инкрустация.
ВЫВОДЫ
Первый опыт установки стента с использованием буккального лоскута при СЦУА дает обнадеживающие результаты и повод для проведения дальнейших исследований. Данная методика проста в использовании и является малотравматичной, что может позволить широко использовать ее в рутинной практике.
ЛИТЕРАТУРА
- Sedigh O, Dalmasso E, Gobbo A, Dashti MH, Bagheri F, Shamsodini A, et al. Feasibility and outcomes of temporary bulbar urethral stent placement after internal urethrotomy in the largest multicenter series. Eur Urol 2023;84(3):313-20. https://doi.org/10.1016/j.eururo.2023.05.019.
- Кызласов П.С., Мартов А.Г., Мустафаев А.Т., Казанцев Д.В., Островский Д.В. Применение уретральных стентов при стриктурах уретры. Урология 2022;(4):109-13. [Kyzlasov P.S., Martov A.G., Mustafayev A.T., Kazantsev D.V., Ostrovsky D.V. Use of urethral stents for urethral strictures. Urologiia = Urologiia 2022;(4):109-113. (In Russian)]. https://doi.org/10.18565/urology.2022.4.109-113.
- Fenton AS, Morey AF, Aviles R, Garcia CR. Anterior urethral strictures: etiology and characteristics. J Urol 2005;65(6):1055-8. https://doi.org/10.1016/j.urology.2004.12.018.
- Abdeen BM, Badreldin AM. Urethral Strictures. In: StatPearls. Treasure Island (FL): StatPearls Publishing; 2021.
- Сомов А.Н., Суслин С.А. Рак предстательной железы. Эпидемиология, факторы риска и раннее выявление. Профилактическая медицина 2020;23(3):149-55. [Somov A.N., Suslin S.A. Prostate cancer. Epidemiology, risk factors and early detection. Profilakticheskaya Meditsina = Preventive medicine 2020;23(3):149-155. (In Russian)]. https://doi.org/10.17116/profmed202023031149.
- Каприн А.Д., Алексеев Б.Я., Матвеев В.Б., Пушкарь Д.Ю., Говоров А.В., Горбань Н.А. и соавт. Рак предстательной железы. Клинические рекомендации. Современная Онкология 2021;23(2):211-47. [Kaprin A.D., Alekseev B.YA., Matveev V.B., Pushkar' D.YU., Govorov A.V., Gorban' N.A., et al. Prostate cancer. Clinical recommendations. Sovremennaya Onkologiya = Modern Oncology 2021;23(2):211-47. (In Russian)]. https://doi.org/10.26442/18151434.2021.2.200959.
- Martins FE, Holm HV, Lumen N. Devastated bladder outlet in pelvic cancer s urvivors: issues on surgical reconstruction and quality of life. J Clin Med 2021;10(21):4920. https://doi.org/10.3390/jcm10214920.
- Herschorn S, Elliott S, Coburn M, Wessells H, Zinman L. SIU/ICUD Consultation on urethral strictures: posterior urethral stenosis after treatment of prostate cancer. Urology 2014;83(3 Suppl):S59-70. https://doi.org/10.1016/j.urology.2013.08.036.
- Borborogly PG, Sands JP, Roberts JL, Amling CL. Risk factors for vesicourethral anastomotic stricture after radical prostatectomy. Urology 2000;56(1):96-100. https://doi.org/10.1016/s0090-4295(00)00556-2.
- Surya BV, Provet J, Johanson KE, Browm J. Anastomotic strictures following radical prostatectomy: risk factors and management. J Urol 1990;143(4):755-8. https://doi.org/10.1016/s0022-5347(17)40082-6.
- Dalkin BL. Endoscopic evaluation and treatment of anastomotic strictures after radical retropubic prostatectomy. J Urol 1996;155(1):206-8.
- Erickson BA, McAninch JW, Eisenberg ML, Washington SL, Breyer BN. Management for prostate cancer treatment related posterior urethral and bladder neck stenosis with stents. J Urol 2011;185(1):198-201. https://doi.org/10.1016/j.juro.2010.09.020.
- Sertcelik MN, Bozkurt IH, Yalcinkaya F, Zengin K. Long-term results of permanent urethral stent Memotherm implantation in the management of recurrent bulbar urethral stenosis. BJU Int 2011;108(11):1839-42. https://doi.org/10.1111/j.1464-410X.2011.10230.x.
- Chapple C, Andrich D, Atala A, Barbagli G, Cavalcanti A, Kulkarni S, et al. SIU/ICUD Consultation on urethral strictures: the management of anterior urethral stricture disease using substitution urethroplasty. Urology 2014;83(3 Suppl):S31. https://doi.org/10.1016/j.urology.2013.09.012.
- Pfalzgraf D, Bouke M, Isbarn H, Reiss CP, Meyer-Moldenhauer W, Dahlem R, et al. Open retropubic reanastomosis for highly recurrent and complex bladder neck stenosis. J Urol 2011;186(5):1944-7. https://doi.org/10.1016/j.juro.2011.07.040.
- Theodorus C, Katsifotis C, Stoumaras P, Moutzouris G, Katsoulis A, Floratos D. Abdomino-perineal repair of recurrent and complex bladder neck-prostatic urethra contractures. Eur Urol 2000;38(6):734-40. https://doi.org/10.1159/000020371.
- Mundy AR, Andrich DE. Posterior urethral complications of the treatment of prostate cancer. BJU Int 2012;110(3):304-25. https://doi.org/10.1111/j.1464-410X.2011.10864.x.
- Schuettfort VM, Dahlem R, Kluth L, Pfalzgraf D, Rosenbaum C, Ludwig T, et al. Transperineal reanastomosis for treatment of highly recurrent anastomotic strictures after radical retropubic prostatectomy: extended follow-up. World J Urol 2017;35(12):1885. https://doi.org/10.1007/s00345-017-2067-8.
- Попов С.В., Орлов И.Н., Цой А.В, Чернышева Д.Ю. Стеноз шейки мочевого пузыря после хирургического лечения пациентов с доброкачественной гиперплазией предстательной железы. Эпидемиология. Современные возможности лечения. Экспериментальная и клиническая урология 2021;14(1):100-7. [Popov S.V., Orlov I.N., Tsoi A.V, Chernysheva D.YU. Bladder neck stenosis after surgical treatment of patients with benign prostatic hyperplasia. Epidemiology. Modern treatment options. Eksperimental'naya i klinicheskaya urologiya = Experimental and clinical urology 2021;14(1):100-7 (In Russian)]. https://doi.org/10.29188/2222-8543-2021-14-1-100-107.
- Avallone MA, Quach A, Warncke J, Nikolavsky D, Flynn BJ. Robotic-assisted laparoscopic subtrigonal inlay of buccal mucosal graft for treatment of refractory bladder neck contracture. Urology 2019;130:209. https://doi.org/10.1016/j.urology.2019.02.048.
- Мамаев И.Э., Ахмедов К.К., Болотов А.Д. Котов С.В. Комбинированное использование трансуретральной резекции и буккального графта в лечении рецидивного стеноза шейки мочевого пузыря. Урология 2022;(4):63-7. [Mamaev I.E., Akhmedov K.K., Bolotov A.D., Yusufov A.G., Kotov S.V. Transurethral resection and buccal mucosal graft for the treatment of refractory bladder neck contracture. Urologiia = Urology 2022;(4):63-7. (In Russian)]. https://doi.org/10.18565/urology.2022.4.63-67.
- Кызласов П.С., Мустафаев А.Т., Островский Д.В., Мартов А.Г. Временный уретральный стент с фиксацией через промежность при стенозах задней уретры (предварительные результаты). Вестник урологии 2021;9(2):80-5. [Kyzlasov P.S., Mustafaev A.T., Ostrovsky D.V., Martov A.G. Temporary urethral stent with perineal fixation for posterior urethral stenosis (preliminary results). Vestnik urologii = Urology Herald 2021;9(2):80-5. (In Russian)]. https://doi.org/10.21886/2308-6424-2021-9-2-80-85.







