ВВЕДЕНИЕ
Рак предстательной железы (РПЖ) является всемирной проблемой. В США в 2017 г. было выявлено 161 300 новых случаев этого заболевания, от которого погибли в этом же году 26 730 пациентов, то есть приблизительно каждый шестой пациент [1,2]. Определение специфичного для предстательной железы антигена (PSA) благоприятствует ранней диагностике РПЖ и, таким образом, улучшает статистику результатов лечения [1-5], в том числе, хирургического. После значительных успехов в хирургической технике, отработанной P.C. Walsh и соавт., включающей сохранение сосудисто-нервного пучка и лучший контроль комплекса дорзальной вены полового члена, радикальная простатэктомия стала безопасной и осуществимой в исполнении большого числа онкоурологов [6]. Через два десятилетия после публикации техники P.C. Walsh и соавт. многие хирурги получили большой опыт, имея крупную когорту прооперированных пациентов [7-9]. При этом основные ранние и поздние осложнения, связанные с радикальной простатэктомией, хорошо задокументированы [5,11-13].
Нарушение целостности уретроцистоанастомоза после радикальной позадилонной простатэктомии является редким осложнением и, несомненно, драматической ситуацией, когда хирург вынужден выбирать между хирургическим вмешательством и консервативным лечением [7]. Выбор всегда спорен, так как превосходство того или иного метода лечения не подтверждено.
МАТЕРИАЛЫ И МЕТОДЫ
Была проведена ретроспективная оценка отдаленных результатов у 93 пациентов, которым по поводу РПЖ в период с января 2015 года по ноябрь 2019 год выполнена радикальная позадилонная простатэктомия в сочетании с двусторонней подвздошной лимфаденэктомией, проведенной в НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина. Наше исследование включало 4 пациентов в возрасте от 55 до 64 лет (среднее значение = 61,5 года), у которых наблюдались нарушения уретроцистоанастомоза в течение послеоперационного периода. У двух пациентов нарушение произошло из-за расхождения швов в зоне резекции и у двух – разрывы анастомоза произошли на первом и на десятом дне после удаления катетера Foley, через 13 и 23 дня после операции, соответственно.
Немедленное лечение состояло в уретроцистоскопии, связанной с введением проволочного проводника и установкой катетера Foley под контролем рентгеноскопии в 4-х случаях. Только 1 пациент был сразу катетеризирован. Затем проводилось еженедельное цистографическое исследование с удалением катетера Foley после отсутствия затека контрастного вещества, подтвержденных уретроцистограммой. Последующее наблюдение проводилось на протяжении от 6 до 120 месяцев (среднее значение – 25,2 месяца). Состояние пациентов оценивали с помощью изучение анамнеза, жалоб, особое внимание уделяли дефектам наполнения при ежемесячной уретроцистографии в течение первого семестра, двухгодичным измерением уровня ПСА сыворотки крови, томографии брюшной полости и сцинтиграфии костей ежегодно.
Из 4-х проанализированных случаев разрыва и нарушения целостности уретроцистоанастомоза после радикальной позадилонной простатэктомии, все 4 разрешились удовлетворительно.
Далее мы подробно представляем описание каждого случая:
Случай 1: Пациент К., 64-х лет, рак предстательной железы рT3аN0M0R0, сумма баллов по шкале Глисона 7 (3+4). Пациенту выполнена радикальная простатэктомия с тазовой лимфодиссекцией. Течение послеоперационного периода осложнилось дефектом уретроцистоанастомоза, подтвержденного затеком контрастного вещества при ретроградной цистографии, в связи с чем, было принято решение о более длительной экспозиции уретрального катетера. Однако на выполненой на 16-е сутки контрольной цистографии был отмечен затек контрастного вещества в паравезикальное пространство с обеих сторон, больше – справа (рис. 1). Баллон катетера, судя по изображению, располагался в паравезикальном пространстве. С целью отведения мочи пациенту на 20-е сутки после операции выполнена уретроцистоскопия, восстановление уретрального катетера. Экспозиция катетера в течение 3-х недель. Затем пациенту была выполнена контрольная цистография, при которой затека контрастного вещества за пределы мочевыводящих путей уже не было выявлено.
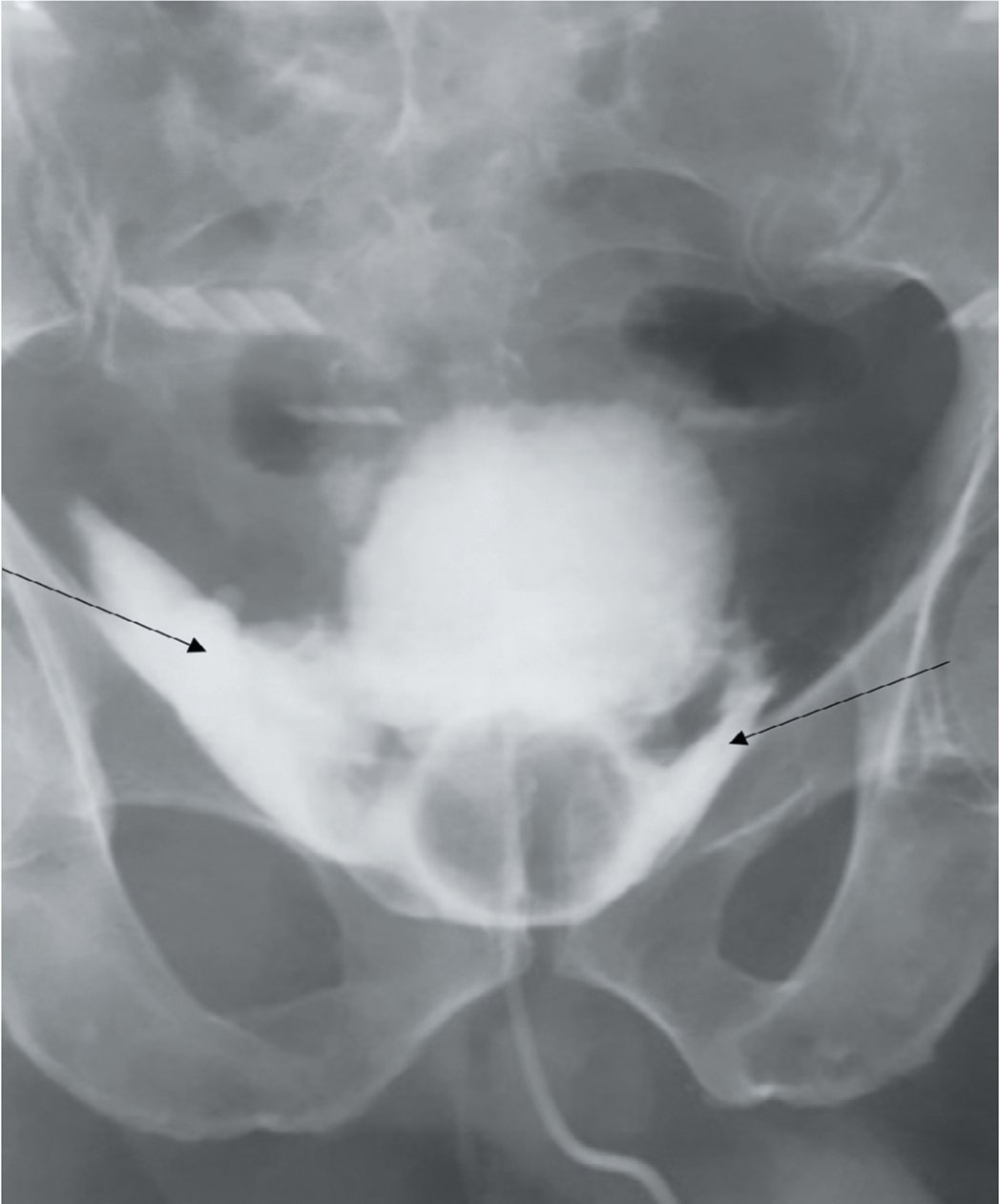
Рис. 1. Пациент К.: Ретроградная цистография на 16е сутки после операции
Fig. 1. Patient K .: Retrograde cystography on the 16th day after surgery
Явления частичного неудержания мочи элиминировались спустя 3 месяца.
Случай 2: Пациент З., 63-х лет, рак предстательной железы рT2сN0M0R0, сумма баллов по шкале Глисона 6 (3+3). Пациенту выполнена радикальная простатэктомия с тазовой лимфодиссекцией. Течение послеоперационного периода осложнилось дефектом уретроцистоанастомоза, подтвержденного затеком контрастного вещества при ретроградной цистографии, выполненной на 9-е сутки (рис.2), в связи с чем было принято решение о более длительной экспозиции уретрального катетера. Спустя 4 недели после операции выполнена контрольная цистография, при которой затека контрастного вещества за пределы мочевыводящих путей не выявлено. Уретральный катетер был удален в указанные сроки, восстановилось самостоятельное мочеиспускание. Сохранявшиеся вначале признаки частичного неудержания мочи при повышении внутрибрюшного давления элиминировались вскоре после удаления уретрального катетера.
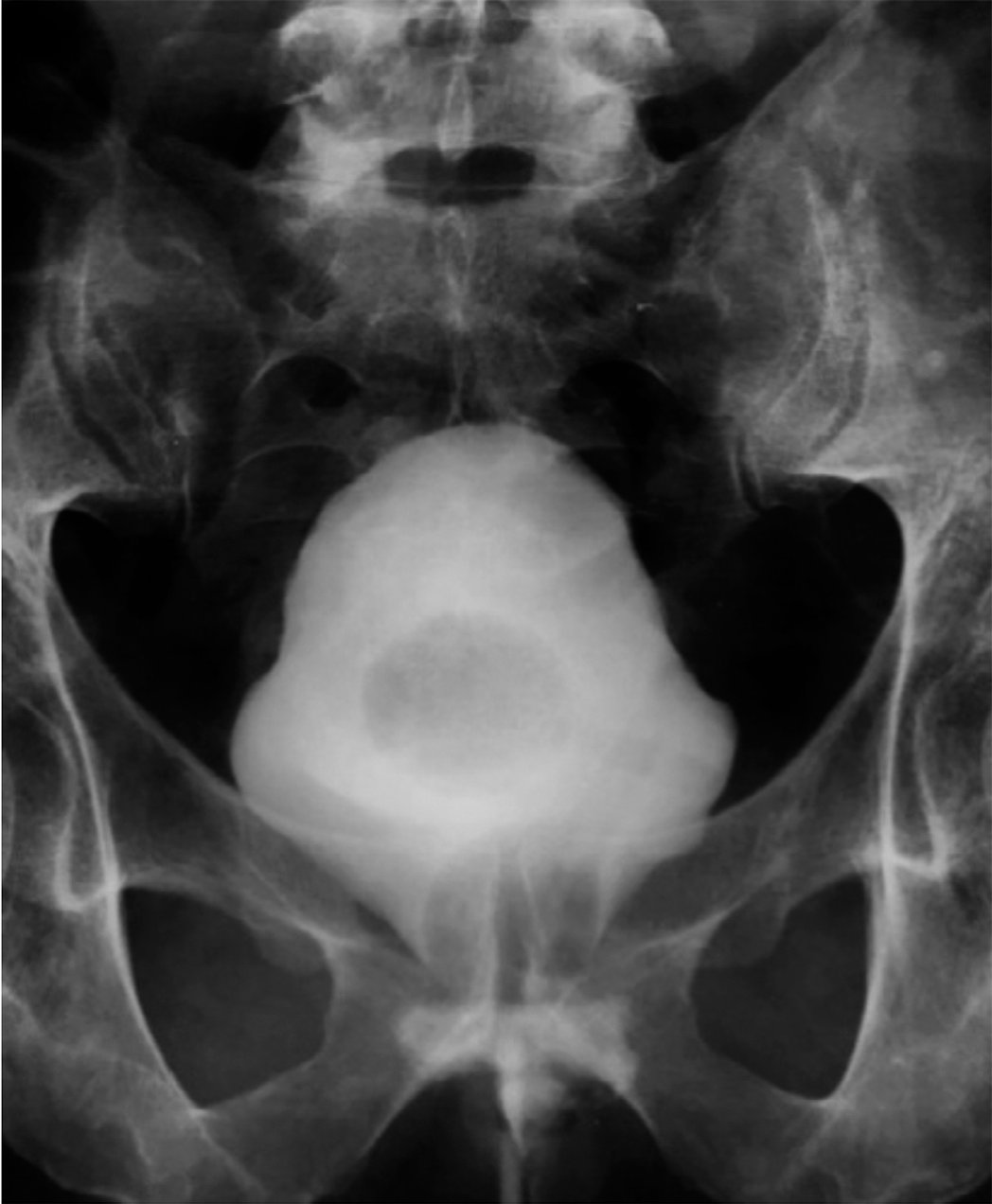
Рис. 2. Пациент З. Ретроградная цистография на 9-е сутки после радикальной простатэктомии
Fig. 2. Patient Z. Retrograde cystography on the 9-th day after radical prostatectomy
Случай 3: Пациент Г., 64-х лет, рак предстательной железы рT2bN0M0R0, сумма баллов по шкале Глисона 7 (3+4). Выполнена радикальная простатэктомия с тазовой лимфодиссекцией. Течение послеоперационного периода осложнилось дефектом уретроцистоанастомоза, подтвержденного затеком контрастного вещества при ретроградной цистографии, выполненной на 7-е сутки после операции, в связи с чем, спустя 10 дней после операции, выполнена контрольная цистография, при которой затека контрастного вещества за пределы мочевыводящих путей не выявлено (рис. 3). Уретральный катетер был удален, однако через сутки у пациента произошла острая задержка мочеиспускания, обусловленная склерозом уретроцистоанастомоза, по поводу чего, была выполнена уретроцистоскопия, восстановление уретрального катетера под оптическим контролем. Экспозиция катетера в течение 3-х недель. Имевшие место явления частичного неудержания мочи при повышении внутрибрюшного давления элиминировались вскоре после удаления уретрального катетера.
Случай 4: Пациент Д., 55 лет, рак предстательной железы рT2сN0M0R0, сумма баллов по шкале Глисона 6 (3+3). Пациенту выполнена радикальная простатэктомия с тазовой лимфодиссекцией. Течение послеоперационного периода осложнилось дефектом уретроцистоанастомоза, подтвержденного затеком контрастного вещества при ретроградной цистографии, выполненной на 10-е сутки после операции, в связи с чем, было принято решение о более длительной экспозиции уретрального катетера. Однако катетер самостоятельно отошел, по поводу чего было выполнено восстановление уретрального катетера под рентгеноскопическим контролем. Экспозиция катетера в течение 3-х недель.
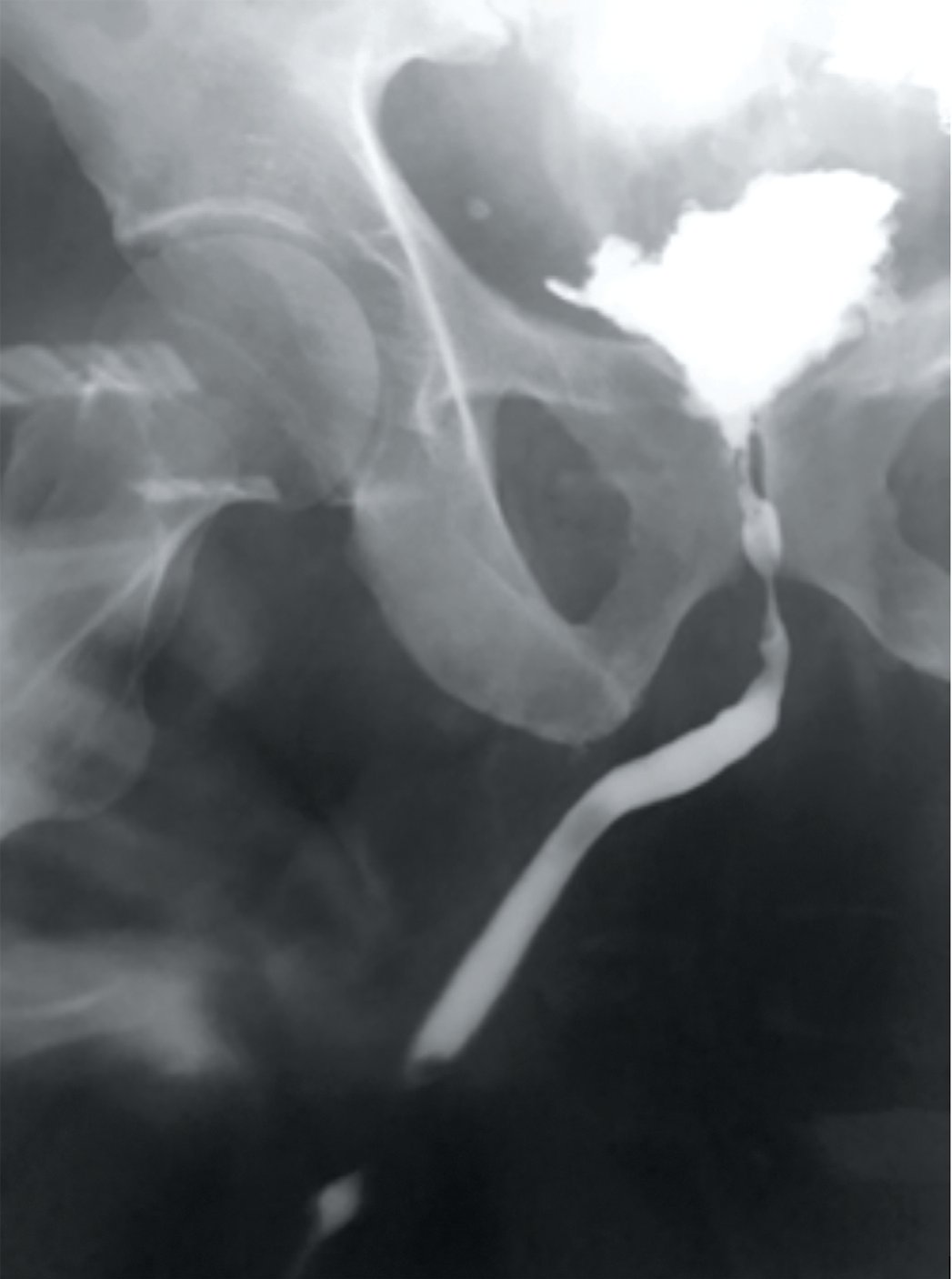
Рис. 3. Пациент Г. Уретроцистография на 10е сутки после радикальной простатэктомии
Fig. 3. Patient G. Urethrocystography on the 10th day on the 9th day after radical prostatectomy
Спустя 20 дней после операции, выполнена контрольная цистография, при которой затека контрастного вещества за пределы мочевыводящих путей не выявлено. Уретральный катетер был удален в указанные сроки, восстановилось самостоятельное мочеиспускание.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Данная работа доказывает, что консервативное ведение нарушения целостности уретроцистоанастомоза посредством установки уретрального катетера Foley было эффективным. По данным литературы частота нарушения целостности уретроцистоанастомоза составляет от 0,2% до 0,5% и наилучший способ ведения все еще является предметом обсуждения [7-9].
Наиболее распространенным послеоперационным осложнением радикальной простатэктомии являются кровотечения, частота которых уменьшается с увеличением опыта хирурга [8,11,12]. С другой стороны, частота значительных кровотечений в месте анастомоза в послеоперационный период колеблется от 0,3% до 3,2% и потребность в переливании крови очень редка [7,9,11,12,14]. Образование небольших гематом предполагает возможность консервативного лечения, однако гематомы большого объема, по данным литературы, могут вытеснять мочевой пузырь в каудальном направлении, вызывая натяжение и разрыв уретроцистоанастомоза [7,11]. В нашей серии пациентов с разрывом анастомоза, обусловленным образованием локальных гематом, не было. S.P. Hedican и P.C. Walsh исследовали 7 пациентов с разрывом уретроцистоанастомоза, возникшего после кровотечения, разделив пациентов на 2 группы. В первой группе, состоящей из 3 пациентов, было проведено консервативное лечение с длительной экспозицией уретрального катетера, в исходе у всех 3 больных развился склероз анастомоза, причем у 2 из них развилось недержание мочи. Вторая группа, подвергнутая хирургическому вмешательству по дренированию гематомы с перекладыванием анастомоза, имела лучший исход. Склероз анастомоза развился у 1 пациента и продолжительное недержание мочи – у другого [7]. О необходимости повторного вмешательства по удалению гематомы малого таза после радикальной простатэктомии указывает H. Lepor и соавт., советуя в подобных случаях перекладывание уретроцистоанастомоза [9].
J. Yang с соавт. в 2014 г. сообщили об опыте использования непрерывного шва при радикальной позадилонной простатэктомии, при этом, в их практике не было случаев разрыва везикоуретрального анастомоза [10].
Консервативное лечение может осложниться склерозом уретровезикоанастомоза, а также продолжительным недержанием мочи, с другой стороны, раннее вмешательство с сшиванием краев анастомоза повышает риск осложнений, таких как недержание мочи, эректильная дисфункция и кровотечение [7,15,16].
При разрыве уретроцистоанастомоза при перестановке уретрального катетера необходима цистоскопия с введением проволочного проводника и при введении катетера его положение должно быть подтверждено рентгеноскопией с контрастированием [10,15]. При радикальной позадилонной простатэктомии при создании уретровезикоанастомоза обычно используют шов 3-0. Уретральный катетер, как правило, удаляется на 7-10 послеоперационные сутки, однако существуют исследования, указывающие на возможность удаления катетера в более раннем периоде без нарушения заживления [14]. У нас было 2 случая острой задержки мочеиспускания после удаления катетера: на 1-й и на 10-й день после удаления катетера, без подтверждения разрыва анастамоза. Только в одном случае преждевременная смена катетера способствовала нарушению целостности анастомоза.
Мы считаем, что разрыв анастомоза не связан с опытом хирурга, учитывая возникновение такого осложнения в когортах с большим числом пациентов и не зависит от количества швов, используемых для уретроцистоанастомоза [5,7-9,13,15,17,18].
Антибиотикотерапия применялась у всех пациентов, случаев сепсиса не зафиксировано. После подтверждения стабильности клинической картины и адекватного расположения катетера, пациент выписывается из стационара для амбулаторного долечивания: прием пероральных антибиотиков и еженедельное амбулаторное обследование в объеме цистографии, что позволяет избежать чрезмерного увеличения затрат на лечение.
ВЫВОДЫ
При нарушении целостности простатического и бульбо-мембранозного отделов уретры с краниальным смещением мочевого пузыря, введение катетера через уретру позволяет выровнять края с меньшей частотой стеноза, с последующим опусканием мочевого пузыря в его анатомическое положение [15]. В связи с этими данными проведение цистотомии у данных пациентов нецелесообразно, а продолжительная экспозиция дренажа помогает избежать повторного оперативного вмешательства.
ЛИТЕРАТУРА
- Aldoukhi AH, Roberts WW, Hall TL, Ghani KR. Holmium laser lithotripsy in the new stone age: dust or bust? Front Surg 2017;4:57. doi: 10.3389/fsurg.2017.00057
- Gross AJ, Netsch C, Knipper S, Hölzel J, Bach T. Complications and early postoperative outcome in 1080 patients after thulium vapoenucleation of the prostate: results at a single institution. Eur Urol 2013;63(5):859-67. doi: 10.1016/j.eururo.2012.11.048.
- Kronenberg P, Traxer O. Update on lasers in urology 2014: current assessment on holmium:yttrium-aluminum-garnet (Ho:YAG) laser lithotripter settings and laser fibers. World J Urol 2015;33(4):463-9. doi: 10.1007/s00345-014-1395-1
- Ketan PV, Prashant HS. Thulium laser enucleation of the prostate is a safe and a highly effective modality for the treatment of benign prostatic hyperplasia - Our experience of 236 patients. Urol Ann 2016;8(1):76-80. doi: 10.4103/0974-7796.171494.
- Eton DT, Lepore SJ, Helgeson VS. Early quality of life in patients with localized prostate carcinoma: an examination of treatment-related, demographic, and sychosocial factors. Cancer 2001;92(6):1451-9.
- Berry MJ, Albertsen PC, Bagshaw MA, Blute ML, Cox R, Middleton RG, et al. Outcomes of men with clinically nonmetastatic prostate carcinoma managed with radical prostatectomy, external beam radiotherapy, or expectant management. a retrospective analysis. Cancer 2001;91(12):2302-14. doi: 10.1002/1097-0142(20010615)91:123.3.co;2-g
- Jacobsen SJ, Kausis SV, Bergstralh EJ, Oesterling JE, Orth, D, Klee GG, et al. Incidence of prostate cancer diagnosis in the eras before and after serum prostate-specific antigen testing. JAMA 1995;274(18):1445-9.
- Epstein JI, Walsh PC, Carter HB. Dedifferentiation of prostate cancer grade with time in men followed expectantly for stage T1c disease. J Urol 2001;166(5):1688-91
- Dillioglugil O, Leibman D, Leibman NS, Kattan MW, Rosas AL, Scardino PT. Risk factors for complication and morbidity after radical retropubic prostatectomy. J Urol 1997;157(5):1760-7
- Yang J, Shao PF, Lv Q, Song NH, Li J, Zhang W, et al. Continuous suture of a single absorbable suture: A new simplified vesicourethral anastomosis technique in laparoscopic radical prostatectomy. Int Surg 2014 Sep-Oct; 99(5): 656-661. doi: 10.9738/INTSURG-D-13-00124.1
- Walsh PC, Partin AW, Epstein JI. Cancer control and quality of life following anatomical radical retropubic prostatectomy. Results at 10 years. J Urol 1984;152(5Pt2):1831-6. doi: 10.1016/s0022-5347(17)32396-0
- Hedican SP, Walsh PC. Postoperative bleeding following radical retropubic prostatectomy. J Urol 1994; 152:1181-3. doi: 10.1016/s0022-5347(17)32534-x
- Catalona WJ, Carvalhal GF, Mager DE, Smith DS. Potency, continence and complication rates in 1,870 consecutive radical retropubic prostatectomies. J Urol 1999;162(2):433-8
- Lepor H, Nieder AM, Ferrandino MN. Intraoperative and postoperative complications of radical retropubic prostatectomy in a consecutive series of 1000 cases. J Urol 2001;166(5):1729-33.
- Shekarriz B, Upadhyay J, Wood DP. Intraoperative, perioperative, and long-term complications of radical prostatectomy. Urol Clin North Am 2001;28(3):639-53. doi:10.1016/s0094-0143(05)70168-3
- Oefelein MG, Conlangelo LA, Rademaker AW, McVary KT. Intraoperative blood loss and prognosis in prostate cancer patients undergoing radical retropubic prostatectomy. J Urol 1995;154(2 Pt 1):442-7. doi: 10.1097/00005392-199508000-00029
- Lu-Yao GL, Albertsen P, Warren J, Yao SL. Effect of age and surgical approach on complications and short-term mortality after radical prostatectomy. A populationbased study. Urology 1999; 54(2):301-7
- Heinzer H, Graefen M, Noldus J, Hammerer P, Huland H. Early complication of anatomical radical prostatectomy: Lessons from a single-center experience. Urol Int 1997;59(1):30-3. doi: 10.1159/000283013
- Guillonneau B, Rozet F, Cathelineau X, Lay F, Barret E, Doublet JD, et al. Perioperative complications of laparoscopic radical prostatectomy: the Montsouris 3-years experience. J Urol 2002;167(1):51-6.
- Fisher RE, Koch MO. Recognition and management of delayed disruption v esicourethral anastomosis in radical prostatectomy. J Urol 1992;147(6):1579-81. doi: 10.1016/s0022-5347(17)37632-2
- Kotkin L, Koch MO. Impotence and incontinence after immediate realignment of posterior urethral trauma: result of injury or management? J Urol 1996;155(5):1600-3.
- Igel TC, Barrett DM, Rife CC. Comparison of techniques for vesicourethral anastomosis: simple direct modified Vest traction sutures. Urology 1988;31(6):474-7. doi: 10.1016/0090-4295(88)90210-5
- Petroski RA, Thrasher JB, Hansberry KL. New use of Foley catheter for precise vesicourethral anastomosis during radical retropubic prostatectomy. J Urol 1996;155(4):1376-7.







