ВВЕДЕНИЕ
Рак предстательной железы (РПЖ) является одним из наиболее распространенных онкологических заболеваний у мужчин, его диагностика и лечение представляют собой сложную проблему современной медицины и практического здравоохранения [1-3]. Радикальная простатэктомия (РПЭ) – основной метод лечения клинически локализованного РПЖ с ожидаемой продолжительностью жизни более 10 лет [4-7]. Стремление сохранить качество жизни у пациентов после РПЭ сегодня стало неотъемлемой частью подхода к лечению больных данной группы [4]. Особое место в этом случае наряду с проблемами удержания мочи занимает состояние эректильной дисфункции (ЭД) [4]. И если с недержанием мочи удалось достичь положительных результатов с помощью усовершенствования хирургических навыков, то ЭД остается наиболее частым осложнением и до сих пор представляет главную проблему как для пациента, так и для врача [4].
ЭД – это неспособность достижения и поддержания эрекции, достаточной для обеспечения сексуальной удовлетворенности у мужчин. ЭД может оказывать пагубное воздействие как на физическое здоровье, так и на психосоциальное состояние и значительно ухудшать качество жизни пациентов и их партнеров [8]. Риск возникновения ЭД в послеоперационном периоде у пациентов, перенесших РПЭ по данным различных авторов, колеблется от 14% до 89% [6, 9, 10].
ПАТОГЕНЕЗ ЭРЕКТИЛЬНОЙ ДИСФУНКЦИИ ПОСЛЕ РАДИКАЛЬНОЙ ПРОСТАТЭКТОМИИ
По мнению большинства авторов, патогенез ЭД после нервосберегающей радикальной простатэктомии (НС-РПЭ) носит сочетанный характер: нейрогенный и сосудистый. Нейрогенный генез связан с повреждением тазового сплетения и кавернозных нервов в процессе операции. Также возможно частичное повреждение нервных образований в результате манипуляций вблизи от них. Даже тщательно выполненная диссекция сосудистонервного пучка с использованием прецизионной техники вызывает нейропраксию кавернозных нервов [6, 8, 9]. Нейропраксия — это наиболее легкая степень травмы сосудисто-нервного пучка, при которой нарушается проводимость, но анатомическая целостность сохраняется [3]. Отсутствие проведения импульсов по кавернозным нервам вызывает нарушение образования фермента синтазы оксида азота (NOS), что значительно снижает выработку эндотелиального оксида азота (NO) [11]. В результате за счет дефицита NO происходит потеря спонтанных и ночных эрекций, что приводит к гипоксии кавернозной ткани.
Развитие артериальной ЭД у больных после РПЭ связывают с травматизацией добавочных пудендальных артерий, которые у некоторых мужчин могут являться основным источником кровоснабжения. K. Hoyland и соавт. приводят данные что у 59% пациентов после НС-РПЭ возникает артериальная недостаточность, а у 26% – происходит венозная утечка из-за нарушения вено-окклюзивного механизма [9]. Кавернозная гипоксия ингибирует выработку простагландина Е1 (PGE-1), за счет этого происходит экспрессия трансформирующего фактора роста, бета-1 (TGF-β1), эндотелина-1 (ET-1), фактора роста нервов (NGF), фактора, индуцируемого гипоксией-1α (HIF-1α). TGF-β1 вызывает накопление коллагена I и III типа, которые снижают функциональную способность кавернозной ткани [9].
За счет стресс-реакций клеточных пулов в кавернозной ткани возникают морфологические изменения гладких миоцитов, фибробластов, эндотелиальных структур, с нарушением монослоя [3]. Таким образом, нейрогенный и сосудистый генез после НС-РПЭ вызывает запуск фиброгенной и цитокиновой продукции, которая приводит к ремоделированию кавернозной ткани. Ремоделирование кавернозной ткани – это патологическое состояние, сочетающее в себе эндотелиальную дисфункцию, дегенерацию гладкомышечных волокон, апоптоз и кавернозный фиброз [3].
Переизбыток образования фиброзной ткани ведет к потере эластичности пещеристых тел и к нарушению сдавления подоболочечных венул, в результате возникает вено-окклюзивная дисфункция [10]. Снижение пенильного артериального кровотока и усиление венозного оттока из-за повреждения вено-окклюзивного механизма приводят к снижению PO2 в кавернозной ткани, и, как следствие, снова происходит экспрессия всех факторов цитокиновой и фиброгенной продукции, то есть возникает «порочный круг» (рис. 1).
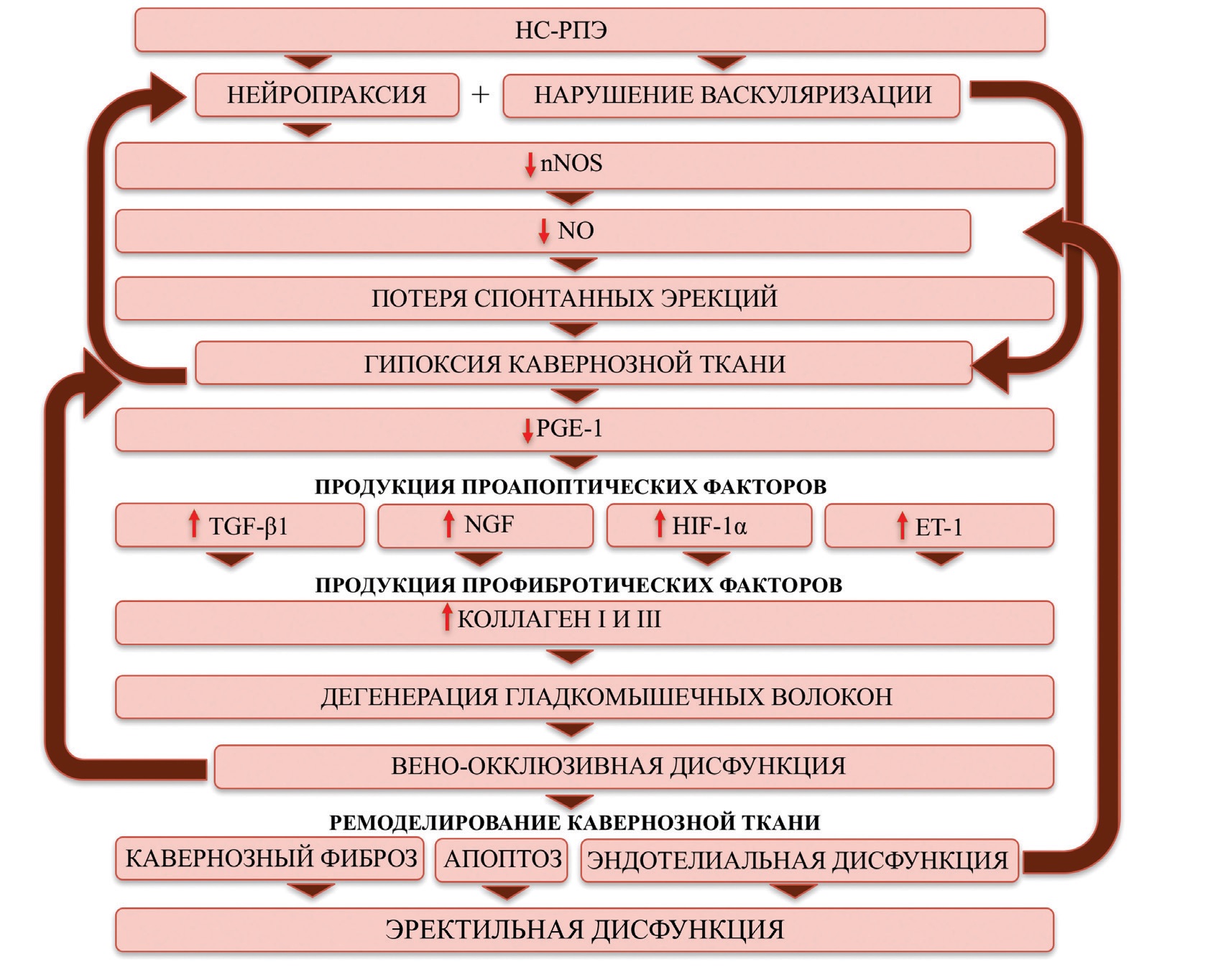
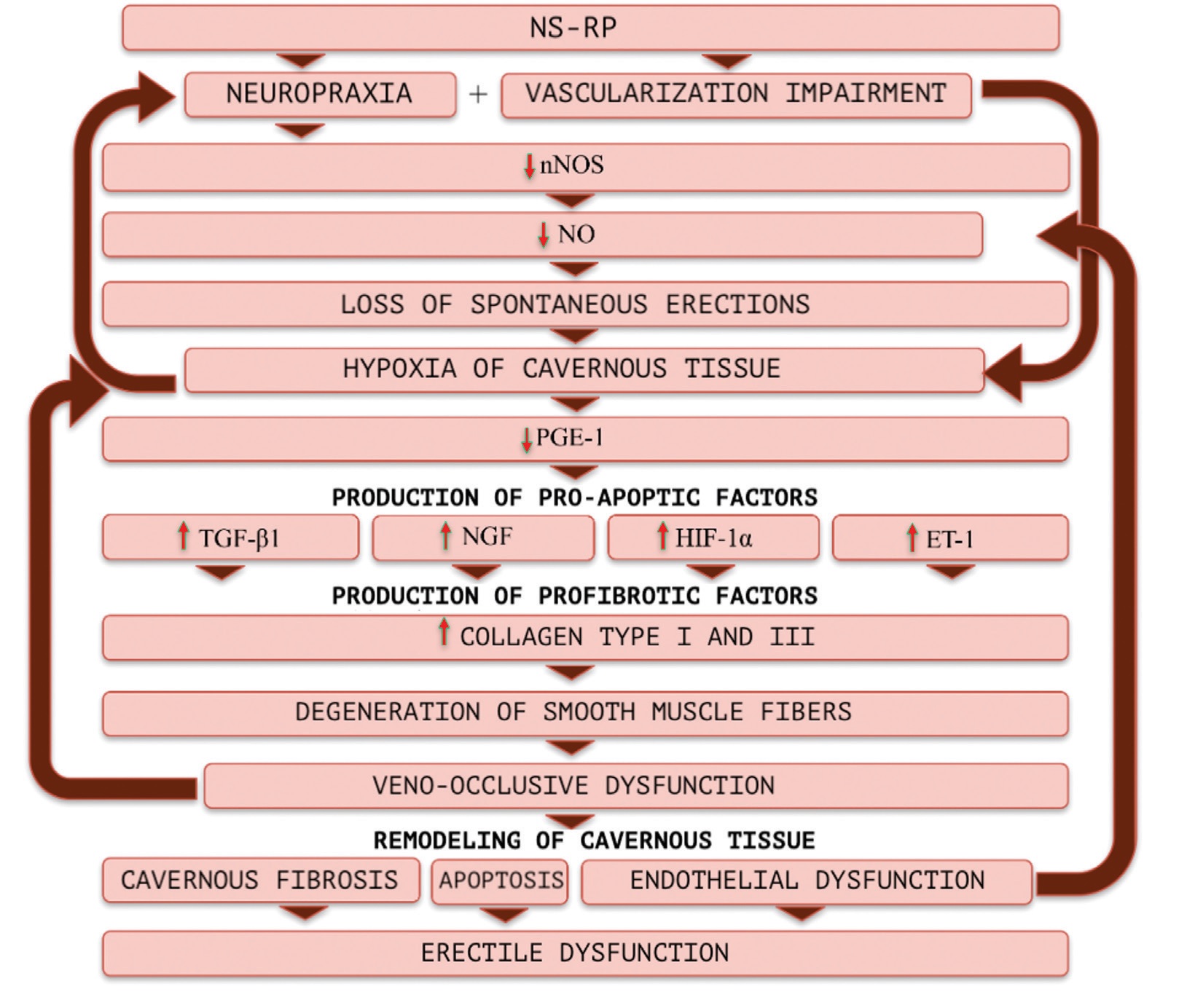
Рис. 1. Патогенез эректильной дисфункции после радикальной простатэктомии
Fig. 1. Pathogenesis of erectile dysfunction after radical prostatectomy
ПЕНИЛЬНАЯ РЕАБИЛИТАЦИЯ
Пенильная (сексуальная) реабилитация (ПР) – это комплекс послеоперационных мероприятий, направленных на раннее восстановление ЭФ с использованием медикаментозной терапии или других методов лечения [5, 9, 11]. По мнению J. Mulhall цель ПР после НС-РПЭ – это минимизация повреждений кавернозной ткани в течение периода нейрогенного восстановления с помощью обеспечения достаточной оксигенации в кавернозной ткани [12]. K. Hoyland и соавт. считают, что процесс восстановления нервной регенерации может достигать 3 лет [9]. Реабилитацию следует начинать как можно раньше для защиты и/или предотвращения повреждения эндотелия и гладкой мускулатуры [10]. По мнению T. Hakky и соавт. раннее достижение эрекций является важнейшей целью после тазовой хирургии [11]. На сегодняшний день не существует единого мнения относительно идеального режима ПР [10].
В настоящее время применяются различные методы лечения ЭД после РПЭ, при этом используют как монотерапию, так и комбинированные подходы для реабилитации ЭФ после РПЭ.
Ингибиторы фосфодиэстеразы 5 типа (и-ФДЭ5)
Ингибиторы фосфодиэстеразы 5 типа являются первой линией терапии в восстановлении эректильной сфункции (ЭФ) у пациентов после НС-РПЭ, они продемонстрировали высокую эффективность, простоту использования, хорошую переносимость и безопасность с положительным воздействием на качество жизни. Механизм действия препаратов и-ФДЭ5 связан с конкурентным и обратимым угнетением активности фермента фосфодиэстеразы 5 типа. Наиболее распространенные препараты этой группы Силденафил, Тадалафил, Варденафил, Уденафил и достаточно новый – Аванафил. Частота ответа на лечение Силденафилом у пациентов после НС-РПЭ в разных исследованиях варьируется от 35% до 75%, Варденафилом – до 71% и Тадалафилом – до 71% [13-15]. В проведенном метаанализе G. Corona и соавт. подтвердили, что действие Аванафила при лечении ЭФ обладает эффективностью сравнимой с остальными препаратами группы и-ФДЭ5 [16].
F. Montorsi и соавт. в масштабном мультицентровом исследовании в Европе и США изучали влияние тадалафила у пациентов с ЭД после НС-РПЭ. Улучшение эректильной функции было достигнуто у 71% пациентов, принимавших 20 мг тадалафила vs. 24% у больных, принимавших плацебо частота успешных попыток совершить половой акт достигала 54% и 26% соответственно [15]. Сходным образом, в мультицентровом, рандомизированном, проспективном, плацебоконтролируемом исследовании на 440 пациентах с ЭД после НС-РПЭ был протестирован варденафил. При приеме 10 и 20 мг варденафила эректильная функция улучшилась на 71% и 60% соответственно. Расширенный анализ этой же когорты пациентов показал преимущество варденафила vs. плацебо в отношении удовлетворенности половым актом, твердости эрекции, оргазма и общей удовлетворенности сексуальным опытом [14].
В 2014 году F. Montorsi и соавт., в крупном многоцентровом исследовании «REACTТ» в течение 9 месяцев изучали эффективность Тадалафила 5 мг и 20 мг у пациентов после НС-РПЭ. Ежедневный прием Тадалафила 5 мг показал более высокие результаты восстановления ЭФ после НС-РПЭ [17]. Более того, по мнению I. Moncada и соавт. ежедневный прием Тадалафила 5 мг значительно сокращает время восстановления ЭФ по сравнению с Тадалафилом «по требованию» [18]. В 2016 году D. Kim и соавт. в проспективном, рандомизированном, плацебо-контролируемом исследовании приводят противоположные результаты и считают, что прием Силденафила на ночь в дозировке 50 мг не дает терапевтического эффекта для восстановления ЭФ у пациентов после РПЭ по сравнению с дозировкой «по требованию» [19]. В том же году E. Hirik и соавт., изучали эффективность ежедневного приема Тадалафила 5 мг в течение 2,5 месяцев у 50 пациентов после НС-РПЭ с сохранной половой функцией до операции. При оценке по опроснику МИЭФ-5 через 3 месяца приема пациенты распределились по степени тяжести ЭД сл. образом: тяжелая – 6 (12%) пациентов, умеренная – 2 (4%), легкая – 6 (12%) и у 36 (72%) отсутствовала ЭД; через 6 месяцев: 5 (10%) пациентов, 3 (6%), 7 (14%) и 35 (70%) тяжелую, умеренную, легкую ЭД или ее отсутствие соответственно (p>0,05) [20]. Н. Cui и соавт., отметили улучшении ЭФ, когда длительный прием Тадалафила 5 мг один раз в день сочетался с Силденафилом 50 мг по мере необходимости [21].
Результаты приведенных исследований не позволяют сделать единый вывод о предпочтительной дозировки и-ФДЭ5 для фармакологической программы ПР после РПЭ. При анализе работ, посвященных ПР у пациентов после НС-РПЭ с помощью и-ФДЭ5 за последние 10 лет, можно обратить внимание на тенденцию к назначению медикаментозной терапии низкими дозами в течение длительного применения.
Ударно-волновая терапия
Это относительно новый неинвазивный метод терапии ЭД, основанный на использовании ударных волн низкой интенсивности, усиливающий местный контролируемый ангиогенез и значительно улучшающий гемодинамику полового члена. В 2016 году Z. Lu и соавт. представили первый систематический обзор и мета-анализ, в котором оценивали эффективность низкоинтенсивной экстракорпоральной ударной волны для лечения ЭД. В 14 исследований вошло 833 пациента с 2005 по 2015 год. Мета-анализ показал, что ударно-волновая терапия может значительно улучшить средний балл опросника МИЭФ (p<0,0001) и шкалы твердости эрекции (Erection Hardness Scale -EHS) (р=0,01). Терапевтическая эффективность может длиться не менее 3 месяцев. У пациентов с умеренной степенью ЭД терапевтическая эффективность после лечения была лучше, чем у пациентов с более выраженной ЭД или сопутствующими заболеваниями [22]. На сегодняшний день крупных работ, посвященных ПР у пациентов после НС-РПЭ с помощью ударно-волновой терапии нет.
Вакуум-эректорная терапия – VED
Механизм работы VED основан полностью на физическом принципе действия. За счет создания отрицательного давления происходит перерастяжение корпоральных синусоидов и осуществляется наполнение полового члена кровью.
Изначально вакуум устройства применялись только со сжимающим кольцом на основании тела полового члена – вакуумное констрикторное устройство (vacuum constriction device – VCD). Отличие от обычного устройства для вакуумной эрекции (vacuum erection device – VED) заключается в наличии кольца, препятствующего оттоку крови из полового члена. В результате, после снятия колбы мужчина способен к осуществлению пенетрации. Многие авторы описывают этот метод крайне неудобным для пациентов в связи со сложностью организации процесса, отсутствием спонтанности, а также приводящим к ишемии.
В настоящее время использование вакуумной терапии без констрикторных колец рассматривается как метод восстановления ЭФ в ПР у пациентов после РПЭ за исключением совершения полового акта по требованию [6].
Несмотря на то, что в 2006 г. Управление по контролю качества пищевых продуктов и лекарственных средств США (FDA) одобрило использование VED, как прибора для создания и поддержания эрекции путем притока артериальной крови к половому члену в течение периода восстановления ЭФ после РПЭ, не было ни одного крупного многоцентрового, рандомизированного, контролируемого исследования VED в качестве ПР. В 2001 году C. Zippe и соавт., одни из первых представили результаты о восстановлении ЭФ у пациентов после РПЭ с помощью VED. 80% мужчин после ежедневного применения VED (с кольцом и без) могли осуществлять половой акт дважды в неделю, у 55% через 9 месяцев появились естественные эрекции после ежедневного использования VED [23]. T. Kohler и соавт. описывают, что более 60% пациентов при использовании VED после РПЭ через 3 и 6 месяцев имели более высокий балл МИЭФ-5 по сравнению с контрольной группой [24]. B. Dalkin и соавт., в проспективном исследовании у 42 мужчин в качестве ПР ежедневно использовали VED в течение 90 дней. Авторы пришли к выводу, что раннее использование VED обеспечило восстановление сексуальной активности [25]. Тем не менее ряд экспертов считают использование VED в программе ПР сомнительным в связи с теоретическим риском ишемии, склероза и фиброза кавернозной ткани [2].
Интракавернозные инъекции
Местные интракавернозные инъекции относятся ко 2-й линии терапии ЭД и назначаются при отсутствии ответа на прием и-ФДЭ5. Стоит отметить, что интракавернозным инъекциям до сих пор не отведено место в профилактике ЭД у пациентов после НС-РПЭ.
При внутрикавернозном введении Алпростадил ингибирует α1-адренорецепторы в тканях, расслабляет мускулатуру кавернозных тел, увеличивает кровоток и улучшает микроциркуляцию. Алпростадил вызывает эрекцию путем релаксации трабекулярной гладкой мускулатуры пещеристых тел и дилатации кавернозных артерий, что ведет к расширению лакунарных пространств и перекрытию кровотока за счет прижатия венул к белочной оболочке.
F. Montorsi в 1997 г. один из первых предложил всем пациентам в послеоперационном периоде применение интракавернозных форм алпростадила с целью улучшения оксигенации кавернозной ткани [26]. T. Domes и соавт. отметили, что у 67% пациентов после НС-РПЭ применение интракавернозных инъекций простогландина E1 (PGE1) в течение 6 месяцев позволило достичь эрекции, достаточной для пенетрации, в то время как у пациентов контрольной группы, не получавшей лечения, данный показатель не превышал 20% [27].
Несмотря на высокий процент успеха данной терапии боль в половом члене в момент детумесценции остается самым частым побочным эффектом терапии Алпростадила.
Протезирование полового члена
При отсутствии положительной динамики ПР после назначения первой и второй линий терапии ЭД у пациентов после НС-РПЭ протезирование полового члена считается крайней мерой медицинской помощи [10]. Показанием для данного метода является необратимое ремоделирование кавернозной ткани при неэффективности профилактики и лечения ЭД у пациентов после НС-РПЭ. По мнению S. Wilson и соавт. удовлетворенность пациентов, подвергшихся фаллопротезированию гидравлическими имплантами после РПЭ, а также их партнерш достигает 90% [28]. После перенесенной РПЭ ретциево пространство, в которое обычно имплантируют резервуар 3-х компонентного пенильного протеза, склерозировано. В результате попытка стандартного размещения баллона под поперечную фасцию может привести к разрыву мочевого пузыря или повреждению подвздошных сосудов с фатальным кровотечением. С целью предотвращения данных осложнений наиболее предпочтительна эктопическая установка резервуара над поперечной фасцией. Также существует современная концепция симультанного протезирования полового члена у пациентов с запланированной РПЭ без сохранения сосудисто-нервных пучков. Возможность протезирования полового члена во время основного этапа РПЭ может быть предпочтительной для пациентов, которым нервосберегающая техника не может гарантировать полного восстановления ЭФ.
Комбинированная терапия
Комбинированная терапия — это альтернативный подход в различных сочетаниях при отсутствии ответа на монотерапию или сразу, когда у пациента имеется высокий риск возникновения ЭД после НС-РПЭ. J. Chen и соавт. оценивали эффективность действия Силденафила и вакуум терапии у 161 пациента после НС-РПЭ. Все пациенты были рандомизированы на 2 группы в зависимости от вида монотерапии. Через 2 месяца 41 пациент пожаловались на отсутствие результатов и была сформирована отдельная когорта, принимавших комбинированную терапию, сочетающую Силденафил и VED. Авторы отметили, что в группе с комбинированной терапией было существенное увеличение баллов во всех доменах МИЭФ [29]. О. Canguvenet и соавт., описывают эффективность комбинированной терапии, сочетавшей и-ФДЭ5 и VED у 69 пациентов. Авторы отмечают улучшение среднего балла по опроснику МИЭФ у 74% пациентов [30]. J. Engel в рандомизированном исследовании сравнивал результаты ПР у пациентов после робот-ассистированной НС-РПЭ. В группу I вошли 10 пациентов, получавших монотерапию препаратом Тадалафил, в группу II – 13 мужчин, использовавших комбинированную терапию: VED и Тадалафил. В группе II средний балл опросника МИЭФ-5 и показатель шкалы жесткости пениса были значительно выше, чем в группе I. По данным анализа результатов через 12 месяцев терапии 92% пациентов группы II были в состоянии осуществлять половой акт vs 57% – из группы I [31].
Данные вышеуказанных исследований подтверждают, что комбинированные программы реабилитации способствуют восстановлению ЭФ после РПЭ с лучшими результатами по сравнению с монотерапией.
ВЫВОДЫ
Главная задача пенильной реабилитации после НС-РПЭ – это помощь мужчинам в восстановлении спонтанной, полноценной эрекции, достаточной для проведения полового акта на более ранних сроках послеоперационного периода с целью повышения качества жизни. К сожалению, медикаментозная монотерапия ЭД у пациентов после НС-РПЭ демонстрирует противоречивые результаты. На сегодняшний день перспективно развитие стратегий комбинированных подходов для реабилитации ЭФ после РПЭ. Необходимо дальнейшее усовершенствование техники выполнения НС-РПЭ, более глубокое понимание ведения послеоперационного процесса для разработки алгоритма выбора программы восстановления ЭФ. Более раннее начало половой жизни после операции позволяет в ряде случаев значительно улучшить качество жизни пациентов и семейные отношения между супругами.
ЛИТЕРАТУРА
1. Качмазов А.А., Кешишев Н.Г., Огнерубова И.Н., Григорьева М.В., Казаченко А.В., Алексеев Б.Я. Проблема раннего восстановления удержания мочи после радикальной простатэктомии. Онкоурология 2017;13(4):70-78. [Kachmazov A.A., Keshishev N.G., Ognerubova I.N., Grigor'eva M.V., Kazachenko A.V., Alekseev B. Ya. The problem of early continence recovery after radical prostatectomy. Onkourologiya = Cancer Urology 2017;13(4):70- 78. (In Russia)]. https://doi.org/10.17650/1726-9776-2017-13-4-70-78.
2. Глыбочко П.В., Матюков И.П., Аляев Ю.Г., Ахвледиани Н.Д., Иноятов Ж.Ш. Сексуальная функция пациентов, перенесших радикальную простатэктомию: современный взгляд на проблему. Урология 2015(2):112-116. [Glybochko P.V. Matjuhov I.P., Aljaev Ju.G., Ahvlediani N.D., Inojatov Zh.Sh. Sexual function of patients undergoing radical prostatectomy: a modern view of the problem. Urologiya = Urologiia 2015(2):112-116. (In Russian)].
3. Петровский Н.В., Глыбочко П.В., Аляев Ю.Г., Амосов А.В., Крупинов Г.Е. Локальный рецидив рака предстательной железы после радикальной простатэктомии. Урология 2017(4):85-90. [Petrovskii N.V., Glybochko P.V., Alyaev Yu.G., Amosov A.V., Krupinov G.E. Local recurrence of prostate cancer after radical prostatectomy. Urologiya = Urologiia 2017(4):85-90. https://doi.org/10.18565/urol.2017.4.85-90. (In Russian)].
4. Gandaglia G, Suardi N, Cucchiara V, Bianchi M, Shariat SF, Roupret M, et al. Penile rehabilitation after radical prostatectomy: does it work? Transl Androl Urol 2015;4(2):110-123. https://doi.org/10.3978/j.issn.2223-4683.2015.02.01.
5. Велиев Е.И., Ванин А.Ф., Котов С.В., Шишло В.К. Современные аспекты патофизиологии и профилактики эректильной дисфункции и кавернозного фиброза после радикальной простатэктомии. Урология 2009(2):46-51. [Veliev Ye.I., Vanin A.F., Kotov S.V., Shishlo V.K. Modern aspects of pathophysiology and prevention of erectile dysfunction and cavernous fibrosis after radical prostatectomy. Urologiya = Urologiia 2009(2):46-51. (In Russian)].
6. Lin H, Wang G, Wang R. Vacuum erectile device for penile rehabilitation. J Integr Nephrol Androl 2014(1):4-10. https://doi.org/10.4103/2225-1243.137541.
7. Mottet N, Bellmunt J, Bolla M, Briers E, Cumberbatch MG, De Santis M, et al. EAU-ESTRO-SIOG Guidelines on Prostate Cancer. Part 1: Screening, Diagnosis, and Local Treatment with Curative Intent. Eur Urol 2017;71(4):618- 629. https://doi.org/10.1016/j.eururo.2016.08.003.
8. Qian SQ, Gao L, Wei Q, Yuan J. Vacuum therapy in penile rehabilitation after radical prostatectomy: review of hemodynamic and antihypoxic evidence. Asian J Androl 2016;18(3):446-451. https://doi.org/10.4103/1008-682X.159716.
9. Hoyland K, Vasdev N, Adshead J. The use of vacuum erection devices in erectile dysfunction after radical prostatectomy. Rev Urol 2013;15(2):67-71.
10. Chung E, Gillman M. Prostate cancer survivorship: a review of erectile dysfunction and penile rehabilitation after prostate cancer therapy. Med J Aust 2014;200(10):582-585. https://doi.org/10.5694/mja13.11028.
11. Hakky TS, Baumgarten AS, Parker J, Zheng Y, Kongnyuy M, Martinez D, et al. Penile rehabilitation: the evolutionary concept in the management of erectile dysfunction. Curr Urol Rep 2014;15(4):393. https://doi.org/10.1007/ s11934-014-0393-6.
12. Mulhall JP, Morgentaler A. Controversies in sexual medicine: penile rehabilitation should become the norm for radical prostatectomy patients. J Sex Med 2007(4):538–43. https://doi.org/10.1111/j.1743-6109.2007.00486.x
13. Salonia A, Burnett AL, Graefen M, Hatzimouratidis K, Montorsi F, Mulhall JP, et al. Prevention and management of postprostatectomy sexual dysfunctions part 2: recovery and preservation of erectile function, sexual desire, and orgasmic function. Eur Urol 2012;62(2):273-286. https://doi.org/10.1016/ j.eururo.2012.04.047.
14. Nehra A, Grantmyre J, Nadel A, Thibonnier M, Brock G. Vardenafil improved patient satisfaction with erectile hardness, orgasmic function and sexual experience in men with erectile dysfunction following nerve sparing radical prostatectomy. J Urol 2005;173(6):2067-2071. https://doi.org/10.1097/01.ju.0000158456.41788.93.
15. Montorsi F, Nathan HP, McCullough A, Brock GB, Broderick G, Ahuja S, et al. Tadalafil in the treatment of erectile dysfunction following bilateral nerve sparing radical retropubic prostatectomy: a randomized, double-blind, placebo controlled trial. J Urol 2004;172(3):1036-1041. https://doi.org/10.1097/01.ju.0000136448.71773.2b.
16. Corona G, Rastrelli G, Burri A, Jannini EA, Maggi M. The safety and efficacy of Avanafil, a new 2(nd) generation PDE5i: comprehensive review and meta-analysis. Expert Opin Drug Saf 2016;15(2):237-247. https://doi.org/10.1517/14740338.2016.1130126.
17. Montorsi F, Brock G, Stolzenburg JU, Mulhall J, Moncada I, Patel HR, et al. Effects of tadalafil treatment on erectile function recovery following bilateral nerve-sparing radical prostatectomy: a randomised placebo-controlled study (REACTT). Eur Urol 2014;65(3):587-596. https://doi.org/10.1016/ j.eururo.2013.09.051.
18. Moncada I, de Bethencourt FR, Lledó-García E, Romero-Otero J, Turbi C, Büttner H, et al. Effects of tadalafil once daily or on demand versus placebo on time to recovery of erectile function in patients after bilateral nerve-sparing radical prostatectomy. World J Urol 2015;33(7):1031-1038. https://doi.org/10.1007/s00345-014-1377-3.
19. Kim DJ, Hawksworth DJ, Hurwitz LM, Cullen J, Rosner IL, Lue TF, et al. A prospective, randomized, placebo-controlled trial of on-demand vs. nightly sildenafil citrate as assessed by Rigiscan and the international index of erectile function. Andrology 2016;4(1):27-32. https://doi.org/10.1111/ andr.12118.
20. Hirik E, Bozkurt A, Karabakan M, Onuk Ö, Balcı MB, Aydın M, et al. Results of tadalafil treatment in patients following an open nerve-sparing radical prostatectomy. Arch Ital Urol Androl 2016;88(1):4-6. https://doi.org/10.4081/ aiua.2016.1.4
21. Cui H, Liu B, Song Z, Fang J, Deng Y, Zhang S, et al. Efficacy and safety of long-term tadalafil 5 mg once daily combined with sildenafil 50 mg as needed at the early stage of treatment for patients with erectile dysfunction. Andrologia 2015;47(1):20-24. https://doi.org/10.1111/and.12216
22. Lu Z, Lin G, Reed-Maldonado A, Wang C, Lee YC, Lue TF. Low-intensity Extracorporeal Shock Wave Treatment Improves Erectile Function: A Systematic Review and Meta-analysis. Eur Urol 2017;71(2):223-233. https://doi.org/10.1016/j.eururo.2016.05.050.
23. Zippe CD, Raina R, Thukral M, Lakin MM, Klein EA, Agarwal A. Management of erectile dysfunction following radical prostatectomy. Curr Urol Rep 2001;2(6):495-503. https://doi.org/10.1007/s11934-001-0045-5.
24. Köhler TS, Pedro R, Hendlin K, Utz W, Ugarte R, Reddy P, et al. A pilot study on the early use of the vacuum erection device after radical retropubic prostatectomy. BJU Int 2007;100(4):858-862. https://doi.org/10.1111/ j.1464-410X.2007.07161.x.
25. Dalkin BL, Christopher BA. Preservation of penile length after radical prostatectomy: early intervention with a vacuum erection device. Int J Impot Res 2007;19(5):501-504. https://doi.org/10.1038/sj.ijir.3901561.
26. Montorsi F, Guazzoni G, Strambi LF, Da Pozzo LF, Nava L, Barbieri L, et al. Recovery of spontaneous erectile function after nerve-sparing radical retropubic prostatectomy with and without early intracavernous injections of alprostadil: results of a prospective, randomized trial. J Urol 1997;158(4):1408-1410.
27. Domes T, Chung E, DeYoung L, MacLean N, Al-Shaiji T, Brock G. Clinical outcomes of intracavernosal injection in postprostatectomy patients: a single-center experience. Urology 2012;79(1):150-155. https://doi.org/10.1016/ j.urology.2011.09.009.
28. Wilson SK, Delk JR, Salem EA, Cleves MA. Long-term survival of inflatable penile prostheses: single surgical group experience with 2,384 first-time implants spanning two decades. J Sex Med 2007;4(4 Pt 1):1074-1079. https://doi.org/10.1111/j.1743-6109.2007.00540.x.
29. Chen J, Sofer M, Kaver I, Matzkin H, Greenstein A. Concomitant use of sildenafil and a vacuum entrapment device for the treatment of erectile dysfunction. J Urol 2004;171(1):292-295. https://doi.org/10.1097/01.ju.0000098460.02560.fe.
30. Canguven O, Bailen J, Fredriksson W, Bock D, Burnett AL. Combination of vacuum erection device and PDE5 inhibitors as salvage therapy in PDE5 inhibitor nonresponders with erectile dysfunction. J Sex Med 2009;6(9):2561-2567. https://doi.org/10.1111/j.1743-6109.2009.01364.x.
31. Engel JD. Effect on sexual function of a vacuum erection device postprostatectomy. Can J Urol 2011;18(3):5721-5725.







