Диагностика и лечение почечно-клеточного рака (ПКР) являются одной из наиболее актуальных проблем современной онкоурологии, что связано с неуклонным ростом заболеваемости данной патологией во всем мире. Так, в 2012 году зарегистрировано более 337 000 первичных больных ПКР и 143 369 пациентов погибло от этого заболевания [1]. В России в 2013 г. выявлено 20 892 больных со злокачественными новообразованиями почки и 8 459 человек умерли от ПКР, стандартизованный показатель заболеваемости злокачественными опухолями почки в 2013 году составил 9,39 на 100 000 населения, занимая по темпам прироста онкологической заболеваемости за последние 10 лет одно из ведущих мест (29,4%). Тем не менее, несмотря на увеличивающиеся показатели заболеваемости, начиная с 2012 года впервые за последнее время отмечено снижение показателя смертности, которое с 2003 по 2013 годы составило 4,25% [2].
Подковообразная почка – наиболее распространенная аномалия формы почек и встречается у 0,25% населения. Эта патология наблюдается с частотой примерно 2,8% среди всех аномалий развития почки [3-5]. Обычно отмечают сращение нижними сегментами, в 1,5-3,8% случаев наблюдается сращение в верхних сегментах. Чаще всего срощенная подковообразная почка является в большей или меньшей степени эктопированной. Значительно реже подковообразная почка располагается в обычном месте. В большинстве случаев перешеек почки находится на уровне IV или V поясничного позвонка. Очень редко наблюдается глубокая тазовая дистопия. Обычно левая половина почки располагается несколько выше правой.
Подковообразная почка является более фиксированной, чем нормальная. Эта фиксация является результатом ее многочисленных сосудистых связей и своеобразной формы органа. Перешеек почки обычно располагается кпереди от магистральных сосудов (аорты, нижней полой вены, общих подвздошных сосудов) и солнечного сплетения. Однако возможно и ретроаортальное расположение перешейка.
Обе срощенные почки часто являются асимметричными и неодинаковыми по объему. Как правило, расстояние между половинами подковообразной почки больше сверху, нежели в нижних отделах за счет более часто выявляемого сращения в этих сегментах. Однако в редких случаях, когда перешеек длинный, ось почек имеет нормальное положение. Отсутствие ротации почки ведет к тому, что в норме внутренняя грань почки располагается кпереди, ворота почки и синус также находятся вентрально. Изредка почечные ворота разделены тяжом из почечной паренхимы, и в таких случаях чашечки каждой почки соединяются и переходят в два отдельных синуса.
Подковообразная почка обычно дренируется двумя мочеточниками, иногда — тремя или четырьмя, очень редко — одним. Длина мочеточника тем меньше, чем более эктопирована почка. Возможны случаи, когда мочеточники располагаются ретроистмически на одной или обеих сторонах. В большинстве случаев подковообразных почек их мочеточники имеют характерное для этой аномалии положение. Так, они вначале направляются внутрь и кпереди, перекидываясь через перешеек или нижние полюса почек; затем, опускаясь кзади и кнаружи, описывают характерный изгиб. Мочеточники располагаются намного ближе к позвоночнику, нежели мочеточники нормальных почек [4, 7].
Более чем в 2/3 случаев подковообразные почки снабжаются 3-5 артериями для каждой половины. Иногда наблюдаются случаи, когда половина подковообразной почки имеет до 10 артерий. Почечные артерии в большинстве случаев отходят от аорты, но уровень их отхождения тем ниже, чем более выражена почечная эктопия. Таким образом, в васкуляризации почки могут участвовать общая подвздошная, нижняя брыжеечная, подчревная артерии и др. Сплетение, образуемое артериальными сосудами, прочно фиксирует почку на месте. Иногда такие особенности анатомического строения сосудистой системы подковообразной почки могут быть причиной сдавления мочеточников или лоханок и вызывать, таким образом, нарушение пассажа мочи.
Перешеек, по данным разных исследователей, в 25-63% случаев имеет свою собственную артерию, которая входит в него со стороны задней поверхности. Отходит эта артерия чаще всего от аорты, реже – от брыжеечных или общих подвздошных артерий. О наличии артерии перешейка необходимо помнить во время оперативного вмешательства на подковообразной почке [3, 5, 6].
Вены менее многочислены, чем артерии. Они впадают в нижнюю полую или в общую подвздошную вену. В значительном числе случаев каждая половина подковообразной почки имеет одну большую вену и несколько мелких [3-5].
Опухоли подковообразной почки наблюдаются крайне редко и встречаются у 2% больных с этой аномалией [5-8]. Основными симптомами опухоли подковообразной почки являются пальпируемая опухоль, гематурия и боль. Нередко, особенно при экстраорганном расположении, опухоль подковообразной почки принимают за опухоль брюшной полости или забрюшинного пространства. На ранних стадиях заболевание протекает, как правило, бессимптомно [6-8]. Внедрение в клиническую практику современных методов обследования привело к увеличению частоты выявления локализованных опухолей, в том числе у больных с пороками развития почек.
МАТЕРИАЛЫ И МЕТОДЫ
Приводим описание клинического случая больной А., 66 лет с диагнозом рак левой половины подковообразной почки I ст T1aN0M0.
Больная А., 66 лет поступила в отделение онкоурологии МНИОИ им. П. А. Герцена 12.12.2014. Из анамнеза известно, что при профилактическом обследовании по месту жительства в декабре 2014 года при УЗИ обнаружена опухоль подковообразной почки. Для проведения дообследования и выработки лечебной тактики больная направлена в МНИОИ им. П. А. Герцена. На момент госпитализации предъявляла жалобы на общую слабость, ощущение тяжести в левой поясничной области. Из сопутствующих заболеваний у больной отмечены гипертоническая болезнь 3-й ст., язвенная болезнь 12-перстной кишки, в стадии ремиссии, глаукома, гипотиреоз (состояние после резекции правой доли щитовидной железы по поводу многоузлового зоба от 2002 г).
При обследовании в институте по данным УЗИ и компьютерной томографии органов брюшной полости определяется аномалия строения почек, при которой они соединены их нижними полюсами посредством предаортального перешейка из почечной ткани. В нижней трети левой половины почки определяется патологические образование, деформирующее задненижний контур почки. Выявленное образование овальной формы, размерами 4,6x3,3x3,6 см (рис.1, 2). Плотность образования при нативной компьютерной томографии (КТ) практически не отличается от плотности неизмененной паренхимы почки и составляет 20-30 HU. При проведении контрастного усиления отмечено отчетливое неравномерное накопление контрастного препарата по контуру образования, соответствующее корковому слою почечной паренхимы, с повышением денситометрических показателей до 60 (230 HU) в артериальную фазу, а затем их снижение до 90-117 HU в паренхиматозную фазу. В паренхиматозную фазу контрастного усиления выявленное образование становится гиподенсивным относительно паренхимы почки. Чашечнолоханочная система несколько расширена, отмечается типичная ротация ворот почек кпереди и кверху. В нижней группе чашечек левой половины почки определяется конкремент овальной формы, размерами 0,9x0,5 см. Выявлены множественные почечные артерии, отходящие от аорты на уровне межпозвонкового диска L1-L2 (диаметром 0,7 см и 0,8 см) и на уровне тела L3 позвонка (диаметром 0,5 см), общим количеством до 7. Кровоснабжение перешейка почки осуществляется за счет собственной артерии, отходящей от аорты на уровне тела L3 позвонка. Заключение: Опухоль левой половины подковообразной почки. Камень нижней группы чашечек левой половины подковообразной почки.
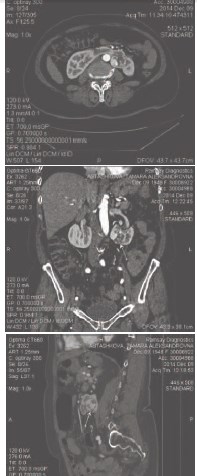
Рис. 1. КТ-картина опухоли подковообразной почки у больной Б., 66 лет. Стрелкой указано объемное образование
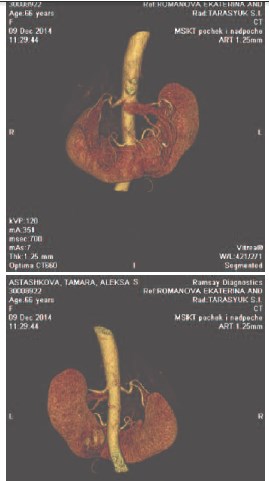
Рис. 2. 3-D реконструкция КТ-исследования у больной Б., 66 лет
По данным динамической нефросцинтиграфии артериальный приток к обеим половинам срощенной в нижних отделах подковообразной почки своевременный, к левой половине почки выше, чем к правой. В левой половине почки определяется объемное образование. Паренхиматозная функция своевременная, достаточная, выведение немного замедлено, отток не задержан, неравномерный. Паренхиматозно-выделительная функция правой половины почки не нарушена, отток своевременный, неравномерный. Косвенные признаки ХПН отсутствуют.
При комплексном обследовании, проведенном в МНИОИ им. П. А. Герцена, признаков другой очаговой патологии и генерализации процесса у больной не выявлено. Таким образом, у больной установлен клинический диагноз: рак подковообразной почки I стадии сT1bNxM0.
26.12.2014 г. пациентке выполнено оперативное вмешательство в объеме резекции подковообразной почки. На операции: выполнена срединная лапаротомия. В брюшной полости асцита, диссеминации, метастазов в печень не выявлено. Забрюшинное пространство вскрыто по линии Тольда. При ревизии выявлена подковообразная почка, срощенная в нижних отделах при помощи перешейка толщиной до 5 см, располагающегося кпереди от аорты и нижней полой вены. В ее левой половине по задней поверхности определяется опухолевое образование, располагающееся в области нижнего полюса размером до 4,5 см в диаметре. Внебрюшинно мобилизованы перешеек, нижняя треть правой и левой половины почки. Частично острым, частично тупым путем выделены и прослежены правый и левый мочеточники (рис. 3), артерии и вены правой и левой половины почки. Мобилизованы три артерии и вена левой половины подковообразной почки. Клетчатка области ворот почки удалена. Почка выделена в области перешейка, выполнена парааортальная лимфаденэктомия. Определяется собственная артерия, кровоснабжающая перешеек почки диаметром до 3 мм (рис. 4), которая пересечена при помощи аппарата Ligashure.
Для разобщения половин почки, на перешеек наложен сшивающий аппарат TLC-75 (трехрядный скрепочный шов), перешеек пересечен (рис. 5). По задней поверхности левой половины подковообразной почки определяется опухолевый узел, размерами до 4,5 см (рис. 6). Сосуды левой половины почки пережаты мягким зажимом Сатинского. На расстоянии 0,5 см от опухолевого узла, выполнена резекция подковообразной почки в переделах здоровых тканей (рис. 7). Препарат удален. На паренхиму наложены гемостатические швы атравматической нитью (рис. 8). Гемостаз. Время аноксии почки 15 мин. Через контрапертуру в забрюшинное пространство к зоне выполненной резекции почки установлен однопросветный дренаж. Рана послойно ушита узловыми швами. Швы на кожу. Йод. Асептическая повязка.
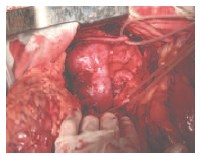
Рис. 3. Перешеек и мочеточники (на держалках) подковообразной почки
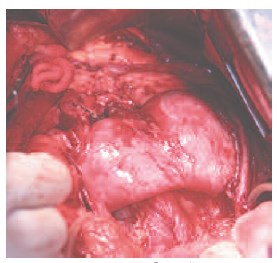
Рис. 4. Перешеек подковообразной почки с кровоснабжающей его артерией
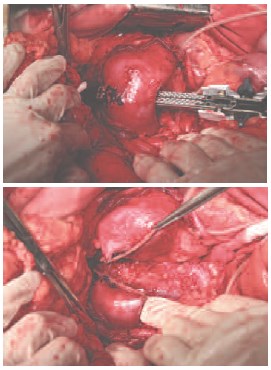
Рис. 5. Разделение подковообразной почки в области перешейка с использованием сшивающего аппарата TLC-75
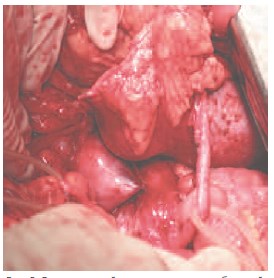
Рис. 6. Опухоль левой половины подковообразной почки, расположенная по ее дорсальной поверхности
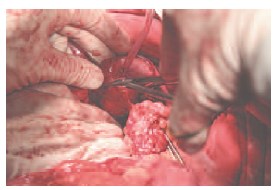
Рис. 7. Резекция левой половины подковообразной почки
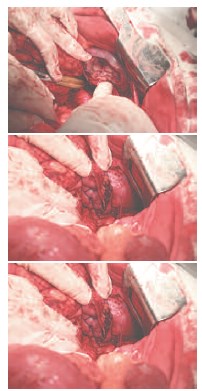
Рис. 8. Окончательный вид резецированной почки
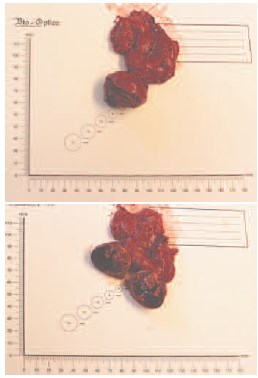
Рис. 9. Резецированная опухоль левой половины подковообразной почки с блоком паранефральной клетчатки
Результаты гистологического исследования № Э47118-20/оп. Описание макропрепарата: фрагмент ткани почки размерами 4,5х3,3х3 см, с прилежащей клетчаткой размерами 6,5х4х2 см. Подкапсульно, в ткани почки определяется мягко-эластичный опухолевый узел размером 4,1х3х2,5 см, на разрезе – пестрого вида, серо-желтый с кровоизлияниями. Минимальное расстояние от опухоли до края резекции – 1 мм. В прилежащей жировой клетчатке – без очаговых уплотнений. Межаортокавальная клетчатка – фрагмент жировой клетчатки размерами 5,5х4 см, из которой выделено 4 лимфоузла, максимальными размерами до 1 см.
Описание микропрепарата: Опухолевый узел в почке представлен почечноклеточным светлоклеточным раком, II степени анаплазии по Фурману, без инвазии в капсулу почки. В краях резекции опухолевого роста нет. В 4-х лимфатических узлах и в паранефральной жировой клетчатке над опухолью опухолевого роста нет (рис. 9).
Таким образом, у больной установлен окончательный диагноз: рак подковообразной почки I стадии pT1bN0M0. Послеоперационный период протекал без осложнений. Дренаж удален на 4-е сутки, швы – на 9-е сутки. Больная выписана из стационара на 10-е сутки после операции. При контроле уровня азотистых шлаков крови 27.12.2014 г. на первые сутки после операции отклонений от нормальных значений не обнаружено. Уровень мочевины составил 4,67 ммоль/л, креатинина – 109 мкмоль/л, калий – 4,6 ммоль/л. На 9-е сутки после операции уровень мочевины составил 5,2 ммоль/л, креатинина – 107 мкмоль/л, калия – 4,4 ммоль/л. Больная выписана в удовлетворительном состоянии.
ОБСУЖДЕНИЕ
Подковообразная почка является наиболее распространенной аномалией формы почек (0,25% населения), при этом у мужчин данная патология выявляется в 2 раза чаще, чем у женщин. Опухоли подковообразной почки чаще всего представлены почечно-клеточным раком, гораздо реже – опухолью Вильмса. В нашем клиническом случае опухоль представлена почечноклеточным светлоклеточным раком, II степени анаплазии по Фурману. Для диагностики опухолей подковообразной почки помимо основных методов визуальной диагностики (УЗИ, КТ) мы рекомендуем использовать 3-D реконструкцию КТ исследования для более точного определения локализации опухоли и ее взаимоотношения с сосудистой системой почки. В данном клиническом наблюдении обе половины подковообразной почки были срощены в типичном месте – в нижних сегментах. Подковообразная почка была дистопирована, кровоснабжение осуществлялось посредством множества артерий, отходящих от аорты, перешеек располагался кпереди от аорты и нижней полой вены, и имел собственную артерию. Опухоль располагалась по задней поверхности в нижней трети левой половины подковообразной почки, что предполагало некоторые технические трудности при ее выделении.
Как уже было отмечено выше, оперативное лечение является основным методом лечения больных ПКР. Хирургическое лечение рака подковообразной почки основано на тех же принципах, что и хирургическое лечение рака почки без аномалии развития. По возможности следует отдавать предпочтение органосохраняющим методам. В то же время, наличие аномалий развития почек может существенно усложнить запланированное оперативное вмешательство. Учитывая расположение опухоли по задней поверхности подковообразной почки, предпочтение отдано открытому доступу, при этом перешеек и собственная артерия перешейка были пересечены, что дало возможность мобилизации левой половины подковообразной почки и доступу к ее задней поверхности, на которой располагалась опухоль.
Подковообразная почка имеет уникальные анатомические особенности, которые делают хирургическое лечение рака почки технически сложной задачей. Выбор хирургического доступа и метода лечения должен осуществляться индивидуально для каждого пациента с учетом анатомических особенностей строения подковообразной почки, размера опухоли, ее расположения и наличия сопутствующих заболеваний. В связи с этим, важным моментом является тщательное обследование пациента на дооперационном этапе с использованием различных методов визуализации и выполнением трехмерной реконструкции органа, особенно при планировании органосохраняющей операции.
Таким образом, данное клиническое наблюдение свидетельствует о возможности выполнения органосохраняющего лечения у больных раком подковообразной почки.
ЛИТЕРАТУРА
- International Agency for Research on Cancer. The GLOBOCAN project: cancer incidence and mortality worldwide in 2012. // URL: http://globocan.iarc.fr/
- Злокачественные новообразования в России в 2013 году: заболеваемость и смертность. [Под ред. Каприна А.Д., Старинского В.В., Петровой Г.В.]. М., 2015. 250 c.
- Alamer A. Renal cell carcinoma in a horseshoe kidney: radiology and pathology correlation. // J Clin Imaging Sci. 2013. Vol.3. doi: 10.4103/2156-7514.109725.
- Koszutski T, Kudela G, Mikosiński M, Utrata W. Quadruplication of dystopic kidney in combination with ureteral cyst. // J Pediatr Surg. 2008. Vol. 43, N 12. P. e13-15.
- Tkocz M, Kupajski M. Tumour in horseshoe kidney different surgical treatment shown in five example cases. // Contemp Oncol (Pozn). 2012. Vol. 16, N 3. P. 254-257.
- Qi X, Liu F, Zhang Q, Zhang D. Laparoscopic heminephrectomy of a horseshoe kidney with giant renal cell carcinoma: A case report. // Oncol Lett. 2014. Vol. 8, N 5. P. 2040-2042.
- Stimac G, Dimanovski J, Ruzic B, Spajic B, Kraus O. Tumors in kidney fusion anomalies report of five cases and review of the literature. // Scand J Urol Nephrol. 2004. Vol. 38, N 6. P. 485-489.
- Kato M, Uchida J, Iwai T, Deguchi T, Nishihara C, Ninomiya N, Kawashima H, Nakatani T. Case of renal cell carcinoma in a horseshoe kidney. // Hinyokika Kiyo. 2008. Vol. 54, N 11. P. 723-725.







