Для хронического простатита (ХП), как и для большинства хронических заболеваний, типично рецидивирующее волнообразное течение с чередованием периодов ремиссий, характеризующихся ослаблением или исчезновением проявлений болезни, и обострений. При каждом обострении функциональное и морфолосостояние железы может ухудшаться, приводя к усилению прежних, или появлению новых симптомов, т.е. к прогрессированию болезни.
Особенно восприимчивой к воздействию факторов риска становится предстательная железа (ПЖ) в периоды сезонных обострений ХП, которые случаются, как правило, дважды в год, – осенью и в начале весны, и связаны со снижением общей сопротивляемости организма, ослаблением местного иммунитета, спазмом сосудов микроциркуляторного русла и гладкой мускулатуры.
Как среди пациентов, так и среди врачей бытует мнение о неизлечимости хронических болезней. И, действительно, вернуть орган в то состояние, в котором он пребывал до болезни, в большинстве случаев невозможно. Но врач и не должен ставить перед собой такой заведомо невыполнимой задачи. Цель лечения должна быть другой – прервать течение воспалительного процесса, восстановить, насколько это возможно, функцию органа, улучшить качество жизни пациента (устранить или уменьшить выраженность симптоматики) и удерживать эти позиции максимально долго, т.е. постараться вывести заболевание в максимально длительную ремиссию. И в этом существенную роль играют своевременно принимаемые меры профилактики, причем всех ее видов – от индивидуальной до общественной и от первичной до третичной.
Комплекс профилактических мероприятий при ХП включает изменение образа жизни (устранение факторов риска, в т.ч. сезонной гиподинамии, переохлаждений, отказ от алкогольных напитков, ограничение приема острой и другой раздражающей, а также жирной пищи, нормализацию работы кишечника – устранение запоров. Важными являются установление оптимального ритма и интенсивности сексуальной активности, отказ от применения прерванного полового акта и принудительной задержки семяизвержения с целью удлинения полового акта, от длительного сексуального возбуждения, не закончившегося оргазмом); предотвращение инфицирования половых путей (отказ от случайных или беспорядочных сексуальных особенно без применения средств контрацепции); нормализацию режима мочеиспускания); применение физкультуры; своевременное лечение очагов хронической инфекции (в первую очередь в органах мочеполовой системы, в полости рта, носои ротоглотке, а также кишечнике).
Для профилактики обострений ХП применяют много лекарственных препаратов и биологически активных добавок, имеющих целью укрепление общего и местного (мукозального) иммунитета, улучшение секреторной функции ПЖ, нормализацию кровообращения в органе, своевременную элиминацию патогенных и условно-патогенных микроорганизмов, устранение конгестивных явлений в органах малого таза в целом и предстательной железе, в частности.
Одним из препаратов, обладающих многоплановым органотропным действием на ПЖ, является Афала, представляющая собой антитела к ПСА. Влияние препарата основано на способности сверхмалых доз антител к эндогенным регуляторам (в т.ч. ПСА) изменять через систему естественных антител их (регуляторов) активность и характер действия.
ПСА служит эндогенным регулятором разнообразных процессов в мужском организме. Все функции этого вещества, продуцируемого ПЖ, возможно, еще не установлены. Основной его «задачей», как протеолитического фермента, является поддержание агрегатного состояния эякулята, т.е. его разжижение в результате расщепления семиногелина 1 и 2, и фибронектина. ПСА также принимает участие в расщеплении Lys-плазминогена до биологически активных фрагментов, антиангиогенная активность которых сопоставима с активностью ангиостатина. Помимо этого ПСА тормозит пролиферацию, миграцию и инвазию эндотелиальных клеток, блокирует действие ангиогенных факторов на эндотелий, а также стимулирует метаболические и пролиферативные процессы в эпителиальных клетках ПЖ посредством воздействия на белок, связывающий инсулиноподобный фактор роста [1].
Большой интерес вызывает роль ПСА в возникновении и поддержании воспалительного процесса при ХП. В нормальной ПЖ большая часть ПСА поступает в эякулят, разжижая его, и только 0,1% абсорбируется через базальную мембрану в кровь. При воспалительном процессе в результате действия медиаторов воспаления на ткани ПЖ нарушается барьерная функция простатических эпителиальных клеток, их базальной мембраны и базальной мембраны и эндотелия кровеносных сосудов [2]. Нарушение барьера между тканью ПЖ и сосудистым руслом приводит к повышению концентрации ПСА в сыворотке крови, характерному и для воспалительного процесса, и для злокачественного новообразования. Кроме того, ПСА выходит за пределы кровеносных сосудов и простатических ацинусов в ткань железы, где, являясь протеолитическим ферментом, усиливает процессы воспаления [3].
По данным Penne G. et al. концентрация интерлейкина-8 в спермальной плазме больных хроническим простатитом/симптомом хронической тазовой боли (СХТБ) прямо зависит от выраженности симптоматики и уровня ПСА, что свидетельствует об участие ПСА в развитии и поддержании воспалительного процесса [4].
Motrich RD et al. [5] показали, что преимущественно у больных хроническим неинфекционным простатитом выявляются высокие уровни ИНФ-гаммасекретирующих лимфоцитов, пролиферация которых происходит в ответ на собственные антигены ПЖ, такие как ПСА и ПАП (простатическая кислая протеаза). Кроме того, у этих пациентов был отмечен высокий уровень провоспалительных цитокинов (IL-1 и TNF-alpha) в семенной жидкости, что говорит о местном воспалении. Авторы предполагают, что ИНФ-гамма-секретирующие лимфоциты могут быть вовлечены в воспалительный процесс в ПЖ и, следовательно, могут менять свою биологическую функцию. Участие ПСА в воспалительном процесса подтверждается и другими авторами. На основании проведенного исследования Kodak et al. [6] пришли к выводу о том, что ПСА индуцирует провоспалительную реакцию, проявляющуюся в повышении секреции ИНФгамма из NK-клеток (клеток-киллеров). Свое действие ПСА оказывает не непосредственно, а стимулируя CD14-моноциты, которые секретирует активирующий NK-клетки.
Исходя из изложенных выше фактов, напрашивается гипотеза о том, что, регулируя активность ПСА, можно влиять на интенсивность воспалительного процесса в ПЖ.
Доклинические исследования препарата Афала подтвердили противовоспалительный эффект: у животных, которым давали с пищей препарат, были менее выражены признаки острого асептического воспаления ПЖ, а также дистрофические и склеротические изменения, как результат хронического воспалительного процесса. Выявлено увеличение под действием препарата концентрации ионов цинка в ткани ПЖ и улучшение ее функционального состояния [7].
ФАРМАКОЛОГИЧЕСКОЕ ДЕЙСТВИЕ
На основании анализа данных клинических исследований доказано, что Афала умеренно уменьшает выраженность асептического воспаления в органе и степень отека (что выражается в уменьшении объема ПЖ, дизурии, в т.ч. обструктивной и ирритативной симптоматики, боли и дискомфорта, вызванных простатитом), лейкоцитарную инфильтрацию, нормализует секреторную функцию (увеличивается количество лецитиновых зерен в секрете) [8, 9].
МАТЕРИАЛЫ И МЕТОДЫ
Чтобы подтвердить влияние препарата на течение воспалительного процесса в ПЖ, мы провели исследование эффективности препарата Афала в профилактике обострений у пациентов с хроническим абактериальным простатитом (влияние на частоту и степень выраженности обострений).
Исследуемая популяция состояла из 60 пациентов в возрасте от 18 лет и старше с ХП NIH IIIA в стадии ремиссии, т.е. с числом лейкоцитов в секрете ПЖ (СПЖ) при микроскопическом исследовании не более 10 в поле зрения (при 400 кратном увеличении) и количестве бактериальной флоры в постмассажной пормочи при бактериологическом исследовании менее 103 КОЕ/мл. Непременным условием включения пациента в исследование было отсутствие клинических проявлений заболевания (по результатам анкетирования).
На период исследования исключался прием лекарственных препаратов (кроме исследуемого), а также лечебных процедур, могущих повлиять на состояние нижних мочевых путей и органов мужской половой системы (альфа-адреноблокаторов, спазмолитиков, антибактериальных, холинергических и антихолинегрических средств, экстрактов растительного и животного происхождения для лечения заболеваний ПЖ, массажа ПЖ, физиотерапевтических методов и т.п.).
Перед включением в исследование пациентам проводили анкетирование с помощью опросника симптомов хронического простатита NIH-CPSI, забор секрета ПЖ для микроскопического и бактериологического исследований и исследование соскоба слизистой уретры на ИППП (Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum, Neisseria gonorrhoeae, Trichomonas vaginalis и Candida alb.) методом ПЦР с целью исключения инфекционного характера воспалительного процесса Обследование повторяли в сокращенном виде по истечении 30-дневного курса профилактики (заполнение опросника NIH-CPSI и микроскопическое исследование СПЖ) и через полтора месяца после окончания курса профилактики, т.е. в конце периода сезонного обострения. Такое обследование, как и профилактическая терапия, проводились дважды – весной и осенью (таблица 1).
Временные периоды сезонных обострений ХП были установлены путем анализа частоты обращений пациентов за амбулаторной помощью. Было выяснено, что наибольшее число обострений приходится на октябрь-ноябрь и март-апрель. Терапия, имеющая целью профилактику обострений ХП, должна предшествовать периодам обострений, поэтому курсы лечения проводили в начале осени (с середины сентября по середину октября) и в конце зимы – начале весны (с середины февраля по середину марта) (рис. 1).
Все пациенты, включенные в исследование, были разделены на две группы по 30 человек:
- Пациенты основной группы для профилактики обострения ХП получали препарат Афала по 2 таблетки 1 раз в сутки сублингвально в течение месяца в периоды, предшествующие времени наиболее частых сезонных обострений ХП.
- Пациенты контрольной группы (30 человек) не получали препаратов для профилактики обострения ХП.
Если с момента начала курса профилактики и до окончания периода сезонных обострений у пациента появлялись симптомы простатита, ему производили анкетирование с помощью анкеты NIH-CPSI и забор СПЖ вне графика для подтверждения (или опровержения) факта обострения ХП. Если обострение подтверждалось, пациенту назначали стандартную терапию, использующуюся для его лечения. После купирования обострения и нормализации количества лейкоцитов в СПЖ, пациентам вновь назначали препарат Афала по 2 таблетки 1 раз в сутки с целью профилактики. Таким образом, сезонные обострения суммировались с середины сентября до конца ноября (осенний период) и с середины февраля до конца апреля (весенний период).
Обострением ХП считали появление характерных симптомов на фоне активизации воспалительного процесса, подтвержденной данными микроскопического исследования секрета предстательной железы (число лейкоцитов более 10 в поле зрения).
Таблица 1. График сезонного обследования (февраль-март; сентябрь-октябрь)
| Дни | 1 | 8 | 38 | 83 |
|---|---|---|---|---|
| Визиты | 1 | 2 | 3 | 4 |
| Анамнез | + | |||
| Заполнение анкеты симптомов хронического простатита NIH-CPSI | + | + | + | |
| Микроскопическое исследование СПЖ | + | + | + | |
| Бактериологическое исследование СПЖ | + | |||
| Исследование на ИППП методом ПЦР | + | |||
| Включение пациента в исследование | + | |||
| Регистрация обострений ХП | + | + |
Рис. 1. Назначение препарата Афала перед сезонными обострениями ХП
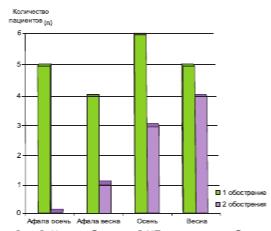
Рис. 2. Число обострений ХП у пациентов обеих групп в ходе исследования
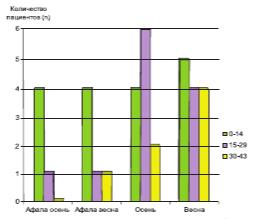
Рис. 3. Степень выраженности симптомов обострения ХП у пациентов обеих групп по шкале NIH-CPSI
Кроме числа обострений ХП, зафиксированных в эти периоды, подсчитывали число пациентов с повторными обострениями, а также выраженность симптоматики обострений по шкале NIH-CPSI: от 0 до14 баллов – маловыраженная симптоматика, 15-29 – умеренная симптоматика и от 30 до 43 – выраженная симптоматика.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
За весь период исследования обострения развились у 10 пациентов (33,3%), принимавших с профилактической целью препарат Афала и у 18 пациентов (60%) из контрольной группы (рис.2).
Всего зарегистрировано 11 обострений в основной группе и 24 обострения в контрольной. При этом в первой группе у 9 пациентов развилось по одному обострению и только у одного пациента (3,3% всех пациентов этой группы) обострение возникло дважды. Среди 30 пациентов, которым не проводилась медикаментозная профилактика ХП, в 11 случаях развилось по 1 обострению и в 7 случаях – по 2 обострения.
Обращает на себя внимание и разная выраженность обострений у пациентов двух групп (рис.3). В основной группе в большинстве случаев (у 8 пациентов) симптомы были незначительно выраженными (0-14 баллов), а у двух – умеренно выраженными (15-29 баллов). И только у одного пациента, которому проводили профилактику обострений препаратом Афала, были зарегистрированы выраженные симптомы (30-43 балла). В контрольной группе картина иная: большая часть обострений (у 10 пациентов) сопровождалась умеренно выраженной симптоматикой (15-29 баллов), а у 6 больных боли, нарушение мочеиспускания и снижение качества жизни носили максимально выраженный характер (30-43 балла).
Таким образом, за период исследования обострения воспалительного процесса развились у меньшего количества пациентов, принимавших препарат Афала по сравнению с контрольной группой. В основной группе также было в семь раз меньше пациентов, имевших повторные обострения – 2,5% (1 пациент) по сравнению с группой плацебо – 17,5% (7 пациентов).
ЗАКЛЮЧЕНИЕ
Настоящее клиническое исследование показало, что применение препарата Афала с целью профилактики обострений воспалительного процесса в ПЖ почти в 2 раза уменьшает вероятность развития обострений ХП. За время наблюдения в основной группе обострения развились у 10 пациентов (33,3%) и у 18 пациентов контрольной группы (60,0%) и вероятность развития повторных обострений у одного и того же пациента (повторные обострения наблюдались у 1 пациента основной группы и у 7 пациентов, которым профилактика не проводилась).
Прием препарата Афала уменьшает выраженность обострений хронического простатита, в первую очередь боли (дискомфорта): у большинства пациентов основной группы была зарегистрирована незначительная симптоматика (0-14 баллов) по шкале NIH-CPSI и только у одного обострение заболевания носило выраженный характер. В контрольной группе большая часть обострений (10 случаев) сопровождались умеренно выраженными симптомами (15-29 баллов), а у 6 пациентов симптоматика ХП и снижение качества жизни были выражены максимально (30-43 балла).
ВЫВОДЫ
1. Учитывая влияние препарата Афала на симптоматику ХП (в первую очередь боли и воспаление), он может применяться с профилактической целью для уменьшения числа обострений заболевания, а также степени их выраженности.
2. Препарат Афала хорошо переносится пациентами и не вызывает побочных явлений.
ЛИТЕРАТУРА
1. Breul J, Pickl U, Hartung R. Prostate-specific antigen in urine. // Eur Urol. 1994. Vol. 26. P. 18-21.
2. Ellis WJ. Prostate specific antigen density versus prostate specific antigen slope as predictors of prostate cancer in men with initially negative prostatic biopsies //J Urol. 1996. Vol. 156. P. 431.
3. Шангичев А.В. Состояние ферментной антиоксидантной системы крови, секрета простаты и эякулята при стандартном лечении хронического абактериального простатита. // Научные журналы РУДН, Медицина, №3, 2009.
4. Penna G, Mondaini N, Amuchastegui S, Degli Innocenti S, Carini M, Giubilei G, Fibbi B, Colli E, Maggi M, Adorini L. Seminal plasma Cctokines and chemokines in prostate inflammation: interleukin 8 as a predictive biomarker in chronic prostatitis/chronic pelvic pain syndrome and benign prostatic hyperplasia. // Eur Urol. 2007. Vol. 51. P. 524-533.
5. Motrich RD, Maccioni M, Molina R, Tissera A, Olmedo J, Riera CM, Rivero VE. Presence of INFgamma-secreting lymphocytes specific to prostate antigens in a group of chronic prostatitis patients. // Clin Immunol. 2005. Vol. 116, N 2. P. 149-157
6. Kodak JA, Mann DL, Klyushnenkova EN, Alexander RB. Activation of innate immunity by prostate specific antigen (PSA). // Prostate. 2006. Vol. 66, N 15. P. 1592-1599
7. Боровская Т.Г., Фомина Т.И., Лоскутова О.П., Баранова О.В., Сергеева С.А., Мартюшев А.В., Эпштейн О.И. Антитела к простатоспецифическому антигену в сверхмалых дозах: влияние на морфологическое и функциональное состояние предстательной железы крыс // Бюлл. эксп. биол. мед. 2002. Прил. 4. С.104-106.
8. Кульчавеня Е.В. Эффективность Афалы в комплексном лечении больных хроническим простатитом // Врачебное сословие. 2007. №5 . C.20-25.
9. Ткачук В.Н. Лечение больных хроническим абактериальным простатитом. // Лечащий врач. 2008. №1. C.2-3.







