ВВЕДЕНИЕ
Хронический простатит (ХП) – заболевание, диагностируемое клинически на основании признаков воспаления предстательной железы (ПЖ), симптомы которого сохраняются >3 месяцев [1].
По данным ВОЗ в США ежегодно около 3 миллионов мужчин трудоспособного возраста заболевает ХП[2]. В России, по данным проведенных исследований, ХП страдает от 8 до 35% мужчин в возрасте 20-40 лет, а в мире, согласно последним эпидемиологическим данным, ХП встречается у 2,5-16,0% мужчин [3-5].
Проблема ХП остается актуальной, так как основными проявлениями заболевания являются симптомы нарушения функции нижних мочевых путей (СНМП), значительно ухудшающие качество жизни у пациентов трудоспособного возраста. Число мужчин с СНМП растет и по данным многочисленных исследований колеблется от 40-90% [6].
Основным патогенетическим механизмом, обуславливающим ирритативную и обструктивную симптоматику, является отек ПЖ и влияние имеющегося воспаления на альфа-адренорецепторы, расположенные в шейке мочевого пузыря [7].
В 1995 году Американский национальный институт здоровья (NIH) и Национальный институт диабета, пищеварения и болезней почек (NIDDK) предложили классификацию, в которой простатит классифицируется в зависимости от наличия клинических проявлений, наличия в секрете ПЖ бактерий и лейкоцитов.
- I категория – острый бактериальный простатит;
- II категория – хронический бактериальный простатит;
- III A категория – воспалительный синдром хронической тазовой боли (СХТБ);
- III B – категория – невоспалительный СХТБ;
- IV категория – бессимптомный простатит. Эта классификация в настоящее время широко используется при диагностике и лечении больных с ХП [8-12].
Часто стандартная терапия не приводит к значимому улучшению состояния пациентов, в связи с чем применяются биостимуляторы, экстракты различных растений и насекомых, а также их биологические компоненты [13].
Цель исследования. Оценить эффективность и безопасность применения препарата Аденопросин® у пациентов с ХП/CХТБ IIIА категории по классификации Национального института здоровья США.
МАТЕРИАЛЫ И МЕТОДЫ
С 10.2021 г. по 10.2022 г. на базе Центра урологии и андрологии ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России было проведено проспективное наблюдательное исследование эффективности и безопасности препарата Аденопросин® в качестве дополнения к стандартной терапии.
В исследовании приняли участие 60 пациентов мужского пола в возрасте от 35 до 60 лет (средний возраст 42,3 года) с установленным диагнозом ХП (IIIА по классификации Национального института здоровья США) и преобладанием фенотипов U (Urinary) и O (Organ-centric)по классификации UPOINTS.
Критерии включения и невключения больных в исследование представлены в таблице 1.
Таблица 1. Критерии включения/невключения
Table 1. Inclusion/non-inclusion criteria
|
Критерии включения |
Пациенты мужского пола в возрасте от 35 до 60 лет с установленным диагнозом ХП (IIIА по классификации Национального института здоровья США), с баллами по опросникам IPSS > 7 и NIH-CPSI > 14, подписавшие информированное добровольное согласие на исследование. |
|---|---|
| Критерии невключения Exclusion Criteria |
|
Все участники исследовании были проинформированы о целях, методах исследования, ожидаемой пользе, сопряженном риске и дали письменное согласие на участие в исследовании.
После получения результатов скрининга пациенты случайным образом были разделены на 2 сопоставимые группы. В контрольной группе лечение проводилось согласно рекомендациям Европейской ассоциации урологов и начиналось с первого визита: терапия альфа-адреноблокатором (Тамсулозин 0,4мг по 1капс. утром – 1 месяц), антибактериальным препаратом (Левофлоксацин 500мг по 1табл. 1р/д – 1 месяц) [12]. В основной группе лечение также начиналось на первом визите, но помимо антибактериального препарата, альфа-адреноблокатора в стандартных дозировках проводилось лечение препаратом Аденопросин® по 1 суппозиторию 1р/д ректально – 1 месяц. Активное вещество, входящее в состав препарата Аденопросин®, представляет собой биомассу, полученную из личинок насекомых вида Непарный шелкопряд (Lymantria dispar), которая оказывает противовоспалительное и антиоксидантное действие. Исследование проводилось в течение 3 месяцев (1 месяц лечения, 2 месяца наблюдения) и включало в себя 4 посещения лечебного учреждения. Процедуры проводимые во время визитов включали в себя: подписание информированного согласия, оценку критериев включения/невключения на основании сбора жалоб, анамнеза заболевания и жизни, объективного осмотра, локального статуса (пальцевое ректальное исследование ПЖ) лабораторно-инструментального обследования, проведенного заранее (биохимический анализ крови, PSA крови общий, трансректальное ультразвуковое исследование ПЖ (ТРУЗИ ПЖ), урофлоуметрия), заполнения опросников IPSS, NIH-CPSI, световой микроскопии секрета ПЖ. Патологическое количество лейкоцитов при световой микроскопии секрета ПЖ оценивалось как > 12 лейкоцитов в поле зрения. Подробные данные о процедурах на визитах исследования представлены в таблице 2.
Таблица 2. График визитов
Table 2. Schedule of visits
|
Процедуры |
Визит 0 – 1 скрининг/ начало терапии |
Визит 2 – через 14 дней от начала терапии |
Визит 3 – 30-е сутки, окончание терапии |
Визит 4 – 90-е сутки |
|---|---|---|---|---|
|
ТРУЗИ предстательной железы |
+ |
|
|
|
|
Определение PSA крови, Биохимический анализ крови; скрининг на ВИЧ, HBsAg, HCV, RW; |
+ |
|
|
|
|
Пальцевое ректальное исследование предстательной железы |
+ |
+ |
+ |
+ |
|
Подписание информированного согласия |
+ |
|
|
|
|
Оценка критериев включения/невключения |
+ |
|
|
|
|
Заполнение шкалы IPSS / |
+ |
+ |
+ |
+ |
|
Заполнение шкалы NIH-CPSI/ |
+ |
+ |
+ |
+ |
|
Заполнение опросника IIEF-5 / |
+ |
+ |
+ |
+ |
|
Анализ секрета предстательной железы |
+ |
+ |
+ |
+ |
|
Оценка нежелательных явлений |
|
+ |
+ |
+ |
Результаты исследования были подвергнуты статистическому анализу с использованием программы IBM SPSS Statistics v.26. Определение значимости статистических различий проводилось при помощи t-критерия Стьюдента. Накопление, корректировку, систематизацию исходной информации осуществляли в электронных таблицах Microsoft Excel.
РЕЗУЛЬТАТЫ
Группы были сопоставимы по возрасту: средний возраст в первой группе составил 41,2 года (от 35 до 60 лет) во второй – 42,3 года (от 36 до 59 лет). По данным ТРУЗИ ПЖ, которое проводилось только на скрининговом визите в целях исключения дизурии, не связанной с ХП, иной патологии выявлено не было. При проведении пальцевого ректального исследования ПЖ до начала терапии у всех пациентов отмечалась болезненность при пальпации. При оценке тонуса ПЖ последний был изменен у 36 (60%) пациентов: повышение тонуса отмечалось у 20 (33,3%), пастозность у 16 (26,7%) пациентов. На 4-м визите при оценке тонуса ПЖ у всех пациентов отмечалась нормализация консистенции (отсутствие пастозности или повышения тонуса). Незначительная болезненность при пальпации ПЖ сохранялась у 3 (5%) пациентов из контрольной группы, все пациенты из основной группы отмечали купирование болевого синдрома при пальпации. В оцениваемых показателях опросников, а также количества лейкоцитов в микроскопии секрета ПЖ, различия в группах до лечения были статистически незначимы: показатели опросника NIH-CPSI общий балл (p=0,4769); NIH-CPSI домен «Качество жизни» (p=0,4823); опросник IPSS (p=0,7927), шкала IIEF-5 (p=0,6391), количество лейкоцитов при микроскопии секрета ПЖ (p=0,5143).
По данным опросника NIH-CPSI до лечения у всех пациентов наблюдалась умеренная и тяжелая симптоматика. Средний общий балл до начала терапии в контрольной группе составил 21,4 балла, в основной – 20,7 баллов. В домене «Качество жизни» средний балл в контрольной и основной группе до лечения составил 5,2 и 5 баллов соответственно. При сравнительном анализе результатов до и после лечения в контрольной и основной группе по данным опросника NIH-CPSI было отмечено, что в группе пациентов, получавших Аденопросин®, через 90 дней от начала терапии среднее общее количество баллов оказалось статистически ниже, чем при проведении стандартной терапии (p=0,0201). Динамика выраженности симптомов по шкале NIH-CPSI на визитах (общий балл, количество баллов в домене «Качество жизни») представлены на рисунках 1 и 2.
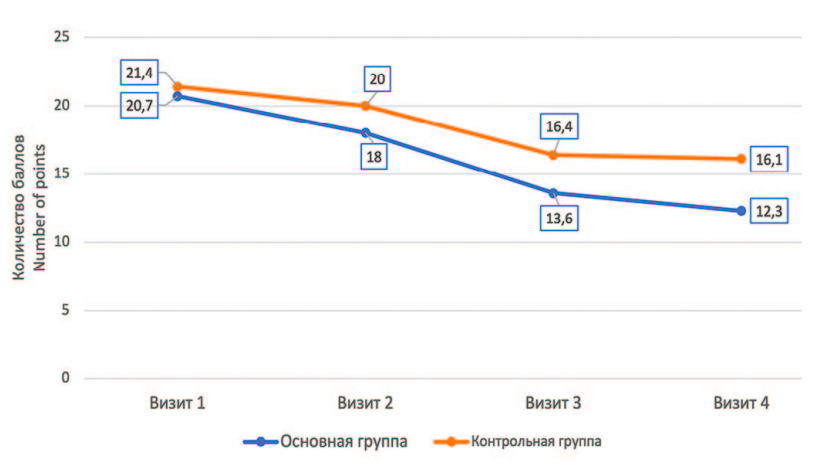
Рис. 1. Динамика выраженности симптомов по шкале NIH-CPSI (общий балл)
Fig. 1. Dynamics of symptoms severity according to the NIH-CPSI scale (total score)
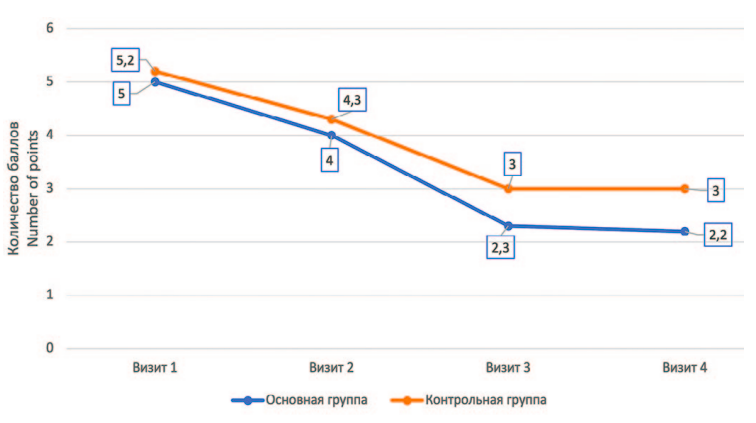
Рис. 2. Динамика выраженности симптомов по шкале NIH-CPSI (домен «Качество жизни»)
Fig. 2. Dynamics of symptoms severity according to the NIH-CPSI scale
(Quality of Life domain)
По данным опросника IPSS до начала терапии у 36 (60%) пациентов наблюдалась умеренно выраженная симптоматика, 24 (40%) составили пациенты с нарушением мочеиспускания тяжелой степени. Средний балл до начала терапии в контрольной и основной группе составил 17,9 и 17,7 соответственно. На рисунке 3 представлена динамика выраженности симптомов, которая показывает, что терапия в обеих группах была эффективна, при сравнительной оценке показателей в группах до и после лечения различия были статистически значимы (p<0,05). В основной группе наблюдалась более выраженная положительная динамика на всех контрольных точках, уменьшение среднего количества баллов составило 9,8 баллов, против 6 баллов в контрольной группе. Через 90 дней удалось достичь статистически значимого различия в пользу основной группы (p=0,0267).
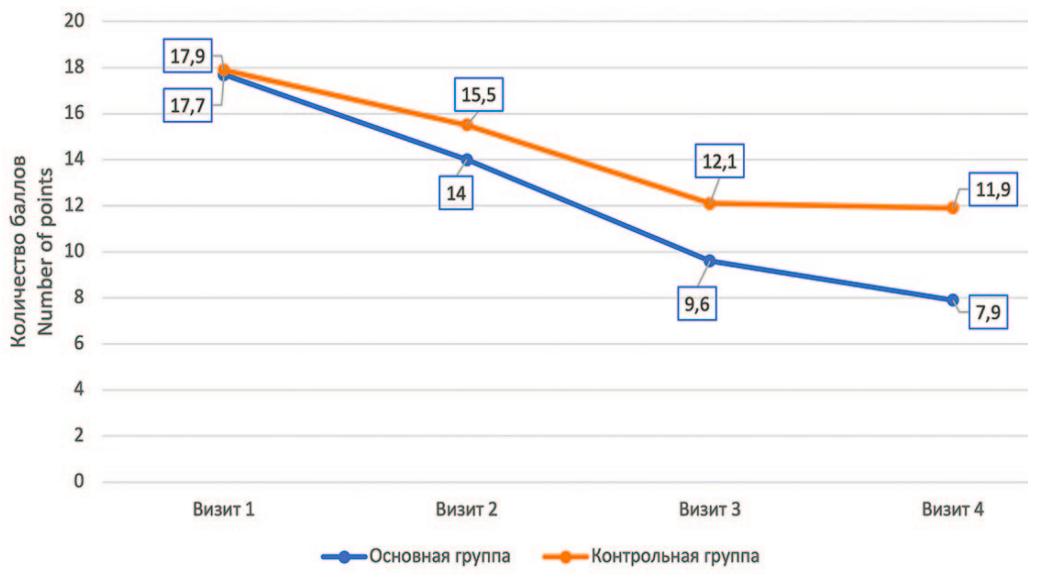
Рис. 3. Динамика выраженности симптомов по данным опросника IPSS
Fig. 3. Dynamics of symptoms severity according to the IPSS questionnaire
Уже на 14-й день от начала терапии отмечалось снижение уровня лейкоцитов в среднем на 6,1 и 7,6 баллов в контрольной и основной группе соответственно. На 30-й день терапии отмечалась нормализация количества лейкоцитов в секрете предстательной железы. При сравнении основной и контрольной группы до и после лечения терапия оказалось достоверно эффективной в обеих группах (p<0,05). Через 90 дней после начала терапии (4-й визит) в группе с добавлением к стандартной терапии препарата Аденопросин® отмечено более выраженное снижение числа лейкоцитов (p=0,0213) (рис. 4).
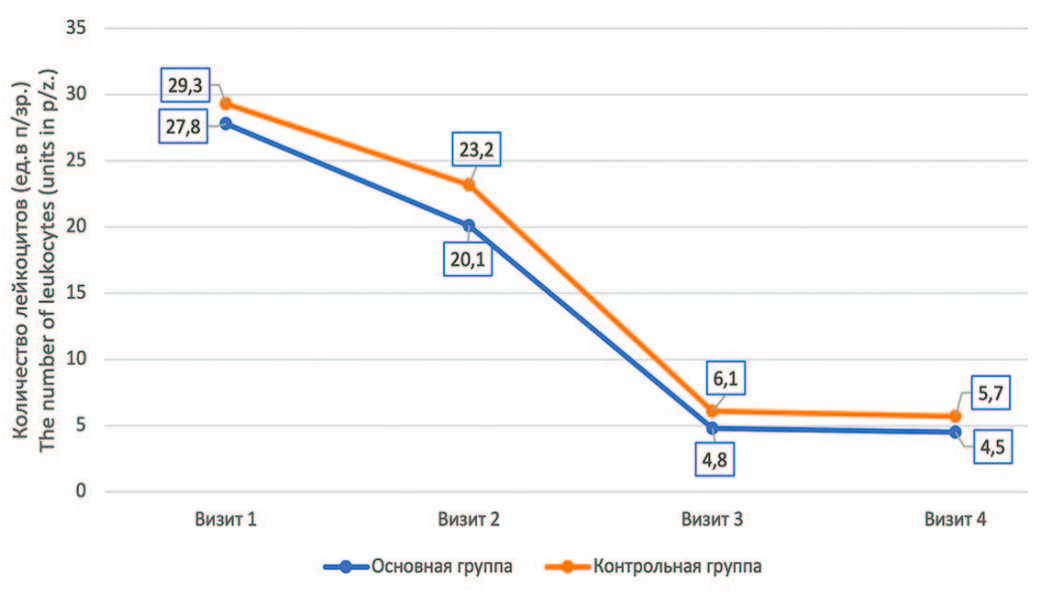
Рис. 4. Динамика количества уровня лейкоцитов в секрете ПЖ
Fig. 4. Dynamics of the number of leukocytes in the secretion of the prostate gland
При проведении урофлоуметрии средняя максимальная скорость потока мочи (Qmax) в контрольной и основной группе до начала терапии составила 11,9 мл/с и 11,1 мл/с соответственно (p>0,05). При статистическом межгрупповом анализе показателей на 4-м визите (60-е сутки после окончания терапии) в обеих группах отмечалась положительная динамика в виде увеличения показателя Qmax, которое в контрольной группе составило 2,7 мл/с, в основной 6,3 мл/с (p=0,0356) (рис. 5).
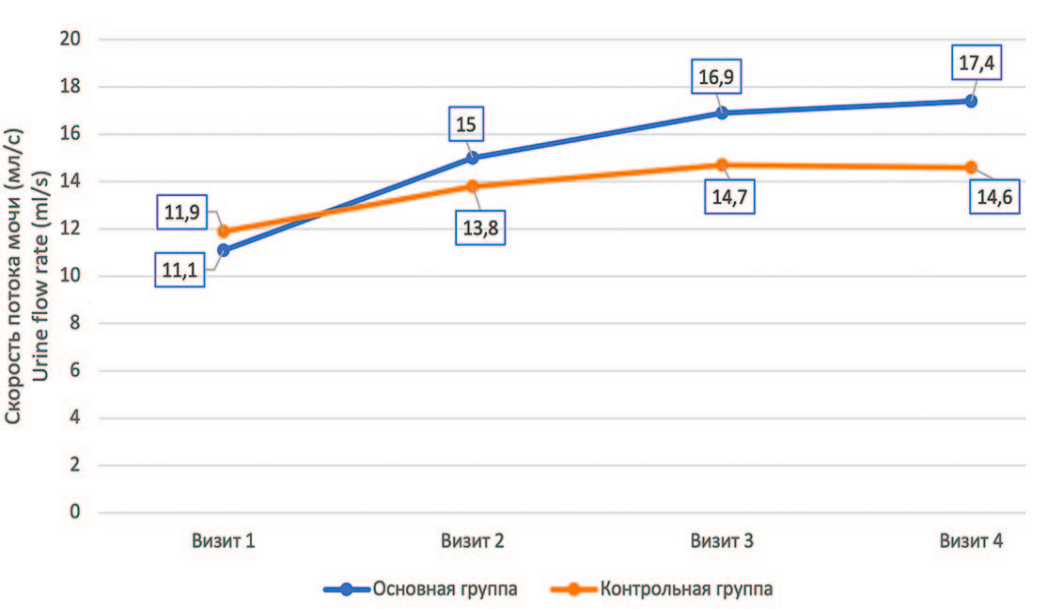
Рис. 5. Динамика максимальной объемной скорости потока мочи Qmax
Fig. 5. Dynamics of the maximum volumetric flow rate of urine Qmax
Нежелательных явлений при применении препарата Аденопросин® не отмечено ни у одного пациента.
ОБСУЖДЕНИЕ
В настоящее время лечение ХП/СХТБ следует рассматривать комплексно с учетом множества этиологических факторов, что требует мультимодального подхода [14]. В связи с этим широкое применение получила классификация ХП/СХТБ – UPOINTS [15]. Согласно данной классификации тазовая боль разделена на 7 доменов и может быть обусловлена нарушением уродинамики (Urinary), психосоциальными (Psychosocial), органоспецифическими (Organ specific), инфекционными (Infections), неврологическими нарушениями (Neurologic), болезненностью скелетных мышц тазового дна (Tenderness of skeletal muscles) и сексуальными расстройствами (Sexual) [16]. Важность данной классификации обусловлена возможностью построения необходимого диагностического алгоритма и плана лечения, позволяющего достичь длительной ремиссии заболевания.
Для ХП/СХТБ IIIА категории характерно лабораторно выявленное повышение количества лейкоцитов в секрете ПЖ при стерильном микробиологическом посеве. Однако даже у данной группы пациентов антибактериальная терапия показывает положительный эффект. По данным В.А. Божедомова и соавт., курс антибактериальной терапии длительностью 2-4 недели приводит к уменьшению количества лейкоцитов в секрете ПЖ у половины пациентов, что свидетельствует о необходимости назначения антибиотиков при кажущемся «стерильном» микробиологическом посеве и участии в воспалении патогенов, не выявляемых при стандартном исследовании [17]. Некоторые авторы связывают это с наличием бактерий, не выявляемых в стандартном посеве, таких как С. Trachomatis, M. Species и U. Urealyticum [18-20].
По данным всех стандартизированных опросников, включенных в исследование, данных микроскопии секрета ПЖ и урофлоуметрии, препарат Аденопросин® показал более выраженную положительную динамику и привел к значимому улучшению качества жизни пациентов, даже при наличии тяжелой клинической симптоматики. Стоит отметить, что в основной группе положительная динамика показателей сохранялась после окончания терапии, что обусловлено механизмом действия препарата Аденопросин®. За счет действия биологически активных компонентов препарата происходит уменьшение образования A2-фосфолипазы, высвобождения арахидоновой кислоты со снижением синтеза простагландинов и лейкотриенов, снижается проницаемость капилляров, уменьшается отек ПЖ. Также препарат действует на гладкомышечную ткань детрузора, снижая его тонус, что в совокупности приводит к улучшению мочеиспускания, купированию болевого синдрома и улучшению качества жизни пациентов.
ЗАКЛЮЧЕНИЕ
Результаты проведенного исследования демонстрируют, что препарат Аденопросин® является эффективным и безопасным. Препарат обладает выраженным противовоспалительным действием у пациентов с ХП. За время исследования не наблюдались какие-либо нежелательные явления, связанные с применением препарата Аденопросин®. Препарат может быть рекомендован пациентам в рамках комплексной терапии ХП/СХТБ, так как достоверно приводит к значимому улучшению мочеиспускания и купированию болевого синдрома.
ЛИТЕРАТУРА
1. Урология. От симптомов к диагнозу и лечению. Иллюстрированное руководство: учеб. пособие. Под ред. Глыбочко П.В., Аляева Ю.Г., Григорьева Н.А.; М.: ГЭОТАР-Медиа 2014;148 с. [Urology. From symptoms to diagnosis and treatment. Illustrated guide: studies. stipend. Ed. Glybochko P.V., Alyaev Yu.G., Grigoriev N.A.; M.: GEOTAR-Media 2014;148 p. (in Russian)].
2. Жуков О.Б., Евдокимов В.В., Брагина Е.Е. Улучшение качества жизни и морфофункицональных характеристик сперматозоидов у мужчин с хроническим абактериальным простатитом и программы прегравидарной подготовки к отцовству. Андрология и генитальная хирургия 2017;18(1):102-108. [Zhukov O.B., Evdokimov V.V., Bragina E.E. Improving the quality of life and morphofunctional characteristics of spermatozoa in men with chronic abacterial prostatitis and programs of pre-gravidar preparation for fatherhood. Andrologiya i genital'naya khirurgiya = Andrology and genital Surgery 2017;18(1):102-108. (in Russian)]. https://doi.org/10.17650/2070-9781-2017-18-1-102-108.
3. Perletti G, Marras E, Wagenlehner FME, Magri V. Antimicrobial therapy for chronic bacterial prostatitis. Cochrane Database of Systematic Reviews 2013, Issue 8. Art. No.: CD009071. http://doi.org/10.1002/14651858.CD009071.pub2.
4. Крупин В.Н., Крупин А.В., Белова А.Н. Патогенетическое лечение больных хроническим бактериальным простатитом с сопутствующей неврологической патологией: наш опыт. Урологические ведомости 2018;8(3):36-43. [Krupin V.N., Krupin A.V., Belova A.N. Pathogenetic treatment of patients with chronic bacterial prostatitis with concomitant neurological pathology: our experience. Urologicheskiye vedomosti = Urological Bulletin 2018;8(3):36-43. (in Russian)]. http://doi.org/10.17816/uroved8336-43.
5. Шорманов И.С. Клиническая и микробиологическая эффективность фаготерапии в лечении хронического бактериального простатита. Шорманов И.С., Соловьев А.С. Известия высших учебных заведений. Поволжский регион. Медицинские науки 2016;3(39):69-77. [Shormanov I.S. Clinical and microbiological efficacy of phage therapy in the treatment of chronic bacterial prostatitis. Shormanov I.S., Soloviev A.S. News of higher educational institutions. Volga region. Meditsinskiye nauki = Medical Sciences 2016;3(39):69-77. (in Russian)].
6. Виноградов И.В., Живулько А.Р., Королев С.В. Хронический простатит, патогенетические механизмы влияния на мужскую фертильность. Вестник последипломного медицинского образования 2018;(4):48–54. [Vinogradov I.V., Zhivulko A.R., Korolev S.V. Chronic prostatitis, pathogenetic mechanisms of influence on male fertility. Vestnik poslediplomnogo meditsinskogo obrazovaniya = Journal of Postgraduate Medical education 2018;(4):48–54. (in Russian)].
7. Wagenlehner FM, van Till JW, Magri V, Perletti G, Houbiers JG, Weidner W, et al. Chronic Prostatitis Symptom Index (NIH-CPSI) symptom evaluation in multinational cohorts of patients with chronic prostatitis/chronic pelvic pain syndrome. Eur Urol 2013;63(5):953–59. https://doi.org/10.1016/j. eururo.2012.10.042.
8. Аляев Ю.Г. Урология. Российские клинические рекомендации. Под ред. Аляева Ю.Г., Глыбочко П.В., Пушкаря Д.Ю. М.: ГЭОТАР-Медиа 2015; 480 с. [Alyaev Yu.G. Urology. Russian clinical guidelines. Ed. Alyaev Yu.G., Glybochko P.V., Pushkary D.Yu. Moscow: GEOTAR-Media 2015; 480 p. (in Russian)].
9. Rees J, Abrahams M, Doble A, Cooper A; Prostatitis Expert Reference Group (PERG). Diagnosis and treatment of chronic bacterial prostatitis and chronic prostatitis/chronic pelvic pain syndrome: a consensus guideline. BJU Int 2015;116(4):509-25. http://doi.org/10.1111/bju.13101.
10. Anothaisintawee T, Attia J, Nickel JC, Thammakraisorn S, Numthavaj P, McEvoy M, Thakkinstian A. Management of chronic prostatitis/chronic pelvic pain syndrome: a systematic review and network meta-analysis. JAMA 2011;305(1):78-86. http://doi.org/10.1001/jama.2010.1913.
11. Krieger JN, Lee SW, Jeon J, Cheah PY, Liong ML, Riley DE. Epidemiology of prostatitis. Int J Antimicrob Agents 2008;31 Suppl 1(Suppl 1):S85-90. http://doi.org/10.1016/ j.ijantimicag.2007.08.028.
12. Engeler D, Baranowski AP, Berghmans B, Birch J, Borovicka J, et al. EAU guidelines on chronic pelvic pain. (Limited text update March 2022). URL: https://uroweb.org/ guidelines/chronic-pelvic-pain.
13. Карпов Е.И. Современный взгляд на лечение синдрома нижних мочевыводящих путей: цитомедины как класс лекарственных препаратов. РМЖ 2017;25(27):1992–6. [Karpov E.I. Modern view on the treatment of lower urinary tract syndrome: cytomedines as a class of drugs. RMJ 2017;25(27):1992-6. (in Russian)].
14. Крючкова М.Н., Солдаткин В.А. Синдром хронической тазовой боли: психопатологические аспекты. Вестник урологии 2017;5(1):52-63. [Kryuchkova M.N., Soldatkin V.A. Chronic pelvic pain syndrome: psychopathological aspects. Vestnik urologii = Bulletin of Urology 2017;5(1):52-63. (in Russian)]. https://doi.org/10.21886/2308-6424-2017-5-1-52-63.
15. Magri V, Marras E, Restelli A, Wagenlehner FM, Perletti G. Multimodal therapy for category III chronic prostatitis/chronic pelvic pain syndrome in UPOINTS phenotyped patients. Exp Ther Med 2015;9(3):658-666. http://doi.org/10.3892/ etm.2014.2152. Epub 2014 Dec 19. PMID: 25667610; PMCID: PMC4316954.
16. Ахмеджанова Л.Т., Баринов А.Н., Леонтьева М.С. и Мандра Е.В. Диагностика и лечение синдрома хронической тазовой боли. Неврология, нейропсихиатрия, психосоматика 2022;14(4):54-61. [Akhmedzhanova L.T., Barinov A.N., Leontieva M.S. and Mandra E.V. Diagnosis and treatment of chronic pelvic pain syndrome. Nevrologiya, neyropsikhiatriya, psikhosomatika = Neurology, Neuropsychiatry, Psychosomatics 2022;14(4):54-61. (in Russian)].
17. Божедомов В.А. Современные возможности лечения хронического простатита. Андрология и генитальная хирургия 2016;17(3):10-22. [Bozhedomov V.A. Modern possibilities of treatment of chronic prostatitis. Andrologiya i genital'naya khirurgiya = Andrology and Genital Surgery 2016;17(3):10-22. (in Russian)]. https://doi.org/10.17650/2070-9781-2016-17-3-10-22.
18. Choi YS, Kim KS, Choi SW, Kim S, Bae WJ, Cho HJ, Hong SH, Kim SW, Hwang TK, Lee JY. Microbiological etiology of bacterial prostatitis in general hospital and primary care clinic in Korea. Prostate Int 2013;1(3):133-8. http://doi.org/10.12954/PI.13023.
19. Chen X, Hu C, Peng Y, Lu J, Yang NQ, Chen L, Zhang GQ, Tang LK, Dai JC. Association of diet and lifestyle with chronic prostatitis/chronic pelvic pain syndrome and pain severity: a case-control study. Prostate Cancer Prostatic Dis 2016;19(1):92-9. http://doi.org/10.1038/pcan.2015.57.
20. Park H, Sim SM, Lee G. The presence of Chlamydia is associated with increased leukocyte counts and pain severity in men with chronic pelvic pain syndrome. Urology 2015;85(3):574-9. http://doi.org/10.1016/j.urology.2014.11.008.







