ВВЕДЕНИЕ
Хронический пиелонефрит – одно из самых частых заболевание почек. Критерием рецидивирующего характера пиелонефрита является развитие трех обострений в течение 12 месяцев или двух обострений в течение 6 месяцев. Часто хронический пиелонефрит является следствием неадекватного или неполного лечения острого пиелонефрита и имеет те же факторы риска и схожий патогенез. Наиболее типичными факторами риска хронического пиелонефрита являются структурные аномалии мочевыводящих путей и рефлюкс-нефропатия [1].
Одним из распространенных осложнений хронического пиелонефрита является образование рубцов в ткани почек с последующим возможным развитием хронической почечной недостаточности [2].
С учетом хронического характера инфекции немаловажным аспектом лечения рецидивирующих неосложненных инфекций верхних мочевых путей является антибиотикорезистентность. Данная проблема актуальна и для России. Врачи не всегда следуют рекомендациям и не назначают препараты первой линии. Более того, вместо этого нередки случаи применения тех антибактериальных средств, которые исключены из рекомендаций [3].
Очевидно, что терапия острого и обострений хронического пиелонефрита должна быть в первую очередь патогенетически обоснованной. При этом необходимо принимать во внимание, что каждое последующее обострение хронического пиелонефрита может приводить к ухудшению функции почек, дальнейшему прогрессированию почечной недостаточности, к развитию антибиотикорезистентности и к побочным эффектам антибактериальной терапии [4, 5]. Проблемы комплаентности заставляют искать безопасные и эффективные режимы длительной профилактики рецидивов хронического пиелонефрита.
Цель данной работы – изучение эффективности и безопасности биологически активной добавки «Нефробак»®, капсулы, (ООО «ЭСЭЙЧ ФАРМА», Россия) при применении у пациентов с обострением хронического пиелонефрита в условиях реальной клинической практики.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование было включено 60 пациенток в возрасте от 24 до 56 лет включительно, обратившихся к врачу-урологу с жалобами на боль в поясничной области, повышение температуры тела, дизурию. Пациенткам на основании обследования, проведенного в соответствии с действующими рекомендациями, был установлен диагноз хронический пиелонефрит. Критерием постановки диагноза хронического пиелонефрита служило наличие двух обострений в течение полугода или трех – в течение года. Из исследования исключали мужчин, пациенток с конкрементами или инородными телами (стенты, катетеры) в мочевых путях, декомпенсированным сахарным диабетом, нарушениями мочеиспускания в анамнезе (гиперактивный мочевой пузырь и др.), наличием у пациентки заболеваний, передающихся половым путем, а также случаи требующие госпитализации. Реальная клиническая практика подразумевала, что все пациентки при диагностике хронического пиелонефрита будут получать антибактериальную терапию в соответствии с действующими клиническими рекомендациями. При этом пациентки рандомизированы в две группы. Первая группа получала только антибиотикотерапию (АБ), вторая группа – антибиотикотерапию в комбинации с биологически активным комплексом «Нефробак»® по 1 капсуле 2 раза в день в течение 1 месяца. Обе группы наблюдались в течение 6 месяцев с начала терапии.Для изучения терапевтического эффекта проводились:
- оценка динамики выраженности симптомов острого пиелонефрита на основании опроса пациентки;
- оценка динамики параметров общего анализа мочи и посева мочи (изменение уровня лейкоцитов, эритроцитов, нитритов, белка, в общем анализе мочи и уровня микробной нагрузки по результатам посева мочи, а также резистентности выявленных микроорганизмов к антибиотикам);
- оценка динамики патологических изменений паренхимы почек по результатам ультразвукового исследования (УЗИ) почек и верхних мочевых путей.
Эффект оценивался как выраженный, хороший, удовлетворительный, неудовлетворительный в зависимости от наличия/отсутствия динамики обострений пиелонефрита в сочетании с лабораторными и инструментальными данными.
Выраженный эффект характеризовался отсутствием обострений хронического пиелонефрита в период наблюдения при исчезновении патогенных микроорганизмов по результатам посева мочи и нормализации УЗ картины почек; хороший эффект – уменьшением титра патогенных микроорганизмов по результатам посева мочи и/или уменьшением уровня лейкоцитов, нитритов в моче при отсутствии признаков воспаления по УЗИ; удовлетворительный эффект – уменьшением степени бактериурии или уменьшением выраженности воспаления по результатам общего анализа мочи неудовлетворительный эффект – отсутствием положительной динамики или ухудшением состояния пациента.
РЕЗУЛЬТАТЫ
Шестьдесят пациенток было исходно включено в исследуемую когорту. По причинам, не связанным с эффективностью и безопасностью терапии 3 пациентки выбыли из исследования (lost for follow-up). Результаты данных пациенток не учитывались в общем анализе.
Полностью завершили исследование 57 пациентов: 28 – в первой группе и 29 – во второй группе. Всем пациенткам на скрининге и на контрольных визитах выполнялся бактериологический анализ мочи и у всех на первичном визите были выявлены те или иные патогены. Структура уропатогенов, выявленных на скрининге представлены в таблице 1.
Таблица 1. Результаты бактериологического анализа мочи
Table 1. Results of bacteriological analysis of urine
|
Выявленный патоген Identified pathogen |
Число пациенток, n (%) Number of patients, n (%) |
|---|---|
|
Escherichia coli |
46 (81) |
|
Enterococcus faecalis |
6 (11) |
|
Klebsiella pneumoniae |
3 (5) |
|
Proteus mirabilis |
2 (3) |
Оценка динамики степени выраженности симптомов обострений хронического пиелонефрита на основании опроса пациента до и после лечения представлена на рисунке 1.
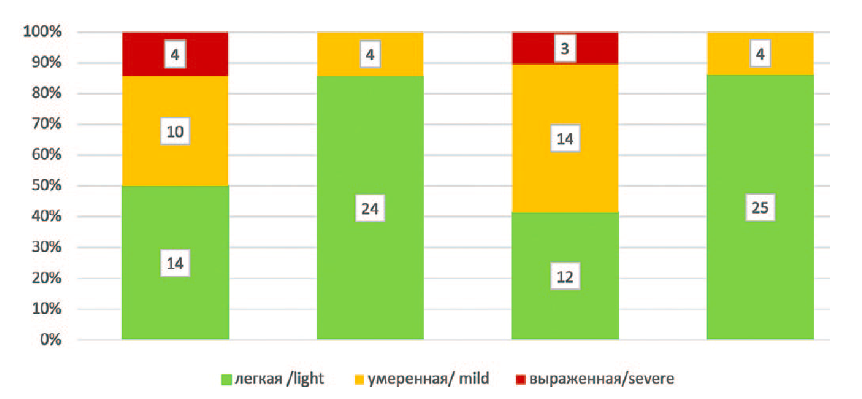
Рис. 1. Динамика выраженности симптомов обострений хронического пиелонефрита до и после лечения (количество пациентов)
Fig. 1. Dynamics of the severity of symptoms of exacerbates pyelonephritis before and after treatment (number of patients)
На фоне терапии в обеих группах достоверно снизился уровень выраженности симптомов, причем в большей степени в группе пациентов, получавших одновременно антибиотикотерапию и «Нефробак»®.
При оценке результатов общего анализа мочи до лечения у всех пациентов в анализах выявлена лейкоцитурия и клинически значимые титры бактериурии.
В обеих группах бактериурия в клинически значимых титрах практически не сохранилась, а сама терапия не повлияла на изменение чувствительности микроорганизмов к антибиотикам у этих больных.
Отмечено значительно меньшее число пациентов с лейкоцитурией на 2-м и и 3-м визитах в группе, получавшей антибиотикотерапию совместно с комплексом «Нефробак»®. В этой группе через 3 месяца наблюдалось на 80% меньше случаев лейкоцитурии, чем в контрольной группе. Через 6 месяцев после начала исследования в данной группе наблюдалось уже на 96% меньше случаев лейкоцитурии (рис. 2). В группе, получавшей только антибиотик, наблюдалось на 60% и 86% меньше случаев лейкоцитурии соответственно.
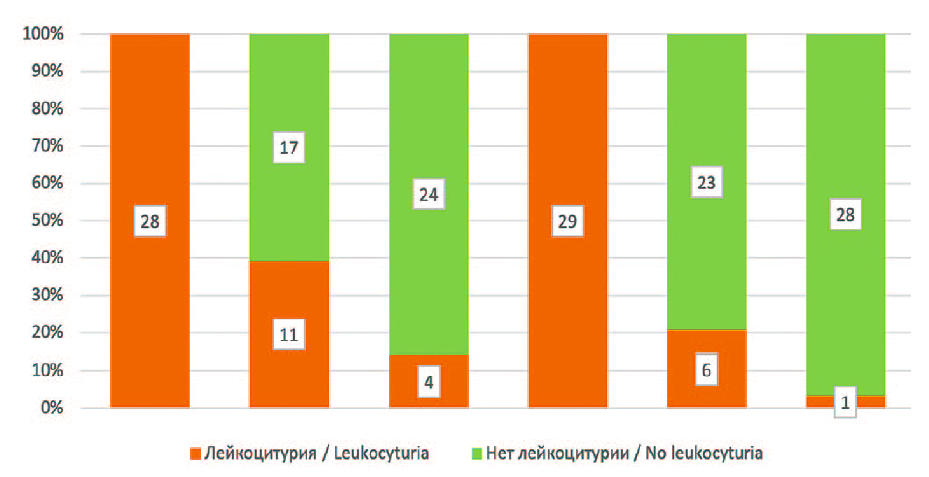
Рис. 2. Динамика лейкоцитурии в обеих группах
Fig.2. Dynamics of leukocyturia in both groups
Отмечается также значительно меньшее количество пациентов с бактериурией на 3-м визите в основной группе по сравнению с контролем (табл. 2). В основной группе, получавшей комплексную терапию, частота бактериурии после лечения сократилась на 96,5% в контрольной – только на 87,5% (p<0,05). В основной группе был отмечен только 1 случай бактериурии, в то время как в контрольной – четыре случая.
Таблица 2. Динамика бактериурии у пациентов в обеих группах
Table 2. Dynamics of bacteriuria in both groups
|
Группа больных Patient group |
До лечения, n / Before treatment, n |
После лечения, n/ After treatment, n |
||
|---|---|---|---|---|
|
Бактериурия есть Bacteriuria is |
Бактериурии нет Bacteriuria no |
Бактериурия есть Bacteriuria is |
Бактериурии нет Bacteriuria no |
|
|
Антибиотик / Antibiotic |
28 |
0 |
4 |
24 |
|
Антибиотик + «Нефробак»® Antibiotic + «Nefrobak»® |
29 |
0 |
1 |
28 |
За все время наблюдения не отмечено ультразвуковых признаков, которые можно было бы трактовать как изменение картины почечного синуса и паренхимы.
Оценка безопасности и регистрация нежелательных явлений проводилась согласно протоколу. Разницы между частотой возникновения нежелательных явлений, обусловленных приемом антибиотиков в обеих группах, не было. Нежелательных явлений, связанных с приемом комплекса «Нефробак»®, отмечено не было ни у одного пациента.
На 2-м визите (через 3 месяца) ни у одного участника исследования в обеих группах не возникло обострения. Однако через 6 месяцев после начала исследования, у 3 пациенток в контрольной группе, принимавшей только антибиотики, выявлено по 1 обострению. В группе, получавшей комбинированную терапию, включающую «Нефробак»®, в течение всего периода наблюдения обострений хронического пиелонефрита обнаружено не было.
ОБСУЖДЕНИЕ
Актуальные руководства Европейской ассоциации урологов и Российского общества урологов рекомендуют применение антибиотиков в качестве препаратов первого выбора при инфекциях мочевыводящих путей (ИМП) [6, 7]. Учитывая, что ИМП являются одними из наиболее распространенных инфекционных заболеваний, встречающихся в общей практике, применение этих рекомендаций может внести значительный вклад в развитие растущей глобальной проблемы устойчивости к антибиотикам [8].
Исходя из этого, крайне важно определить потенциальные альтернативные стратегии. Предыдущие исследования показали, что общее использование антибиотиков может быть значительно снижено за счет начального симптоматического лечения инфекции нижних мочевых путей с помощью нестероидных противовоспалительных препаратов (НПВП), даже несмотря на то, что симптоматическое лечение этими препаратами клинически уступает антибиотикотерапии [9, 10]. Однако в отношении инфекций верхних мочевых путей подобные исследования отсутствуют.
Биологически активный комплекс «Нефробак»® представляет собой экстракты Шлемника байкальского (90% байкалин), Момордики харанции (10% харантин) и листьев Шелковицы белой (1% 1-дезоксиноиримицина). Данные компоненты усиливают бактериостатическое действие пенициллиновых антибиотиков, защищают ткани от последствий избыточного воспалительного ответа, ингибируют рост грамотрицательных (E. coli) и грамположительных (S. epidermis, S. аureus, метициллинрезистентного золотистого стафилококка – MRSA) бактерий, усиливают противоинфекционный иммунитет. В частности, байкалин, содержащийся в Шлемнике байкальском, предотвращает образование биопленок за счет воздействия на РНК бактерий одних штаммов и влияния на QS (quorum sensing – контролируемый фактор вирулентности) других штаммов бактерий, а также защищает ткани почек от избыточного воспалительного ответа [11 – 13]. Экстракт Момордики харанции обладает прямым антибактериальным эффектом в отношении широкого числа микроорганизмов [14, 15]. Экстракт Шелковицы белой ингибирует рост бактерий, усиливает не только действие антибиотиков, но и фагоцитарную активность макрофагов [16–19].
Проведенное нами рандомизированное сравнительное исследование показывает преимущество комбинированной терапии антибиотиками и растительными комплексами над монотерапией в отношении клинических, микробиологических параметров и длительности периода ремиссии хронического пиелонефрита. Применение комплекса «Нефробак»® в течение 1 месяца с последующим наблюдением в течение 5 месяцев показало существенное превосходство по результатам общего и микробиологического анализа мочи, а с учетом высокого профиля безопасности комплекса «Нефробак»® в формате профилактики обострений пиелонефрита будет не лишним предположить о возможности пролонгации месячного курса приема до 3-6 месяцев с целью достижения максимальной эффективности в создании стойкой ремиссии.
Наиболее важным и значимым результатом исследования является снижение количества обострений хронического пиелонефрита за период наблюдения. Данный факт свидетельствует в пользу того, что «Нефробак»® способен не только уменьшать выраженность инфекционно-воспалительного процесса в почке, что отражается в исчезновении лейкоцитурии и бактериурии у пациентов, но и удлинять период ремиссии хронического пиелонефрита.
Так как данное исследование является первым анализом применения препарата «Нефробак»® для лечения и профилактики хронического пиелонефрита, в связи с этим невозможно выполнить сравнительный анализ результатов.
ВЫВОДЫ
На основании результатов проведенного исследования «Нефробак»® может быть рекомендован в качестве элемента комплексной терапии хронического пиелонефрита, оказывающего противорецидивное и противовоспалительное действие, усиливающее антибиотики.
ЛИТЕРАТУРА
1. Зайцев А.В., Касян Г.Р., Харчилава Р.Р. Хронический пиелонефрит. Урология 2016;3:11–17. [Zaitsev A.V., Kasyan G.R., Kharchilava R.R. Chronic pyelonephritis. Urologiya = Urologiia 2016;3:11–17. (In Russian)]. https://doi.org/ 10.18565/urol.2017.1-supplement.27-33.
2. Киличева Т.А. Клиническое течение, противорецидивная терапия и профилактика острых и хронических пиелонефритов у детей. Актуальные научные исследования в современном мире 2017;5:59–61. [Kilicheva T.A. Clinical course, anti-relapse therapy and prevention of acute and chronic pyelonephritis in children. Aktualnyye nauchnyye issledovaniya v sovremennom mire = Actual scientific research in the modern world 2017;5:59–61. (In Russian)].
3. Hoon D, Taylor MT, Kapadia P, Gerhard T, Strom BL, Horton DB. Trends in Off-Label Drug Use in Ambulatory Settings: 2006-2015. Pediatrics 2019;144(4):e20190896. https://doi.org/10.1542/peds.2019-0896.
4. Ventola CL. The antibiotic resistance crisis: part 1: causes and threats. Pharm Ther 2015;11(4):181–224.
5. Langdon A, Crook N, Dantas G. The effects of antibiotics on the microbiome throughout development and alternative approaches for therapeutic modulation. Genome Med. Genome Medicine 2016;8(1):39. https://doi.org/10.1186/s13073-016-0294-z.
6. Bonkat G, Bartoletti R, Bruyère F, Cai T, Geerlings SE Köves B, Kranz J, et al. EAU Guidelines on Urological Infection; 2023; 84 p. URL: https://uroweb.org/guidelines/urological-infections.
7. Урология: Национальное руководство. Краткое издание. Под ред. Н.А. Лопаткина. Москва: ГЭОТАР-Медиа 2013;608. (Серия «Национальные руководства»). [. Urology: National Guide. Brief edition. Ed. N.A. Lopatkin. Moscow: GEOTAR-Media 2013;608. (Series «National guides»). )In Russian)].
8. Wagenlehner FME, Weidner W, Naber G, An update on uncomplicated urinary tract infections in women. Curr Opin Urol 2009;19(4):368–374. https://doi.org/10.1097/ MOU.0b013e32832ae18c.
9. Gágyor I, Bleidorn J, Kochen MM, Schmiemann G, Wegscheider K, Hummers-Pradier E. Ibuprofen versus fosfomycin for uncomplicated urinary tract infection in women: randomised controlled trial. BMJ 2015;351:h6544. https://doi.org/10.1136/bmj.h6544.
10. Kronenberg A, Bütikofer L, Odutayo A, Mühlemann K, da Costa BR, Battaglia M, et al. Symptomatic treatment of uncomplicated lower urinary tract infections in the ambulatory setting: randomised, double blind trial. BMJ 2017;359:j4784. https://doi.org/10.1136/ bmj.j4784.
11. Luo J, Dong B, Wang K, Cai S, Liu T, Cheng X et al. Baicalin inhibits biofilm formation, attenuates the quorum sensing-controlled virulence and enhances Pseudomonas aeruginosa clearance in a mouse peritoneal implant infection model. PLoS One 2017;12(4):e0176883. https://doi.org/10.1371/journal.pone.0176883.
12. Chen W, Li B, Li S, Ou YW, Ou Q. Effects of Scutellaria Baicalensis on Activity and Biofilm Formation of Klebsiella Pneumoniae. Chinese Med Sci J 2016;31(3):180–184. https://doi.org/10.1016/s1001-9294(16)30048-7.
13. Zhao QY, Yuan FW, Liang T, Liang XC, Luo YR, Jiang M, et al. Baicalin inhibits Escherichia coli isolates in bovine mastitic milk and reduces antimicrobial resistance. J Dairy Sci 2018;101(3):2415–2422. https://doi.org/10.3168/jds.2017-13349.
14. Lucena Filho JH, Lima Rde F, Medeiros AC, Pereira JV, Granville-Garcia AF, Costa EM.. Antimicrobial Potential of Momordica charantia L. against Multiresistant Standard Species and Clinical Isolates. J Contemp Dent Pract 2015;16(11):854–858. https://doi.org/10.5005/jp-journals-10024-1770.
15. Kuok CF, Hoi SO, Hoi CF, Chan CH, Fong IH, Ngok CK et al. Synergistic antibacterial effects of herbal extracts and antibiotics on methicillin-resistant Staphylococcus aureus: A computational and experimental study. Exp Biol Med (Maywood) 2017;242(7)731–743. https://doi.org/10.1177/1535370216689828.
16. Sohn HY, Son KH, Kwon CS, Kwon GS, Kang SS. Antimicrobial and cytotoxic activity of 18 prenylated flavonoids isolated from medicinal plants: Morus alba L., Morus mongolica Schneider, Broussnetia papyrifera (L.) Vent, Sophora flavescens Ait and Echinosophora koreensis Nakai. Phytomedicine 2004;11(7–8):666–672. https://doi.org/10.1016/j.phymed.2003.09.005.
17. Park KM, You JS, Lee HY, Baek NI, Hwang JK. Kuwanon G: an antibacterial agent from the root bark of Morus alba against oral pathogens. J Ethnopharma- col 2003;84(2–3):181–185. https://doi.org/10.1016/s0378-8741(02)00318-5.
18. Zuo GY, Yang CX, Han J, Li YQ, Wang GC. Synergism of prenylflavonoids from Morus alba root bark against clinical MRSA isolates. Phytomedicine 2018;39:93–99. https://doi.org/10.1016/j.phymed.2017.12.023.
19. Chang B, Koo B, Lee H, Oh JS, Kim S. Activation of macrophage mediated host defense against salmonella typhimurium by morus alba L. Food Nutr Res 2018;62:1289 https://doi.org/ 10.29219/fnr.v62.1289.







