ВВЕДЕНИЕ
Несмотря на развитие малоинвазивных технологических методов лечения мочекаменной болезни, улучшение функционального состояния почек в послеоперационном периоде не теряет своей значимости в современной урологии. Наиболее часто применяемые эндоскопические методы лечения сложных случаев нефролитиаза позволяют в максимально короткие сроки реабилитировать пациента и социально адаптировать его в повседневной жизни, но вопрос сохранения функционального состояния почечной паренхимы, к сожалению, не оценивается в исходах хирургического лечения. Восстановление почечной функции в послеоперационном периоде является приоритетной задачей при решении проблемы реабилитации пациентов с мочекаменной болезнью.
Снижение и потеря почечной функции после оперативного лечения сложных форм нефролитиаза различными способами создает проблематику вопроса выбора той или иной хирургической техники во избежание отрицательных результатов хирургического лечения. Определение наиболее щадящей и в то же время наиболее эффективной методики оперативного способа лечения мочекаменной болезни продиктовано не только необходимостью сохранения и улучшения параметров степени очистки почки от камней, но и улучшением функционального состояния почки в послеоперационном периоде. Негативные функциональные результаты оперативного лечения могут приводить к инвалидизации пациентов в связи с рисками ухудшения функции почек, к проведению заместительной почечной терапии. В связи с актуальностью проблемы, в нашей работе был проведен анализ корреляции объема интраоперационной кровопотери с изменениями скорости клубочковой фильтрации (СКФ) в послеоперационном периоде при различных способах оперативного лечения сложных форм нефролитиаза.
Цель работы: оценка корреляции объема интраоперационной кровопотери и динамических изменений СКФ в послеоперационном периоде при различных способах хирургического лечения крупных и сложных камней почек.
МАТЕРИАЛЫ И МЕТОДЫ
Проведен ретроспективный анализ 97 пациентов с мочекаменной болезнью, крупными и сложными камнями почек, выбранных методом случайной выборки в период с 2012 по 2019 г. в урологическом отделении городской больницы № 2 г. Нур-Султан Республики Казахстан.
Возраст обследованных пациентов колебался от 23 до 73 лет. Средний возраст составил 49,8±1,42 года. Наибольшее количество пациентов с мочекаменной болезнью представлено в группе 51–60 лет и составило 26 (26,8%) случаев. Самому молодому пациенту было 18 лет, максимальный возраст составил 73 года. В возрасте от 18 до 30 лет было пролечено 12 пациентов (12,4%), с 31 до 40 лет – 13 (13,4%), с 41 до 50 лет – 19 (19,6%), с 71 до 80 лет – 3 пациента (3,1%). Отмечался высокий удельный вес в группе пациентов с 61 до 70 лет – 24 случая (24,7%).
Разделение пациентов по половому признаку в нашем исследовании составило: женщин – 40 (41,2%), мужчин – 57 (58,8%).
Среди интеркуррентных заболеваний чаще встречались заболевания сердечно-сосудистой системы, в частности, артериальная гипертензия (в исследуемых группах ее показатели составили 50,8%), ишемическая болезнь сердца (4,1%), сахарный диабет 2-го типа (12,4%). Все остальные сопутствующие заболевания, такие как язвенная болезнь желудка и 12-перстной кишки, хронический бронхит, бронхиальная астма, составили менее 1%.
У всех пациентов была верифицирована мочекаменная болезнь, крупные и сложные камни почек. Площадь почечных конкрементов менее 300 мм2 составила 42,3%, более 300 мм2 – 54,6% и более 1200 мм2 – 3,1%. Средняя площадь камня составила 428,3± 36,1 мм2, его средняя плотность по Хаунсфилду 1042,9±34,8 HU.
Анализ индекса массы тела пациентов показал следующее распределение: с повышенным весом – 22 пациента (22,7%), с ожирением 1-й степени – 23 пациента (23,7%), с ожирением 2-й степени – 9 больных (9,3%), с ожирением 3-й степени – 5 человек (5,1%). Таким образом, количество пациентов с повышенным весом или с ожирением различной степени превалировало по отношению к группе больных с нормальной массой тела, в отношении 59 (60,8%) против 37 (38,1%), 1 (1,0%) пациент был с дефицитом массы тела.
Все пациенты были разделены на 3 когортные группы сравнения методом случайной выборки. Всем пациентам проводилось хирургическое лечение мочекаменной болезни. Так, распределение исследуемых групп по методу хирургического лечения выглядит следующим образом: перкутанная нефролитотрипсия (ПНЛ) в положении на животе (prone position) – 44 пациента (45,36%), ПНЛ в положении на спине (supine position) – 29 пациентов (29,9%), лапароскопическая пиелолитотомия – 24 пациента (24,74%).
По категории сложности почечных камней, распределение было проведено согласно классификации Guy,s Stone Score. В группе пациентов после проведенной нефролитотрипсии на животе в категорию Grade I вошло 20 (45,4%) пациентов, Grade II и III по 10 (22,8%) пациентов соответственно, в самую сложную категорию Grade IV – 4 (9,1%) пациента. Распределение пациентов в группе ПНЛ на спине выглядит следующим образом: Grade I – 11 (37,9 %), Grade II – 10 (34,5 %), Grade III – 3 (10,3 %), Grade IV – 5 (17,2%) пациентов. В группе лапароскопической пиелолитотомии было отмечено только 3 категории сложности: Grade I – 21 (84%), Grade II – 2 (8%) и Grade III – 2 (8%) пациента.
Средняя продолжительность хирургического вмешательства при проведении ПНЛ на животе составила 92,8±6,81 мин, ПНЛ на спине – 119,65±10,92 мин, лапароскопической пиелолитотомии – 183,7±11,12 мин.
Интраоперационное кровотечение встречалось при выполнении ПНЛ на животе в 3 (6,8%) случаях (ОР = 0,494; 95%; ДИ 0,11–2,04; p<0,05), ПНЛ на спине в 4 (13,8%) случаях (ОР = 2,023; 95%; ДИ 0,48–8,38; p<0,05), при лапароскопической пиелолитотомии в 1 (4 %) случае (ОР = 0,56; 95%; ДИ 0,06–5,14; p<0,05). Так средняя кровопотеря при ПНЛ на животе составила 144,5±9,1 мл, при ПНЛ на спине 235,23±19,1 мл, при лапароскопической пиелолитотомии 43,1±5,2 мл. Объем интраоперационной кровопотери определялся непрямым методом по упрощенной формуле Moore:
Vк = ОЦКд (Hbд – Hbф) / Hbд,
где Vк – объем кровопотери, мл;
ОЦКд – объем циркулирующей крови, мл;
Hbд – должный гемоглобин,
Hbф – фактический гемоглобин (определяется после остановки кровотечения и стабилизации гемодинамики) [1-3].
Оценка показателя СКФ оценивалась по формуле CKD-EPI (Chronic Kidney Desease Epidemiology Collaboration). Медиана исходной СКФ в группе пациентов ПНЛ на животе составила 91 (мл/мин/1,73 м2 ), в группе пациентов ПНЛ на спине 95 (мл/мин/1,73 м2 ), в группе пациентов лапароскопической пиелолитотомии 101 (мл/мин/1,73 м2 ). Исходное снижение СКФ (менее 60 мл/мин/1,73 м2 ), соответствующее ХБП (хроническая болезнь почек) III стадии, в группе пациентов ПНЛ на животе отмечено в 6 (6,2%) случаях, в группе пациентов ПНЛ на спине в 3 (3,1%) случаях, в группе пациентов лапароскопической пиелолитотомии в 2 (2,1%) случаях. В 2 (2,1%) случаях в группе пациентов ПНЛ на спине отмечалось снижение СКФ менее 30 (мл/мин/1,73 м2), что соответствует ХБП IV. Пациентов с терминальной V стадией ХБП в исследуемых группах не было. Почечную функцию оценивали в раннем послеоперационном периоде по формуле CKD-EPI на 7-е сутки, изменения в раннем послеоперационном периоде оценивали по системе RIFLE (Risk – риск, Injury – повреждение, Failure – недостаточность, Loss of kidney function – утрата почечной функции, End-stage kidney disease – терминальная стадия болезни почек).
Статистическая обработка полученных данных проводилась в программе Excel Microsoft Office. Определялся коэффициент ранговой корреляции Спирмена – непараметрический метод, который используется с целью статистического изучения связи между явлениями. В этом случае определяется фактическая степень параллелизма между двумя количественными рядами изучаемых признаков и дается оценка тесноты установленной связи с помощью количественно выраженного коэффициента.
РЕЗУЛЬТАТЫ
Послеоперационные изменения функционального состояния почек в исследуемых группах имеют определенные различия в зависимости от вида проведенного хирургического лечения пациентов с мочекаменной болезнью. Так, в группе ПНЛ на животе медиана СКФ составила – 91 (мл/мин/1,73м2), в группе ПНЛ на спине – 86,5 (мл/мин/1,73м2), после лапароскопической пиелолитотомии – 107 (мл/мин/1,73м2). Снижение послеоперационной СКФ менее 60 (мл/мин/1,73м2), соответствующее ХБП III стадии, выявлено в группе ПНЛ на животе в 6 (6,2%) случаях, в группе ПНЛ на спине определяется увеличение случаев до 7 (7,2%) пациентов, после лапароскопической пиелолитотомии не выявлено ни одного случая. В группе ПНЛ на спине в 3 (3,1%) случаях имеется снижение СКФ менее 30 (мл/мин/1,73м2), что соответствует ХБП IV стадии.
Сравнение медианы СКФ до операции и в послеоперационном периоде выявило следующие изменения. Так, в группе ПНЛ на животе определяется увеличение показателя медианы СКФ на 2 (мл/мин/1,73м2), после ПНЛ на спине отмечается снижение медианы СКФ на 1 (мл/мин/1,73м2), в группе лапароскопической пиелолитотомии выявлено увеличение медианы СКФ на 3,5 (мл/мин/1,73м2).
Риск развития острого почечного повреждения в послеоперационном периоде выявлялся на основании оценки классификации по системе RIFLE (табл. 1). Выявлено, что риск развития острого почечного повреждения в послеоперационном периоде наиболее высок в группе ПНЛ на спине: в категории «Риск» выявлено 3 (3,1%) случая, в категории «Повреждение» – 2 (2,1%) случая. Наряду с этим, стоит отметить наличие риска острого почечного повреждения и в группе ПНЛ на животе: категория «Риск» составляет 4 (4,1%) случая. В группе пациентов лапароскопической пиелолитотомии риски развития острого почечного повреждения отсутствуют.
Таблица 1. Острое снижение функции почки в раннем послеоперационном периоде (n = 97) в исследуемых группах сравнения различных хирургических методов лечения крупных и сложных камней почек, n (%)
Table 1. Acute decrease in renal function in the early postoperative period (n = 97) in the study groups comparing different surgical methods of treating large and complex kidney stones, n (%)
| Категория Category |
ПНЛ на животе Percutaneous nephrolithotripsy prone position |
ПНЛ на спине Percutaneous nephrolithotripsy supine position |
Лапароскопическая пиелолитотомия Laparoscopic pyelolitotomy |
|---|---|---|---|
| Риск Risk |
4 (4,1%) | 3 (3,19%) | 0 |
| Повреждение Injury |
0 | 2 (2,1%) | 0 |
| Потеря почечной функции Loss |
0 | 0 | 0 |
| Терминальная почечная недостаточность End stage renal disease |
0 | 0 | 0 |
| Всего Total |
4 | 5 | 0 |
Проведен анализ и поиск возможных корреляций, способствующих увеличению развития рисков возникновения острого почечного повреждения в послеоперационном периоде. Среди возможных факторов риска развития острого почечного повреждения в послеоперационном периоде рассматривалась возможная связь с объемом интраоперационной кровопотери. Статистический анализ проводился с учетом оценки парных корреляций (корреляция Спирмена, двусторонняя значимость).
Обнаружена корреляция СКФ в послеоперационном периоде с интраоперационной кровопотерей в общей группе (r = 0,410, p<0,001) в исследуемых группах: в 1-й группе при ПНЛ на животе (r = 0,363, p<0,05), во 2-й группе при ПНЛ на спине (r = 0,49, p>0,1), в 3-й группе при лапароскопической пиелолитотомии (r = 0,264, p>0,1). Таким образом, отмечена корреляция рисков ухудшения функционального состояния почек и объема интраоперационной кровопотери в послеоперационном периоде на основании показателей СКФ.
Также проведен анализ связи показателей объема интраоперационной кровопотери с различными факторами, такими как: индекс массы тела (ИМТ), плотность камня, площадь камня, диаметр используемого нефроскопа. В 1-й группе корреляция объема интраоперационной кровопотери с ИМТ составила r = 0,459, p = 0,001; с плотностью камня: r = 0,361, p<0,05; с площадью камня: r = 0,507, p = 0,001. Таким образом, в 1-й группе имеется корреляция плотности камня, его площади и ИМТ пациента с объемом предполагаемой кровопотери, при этом превалирующее значение имеет ИМТ пациента. Во 2-й группе корреляция объема интраоперационной кровопотери с ИМТ составила r = 0,445, p<0,05; с плотностью камня: r = 0,541, p<0,01; с площадью камня: r = 0,374, p<0,05. Анализ данных параметров определяет наличие во 2-й группе корреляции плотности камня, его площади и ИМТ пациента с объемом предполагаемой кровопотери, однако более выраженная связь отмечается с плотностью камня. В 3-й группе определена корреляция объема интраоперационной кровопотери с ИМТ: r = 0,593, p<0,01; с плотностью камня: r = 0,431, p<0,05; с площадью камня: r = 0,588, p<0,01. В данной группе также выявлена корреляция плотности и площади почечного камня и ИМТ пациента с объемом предполагаемой интраоперационной кровопотери, более четкая связь определяется с ИМТ пациента.
Таким образом, риск кровотечения наиболее вероятен во 2-й группе. Следует учитывать данные корреляции таких параметров, как плотность и площадь почечного камня, ИМТ, при выборе оптимального способа лечения пациентов с крупными и сложными камнями почек. При этом ИМТ имеет более выраженную корреляцию с рисками развития кровотечения в 1-й и 3-й группах, а плотность камня имеет значение в прогнозируемых рисках развития интраоперационной кровопотери во 2-й группе. Факторы риска развития интраоперационного кровотечения при различных видах оперативных вмешательств по поводу камней почек представлены в таблице 2.
Таблица 2. Факторы риска развития интраоперационного кровотечения при различных видах оперативных вмешательств по поводу камней почек
Table 2. Risk factors for intraoperative bleeding in various types of kidney stone surgery
| Показатель Index |
1-я группа 1st cohort |
2-я группа 2nd cohort |
3-я группа 3rd cohort |
|||
|---|---|---|---|---|---|---|
| r | p | r | p | r | p | |
| Плотность камня Stone density |
0,361 | <0,05 | 0,541 | <0,01 | 0,431 | <0,05 |
| Площадь камня Stone area |
0,507 | 0,001 | 0,374 | <0,05 | 0,588 | <0,01 |
| ИМТ Index body mass |
0,459 | 0,001 | 0,445 | <0,05 | 0,593 | <0,01 |
Примечание: r – корреляция Спирмена, p – двухсторонняя значимость
Note: r – Spearman correlation, p – two-tailed significance
Проанализировав данные интраоперационной кровопотери, обнаружена корреляция между диаметром используемого нефроскопа и объемом кровопотери (r = 0,7, p<0,001). Средняя интраоперационная кровопотеря при использовании стандартного нефроскопа диаметром 26 Fr составила 213,6±112,3 мл, при использовании мини-нефроскопа диаметром 12 Fr – 142,7±58,8 мл (рис. 1). Полученные нами данные доказывают преимущество использования мини-перкутанной техники при выполнении нефролитотрипсии, позволяющей снизить риски развития интраоперационного кровотечения и уменьшить объем интраоперационной кровопотери.
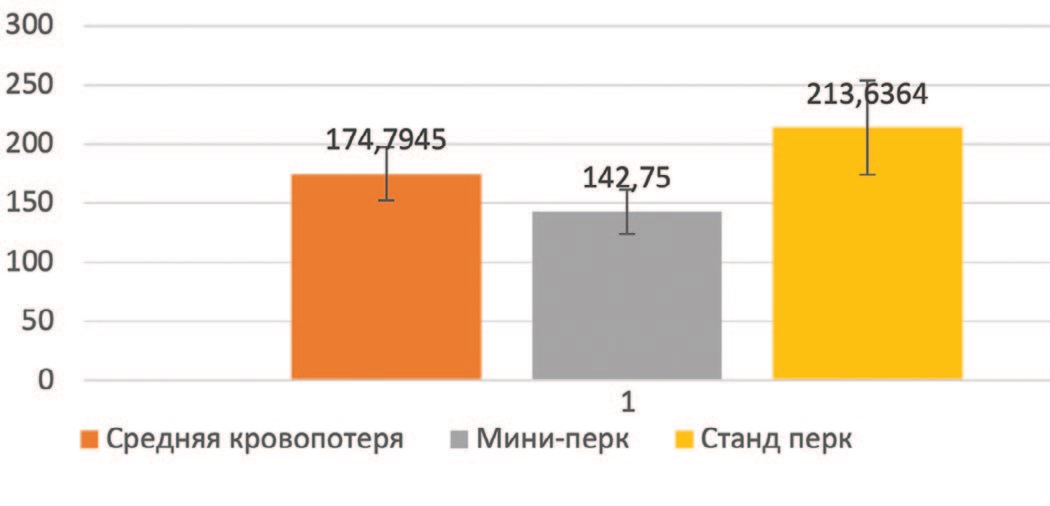
Рис.1. Объем интраоперационной кровопотери в зависимости от диаметра используемого нефроскопа
Fig. 1. Volume of intraoperational blood loss by nephroscope diameter used
ОБСУЖДЕНИЕ
Оценка процессов, влияющих на динамические изменения скорости клубочковой фильтрации в течение раннего послеоперационного периода при различных современных методах лечения мочекаменной болезни, таких как ПНЛ, лапароскопическая пиелолитотомия, позволит определить и изменить подходы ведения и лечения, улучшить функциональные результаты состояния почечной паренхимы данной категории пациентов. При анализе послеоперационного течения СКФ в качестве критериев оценки функционального состояния паренхимы почек использовались стадии ХБП, динамические изменения СКФ до операции и в послеоперационном периоде, критерии RIFLE, частота использования заместительной почечной терапии. Сохранение почечной функции является наиболее важным фактором в принятии решения пациента на проведение оперативного лечения. Так, выраженное беспокойство пациентов с мочекаменной болезнью связано с высоким риском потери функции почек и высокой вероятностью проведения программного гемодиализа [4].
К факторам риска, способствующим развитию ХБП у пациентов с нефролитиазом, следует отнести: дистальный почечный ацидоз, медуллярную губчатую почку, первичный гиперпаратиреоидизм, гиперкальциурию, мальабсортивный синдром и другие генетические нарушения обмена веществ, например расстройства натрийфосфорного обмена [5, 6]. Патогенез развития ХБП имеет несколько различных механизмов развития [7, 8]. Так, одним из наиболее вероятных является нарушение оттока мочи вследствие обструкции просвета мочеточника мочевым камнем [9-14]. ХБП также может развиваться вследствие повреждения почечной паренхимы при осложненных формах мочекаменной болезни, таких как острый пиелонефрит, а также обструктивные нефропатии, либо вследствие проведенного хирургического лечения камней почек [15].
Послеоперационное острое почечное повреждение встречается достаточно часто и составляет от 6,7 до 38,2% от общего числа операций, приводит к ухудшению послеоперационных результатов, способствует увеличению сроков пребывания в стационаре с большой вероятностью использования реанимационной койки [16, 17]. В своей работе J. Yu и соавт. провели анализ вероятности развития острого почечного повреждения после ПНЛ, а также формирования ХБП в отдаленном периоде. Частота развития острого почечного повреждения в послеоперационном периоде в исследовании по данным авторов составила 16,2 % [18]. Некоторые авторов считают интраоперационную кровопотерю и гипотензию наиболее вероятными причинами развития острого почечного повреждения, наряду с такими факторами риска, как возраст, сахарный диабет, гиперурикемия, длительность оперативного вмешательства [19-21]. Большинство случаев периоперационного острого почечного повреждения, по данным различных авторов вызваны преренальной азотемией или острым трубчатым некрозом из-за почечной гипоперфузии, что является следствием неблагоприятных исходов (таких как ишемическая травма почек) и увеличивает риск развития ХБП [22, 23].
В исследуемых нами группах исходное снижение СКФ (менее 60 мл/мин/1,73м2), соответствующее ХБП III стадии, в группе пациентов ПНЛ на животе отмечено в 6 (6,2%) случаях, в группе пациентов на спине в 3 (3,1%) случаях, в группе пациентов лапароскопической пиелолитотомии в 2 (2,1%) случаях. В 2 (2,1%) случаях в группе пациентов ПНЛ на спине отмечалось снижение СКФ менее 30 (мл/мин/1,73м2), что соответствует ХБП IV степени. В сравнении с исходными значениями СКФ, в исследуемых группах отмечалось увеличение показателя медианы СКФ на 2 (мл/мин/1,73м2) после ПНЛ на животе, рост медианы СКФ на 3,5 (мл/мин/1,73м2) после лапароскопической пиелолитотомии. Однако после перенесенной ПНЛ на спине отмечалась отрицательная динамика в виде снижения показателя медианы СКФ на 1 (мл/мин/1,73м2).
В отличие от предоперационного периода распределение пациентов согласно классификации стадий ХБП было следующим: в группе пациентов после ПНЛ на животе количество пациентов с ХБП III стадии (СКФ менее 60 мл/мин/1,73 м2) оставалось на исходном уровне и составляло 6 (6,2 %) человек, в группе лапароскопической пиелолитотомии отмечалась стойкая положительная динамика улучшения показателей СКФ и отсутствие случаев с ХБП III стадии. Наиболее отрицательные изменения СКФ наблюдались в группе пациентов после ПНЛ на спине. Так, отмечалось увеличение количества пациентов с ХБП III стадии с 3 (3,1%) до 7 (7,2%) случаев, с ХБП IV стадии (СКФ менее 30 мл/мин/1,73м2) – с 2 (2,1%) до 3 (3,1%) случаев. Одним из основных факторов риска, способствующих СКФ, на наш взгляд, является характеристика хирургической агрессии. Так, немаловажное значение имеет интраоперационная кровопотеря, способствующая ишемизации почечной паренхимы и возможной гибели части функционирующих нефронов почки. Частота хирургической агрессии в исследуемых группах выглядела следующим образом: при ПНЛ на животе – в 3 (6,8%) случаях (ОР = 0,494; 95 %; ДИ 0,11–2,04; p<0,05), ПНЛ на спине – в 4 (13,79%) случаях (ОР = 2,023; 95 %; ДИ 0,48–8,38; p<0,05), при лапароскопической пиелолитотомии – в 1 (4%) случае (ОР = 0,56; 95 %; ДИ 0,06–5,14; p<0,05). Средняя кровопотеря при ПНЛ на животе составила 144,54±9,09 мл, при ПНЛ на спине – 235,29±19,06 мл, при лапароскопической пиелолитотомии – 43,12±5,22 мл. Обнаружена корреляция изменений СКФ в послеоперационном периоде с интраоперационной кровопотерей (r = 0,410, p<0,001).
Оценка рисков развития острого почечного повреждения, на наш взгляд, является немаловажным фактором определения эффективности проведенного хирургического лечения. Так, систематизация исходных и послеоперационных данных СКФ по критериям риска развития острого повреждения почек системы RIFLE позволяет получить объективные данные о тяжести повреждения почечной паренхимы для определения дальнейшей тактики лечения. Соответственно, в нашем исследовании риск развития острого почечного повреждения в послеоперационном периоде был наиболее высок в группе ПНЛ на спине: в категории «Риск» выявлено 3 (3,1%) случая, категории «Повреждение» 2 (2,1%) случая. Наряду с этим, в группе ПНЛ на животе категория «Риск» составила 4 (4,1%) случая. В группе пациентов лапароскопической пиелолитотомии риски развития острого почечного повреждения по критериям RIFLE отсутствовали. Одному пациенту (1,0%), соответствующему категории «Повреждение», в раннем послеоперационном периоде проводилась заместительная почечная терапия.
Таким образом, оценка функционального состояния почки с использованием динамики СКФ, системы рисков развития острого почечного повреждения RIFLE, с учетом параметров условного риска объема интраоперационной кровопотери, оправдана и поможет лечащему персоналу при выборе соответствующей методики хирургического лечения крупных и сложных камней почек, а также позволит избежать или спрогнозировать риски развития острого почечного повреждения в раннем послеоперационном периоде.
ЗАКЛЮЧЕНИЕ
Объем интраоперационной кровопотери имеет огромное значение в прогнозировании рисков возникновения острого почечного повреждения в послеоперационном периоде. Использование динамической оценки СКФ позволяет оценить риски развития острого почечного повреждения в послеоперационном периоде, что, безусловно, увеличивает шансы скорейшей реабилитации пациентов с мочекаменной болезнью. Анализ характера изменений функционального состояния почечной паренхимы после различного рода хирургических вмешательств по поводу крупных и сложных камней почек позволяет планировать наиболее безопасный и эффективный способ предстоящего оперативного вмешательства. Наше исследование показало, что в группах сравнения различных методов хирургического лечения крупных и сложных камней почек ПНЛ на спине является прогностически отягощающей состояние функциональной активности почки.







