По данным Российских клинических рекомендаций Российского общества урологов мочекаменная болезнь (МКБ) – хроническое системное заболевание, являющееся следствием метаболических нарушений и/или влияния факторов внешней среды и проявляющееся образованием камней в верхних мочевых путях [1]. Необходимо подчеркнуть, что уролитиаз – заболевание хроническое, то есть медленно прогрессирующее и длительно текущее [2]. Диагностика и лечение хронических заболеваний является достаточно сложным процессом, что обусловлено наличием большого количества пробелов в понимании этиологии и патогенеза данных расстройств [3].
При лечении хронических заболеваний издавна и с успехом используется традиционная медицина – комплекс накопленных народом эмпирических знаний. Важным направлением традиционной медицины является фитотерапия метод лечения, основанный на использовании лекарственных растений и комплексных препаратов из них. Фитотерапия с успехом применяется при МКБ и в настоящее время [4-6]. На фоне лечения травами отмечается снижение количества рецидивов уролитиаза, улучшается способность организма к самостоятельному отхождению камней. Несмотря на то, что фитотерапия является частью традиционной медицины и лечение травами применяется в течение многих столетий, существует большое количество научных работ, доказывающих эффективность применения данной группы препаратов у пациентов, в том числе и при МКБ.
Отличительным свойством растительных препаратов является безопасность и надежность их применения. Вероятность возникновения побочных действий и явлений крайне низка и, как правило, связана с индивидуальной непереносимостью компонентов фитопрепарата.
На отечественном фармацевтическом рынке достаточно широко распространены биологически активные добавки к пище (БАД), состоящие из экстрактов различных трав, применяемые при МКБ. Одной из подобных биодобавок является отечественный препарат «Оксалит», производства компании OOO «ЭСЭЙЧ ФАРМА», Россия. В состав препарата «Оксалит» входят сухие экстракты Фукуса пузырчатого, травы Филлантуса нирури, травы Десмодиума стираксолистного (рис. 1) [7-16].

Рис. 1 Растения, входящие в состав БАД «ОКСАЛИТ»: А. Десмодиум стираксолистный Б. Филлантус нирури В. Фукус пузырчатый
Fig. 1 Plants that make up the OXALIT dietary supplement: A. Styrofoam desmodium B. Phyllanthus niruri V. Fucus vesiculus
Целью нашей работы стало изучение влияния препарата на метаболические показатели пациентов, страдающих уролитиазом, и определение возможностей применения данного препарата в лечении больных МКБ.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
На базе двух медицинских учреждений: НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал «НМИЦ радиологии» Минздрава России и кафедры урологии и андрологии Федерального медико-биологического агентства России в течение 5 месяцев проводилось клиническое исследование комплекса «Оксалит».
В исследовании приняли участие 60 пациентов с диагнозом МКБ, кальций-оксалатный уролитиаз. Всего было обследовано 43 мужчины и 17 женщин, средний возраст пациентов составил 46,1 лет. Пациенты случайным образом были распределены в основную группу и группу контроля.
Основную группу составили 30 (50%) пациентов, получавших в качестве основного лечения БАД «Оксалит» и соблюдавших рекомендации по диетотерапии в течение 90 дней. Контрольную группу составили 30 (50%) больных МКБ, соблюдавших диету в течение 90 дней. Группы пациентов четко соответствовали критериям включения и исключения, предусмотренными протоколом исследования.
Методы исследования: сбор анамнестических данных, оценка стереотипа питания с помощью компьютерной версии анализатора стереотипа питания, общий анализ мочи, биохимический анализ суточной мочи: кальций, натрий, магний, фосфор, мочевина, креатинин, мочевая кислота, оксалаты, цитраты.
Биохимические исследования осуществляли на автоматическом анализаторе «ADVIA-1200» («Bayer-Siemens»). Общий клинический анализ мочи выполнялся с помощью портативного анализатора мочи «ЭТТА АМП-01».
Биологически активный комплекс «Оксалит» назначался по 1 капсуле (406 мг) два раза в день во время приема пищи. Курс лечения составил 90 дней. Влияние препарата на состояние пациентов оценивалось по изменению биохимических показателей суточной мочи, отражающих функциональное состояние почек и метаболизм основных камнеобразующих веществ, по изменению диуреза, pH мочи и других показателей общего анализа мочи.
Анализ полученных данных осуществлялся с помощью методов статического анализа: критерия МаннаУитни и t-критерия Стъюдента посредством компьютерной программы Statistica 10 (StatSoft USA).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Анализ данных, отражающих состояние обмена камнеобразующих веществ, показал, что под действием БАД происходит изменение следующих биохимических показателей обмена литогенных веществ: снижается уровень почечной суточной экскреции оксалатов в 2,4 раза: с 0,22±0,04 до 0,09±0,01 ммоль/сутки (р<0,05), увеличивается уровень почечной суточной экскреции ингибитора кальций-оксалатного камнеобразования – магния – на 53,4%: с 3,41 ± 0,29 до 5,23 ± 0,57 ммоль/сутки (р=0,01) (табл. 1, рис. 2).
Таблица 1. Биохимические показатели мочи у пациентов в основной группе (n=30)
Table 1. Biochemical parameters of urine in patients in the main group (n = 30)
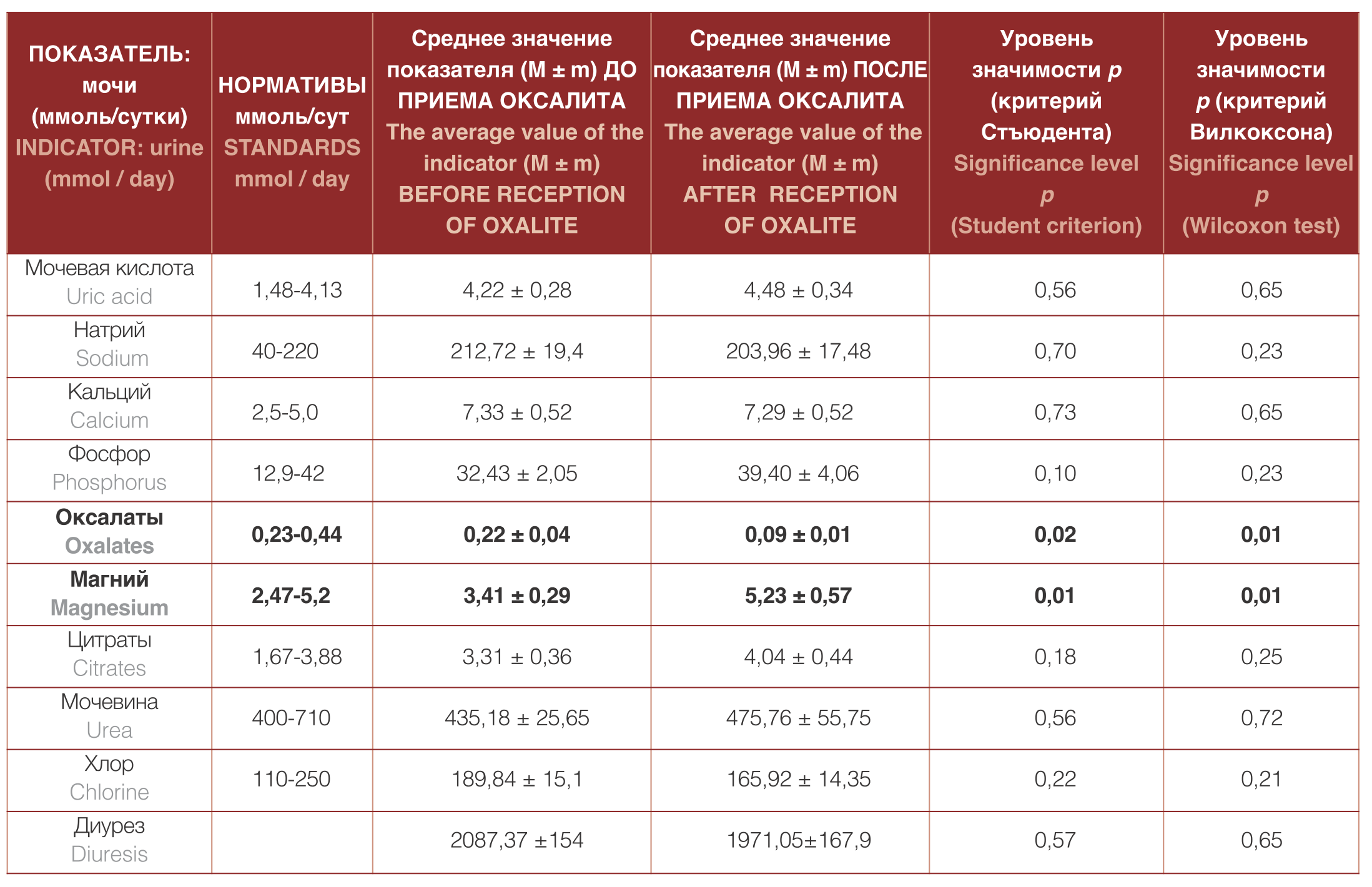
Примечание: n – число наблюдений в группах, M – среднее арифметическое, m – стандартная ошибка среднего, p – статистический показатель достоверности различия
Note: n is the number of observations in groups, M is the arithmetic mean, m is the standard error of the mean, p is a statistical indicator of the significance of the difference
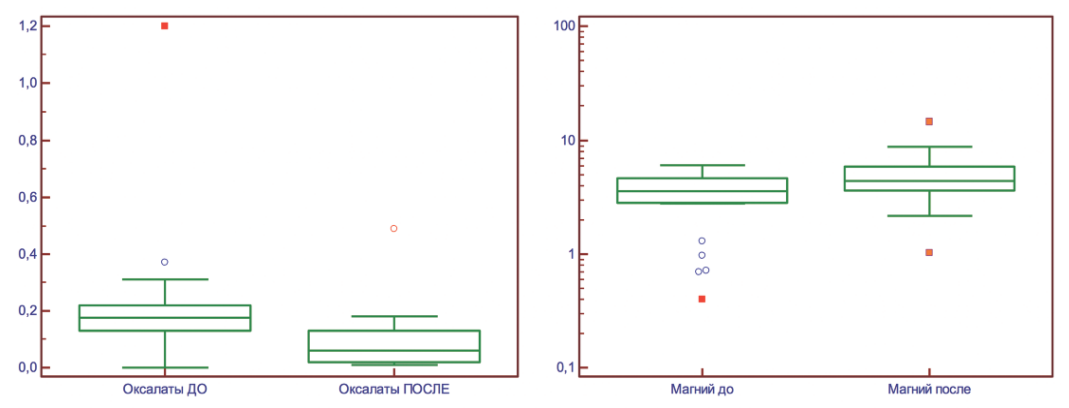
Рис. 2. Изменения показателей уровня экскреции оксалатов и магния у пациентов с МКБ на фоне приема биологически активного комплекса «Оксалит».
Fig. 2. Changes in indicators of the level of excretion of oxalates and magnesium in patients with MKD while taking the biologically active complex «Oxalit»
Влияния препарата на почечную суточную экскрецию других литогенных веществ: кальция, мочевой кислоты, натрия, фосфора, цитратов не отмечено. Также не обнаружено влияния изучаемой биологически активной добавки к пище на содержание в суточной моче мочевины и креатинина.
Установлено, что на фоне приема препарата показатели суточного диуреза оставались без изменений.
Результаты проведения исследования биологически активного комплекса «Оксалит» представлены в таблицах 1-3.
Таблица 2. Биохимические показатели мочи у пациентов в контрольной группе (n=30)
Table 2. Biochemical parameters of urine in patients in control group (n = 30)
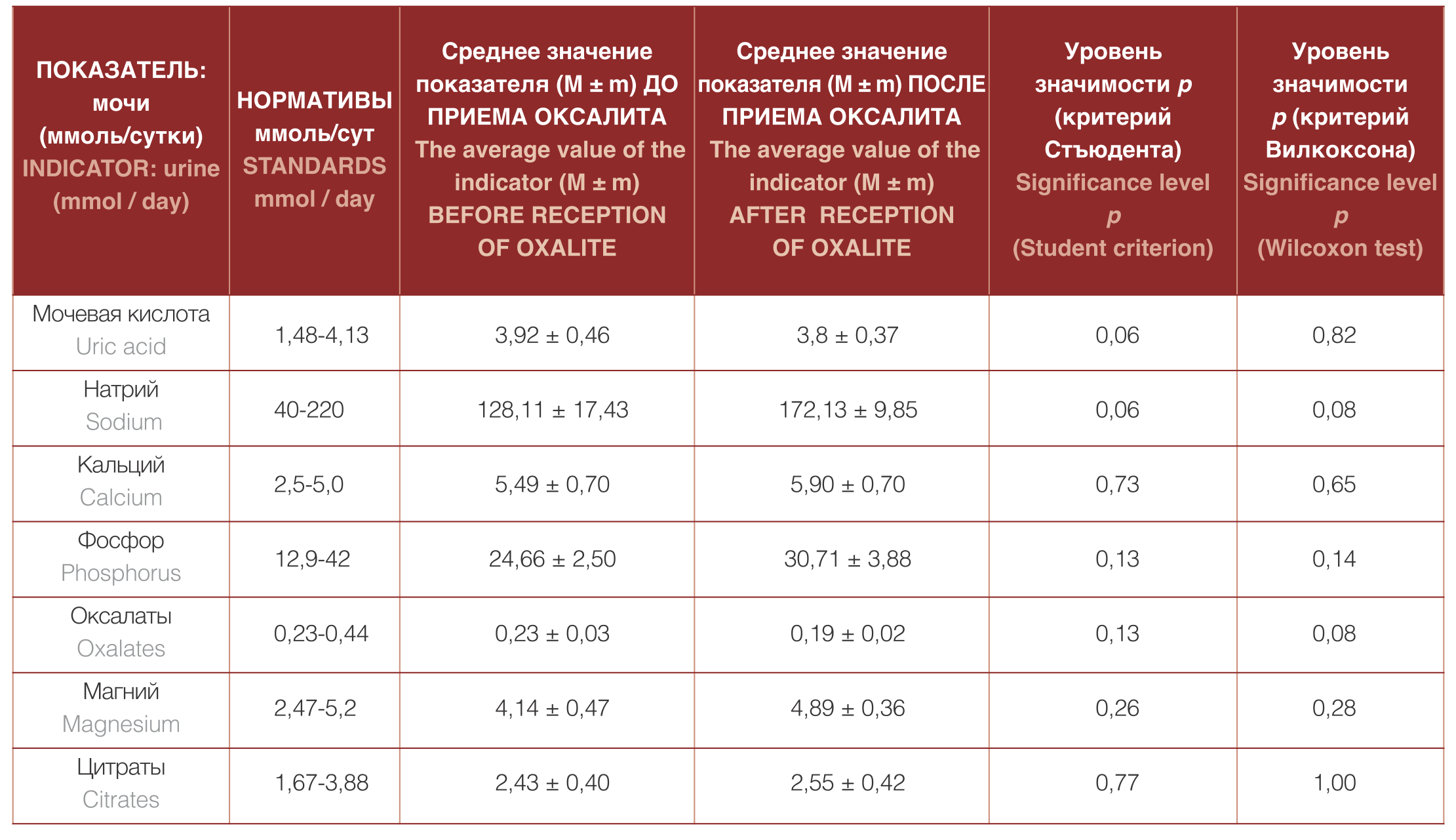
Примечание: n – число наблюдений в группах, M – среднее арифметическое, m – стандартная ошибка среднего, p – статистический показатель достоверности различия
Note: n is the number of observations in groups, M is the arithmetic mean, m is the standard error of the mean, p is a statistical indicator of the significance of the difference
Проведен сравнительный анализ результатов, полученных при применении препарата, с результатами, полученными при назначении только диетотерапии пациентам контрольной группы. Результаты исследования контрольной группы представлены в таблице 2, на рисунке 3 Установлено, что при назначении пациентам с МКБ диетотерапии изменений в их метаболическом статусе по изучаемым показателям не произошло в отличие от больных, получавших кроме диетотерапии и препарат. Отсутствие положительных изменений в биохимическом анализе суточной мочи у пациентов, вошедших в контрольную группу, вероятно связано с тем, что многие больные уже соблюдали общие диетологические рекомендации до начала исследования.
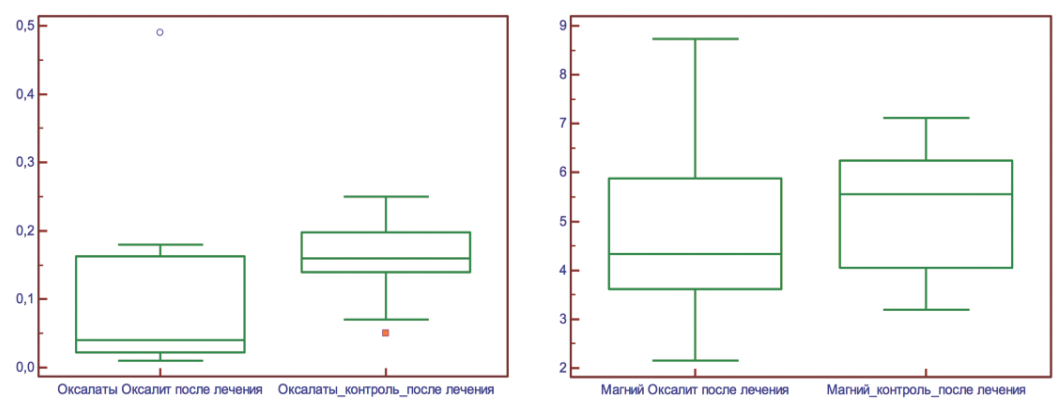
Рис. 3. Изменения показателей уровня экскреции оксалатов и магния у пациентов с МКБ на фоне приема биологически активного комплекса «Оксалит» и на фоне диетотерапии (контрольная группа)
Fig. 3. Changes in the indicators of the level of excretion of oxalates and magnesium in patients with MKD while taking the biologically active complex «Oxalit» and against the background of diet therapy (control group)
Результаты анализа данных общего клинического анализа мочи больных основной и контрольной групп показали, что при применении биологически активного комплекса «Оксалит» уровень общего белка в моче был более, чем в 3 раза ниже, чем у пациентов, не получавших биодобавки, что является положительным влиянием препарата. Также отмечено более низкое содержание в моче кетонов по сравнению с контрольной группой, что также является позитивным эффектом. Уровень лейкоцитурии на фоне применения препарата оказался почти в 2,5 раза ниже, чем у пациентов, не получавших биодобавки. Уровень эритроцитурии был почти в 3 раза меньше при применении БАД по сравнению с контрольной группой. На фоне лечения Препаратом незначительно выше (в пределах нормы) оказалась относительная плотность мочи. Обнаружено более высокое содержание в моче аскорбиновой кислоты, что могло явиться причиной незначительного снижения рН мочи.
При применении препарата уровень глюкозы в моче увеличивался выше нормальных показателей, что, скорее всего, не свидетельствует о возникновении патологического процесса, так как подобное изменение может быть и в физиологических условиях: временно в связи с приемом препарата.
Содержание билирубина в моче больных основной и контрольной групп на фоне лечения было одинаковым. Полученные результаты могут свидетельствовать о том, что Препарат не оказывает токсического действия на печень и почки.
Результаты анализа данных обследования больных уролитиазом на предмет возможного влияния биологически активного комплекса «Оксалит» на показатели общего клинического анализа мочи представлен в таблице 3
Таблица 3. Сравнительный анализ средних значений показателей общего клинического анализа мочи в основной и контрольной группах у больных кальций-оксалатным уролитиазом
Table 3. Comparative analysis of the average values of the indicators of the urine general clinical analysis in the main and control groups in patients with calcium-oxalate urolithiasis
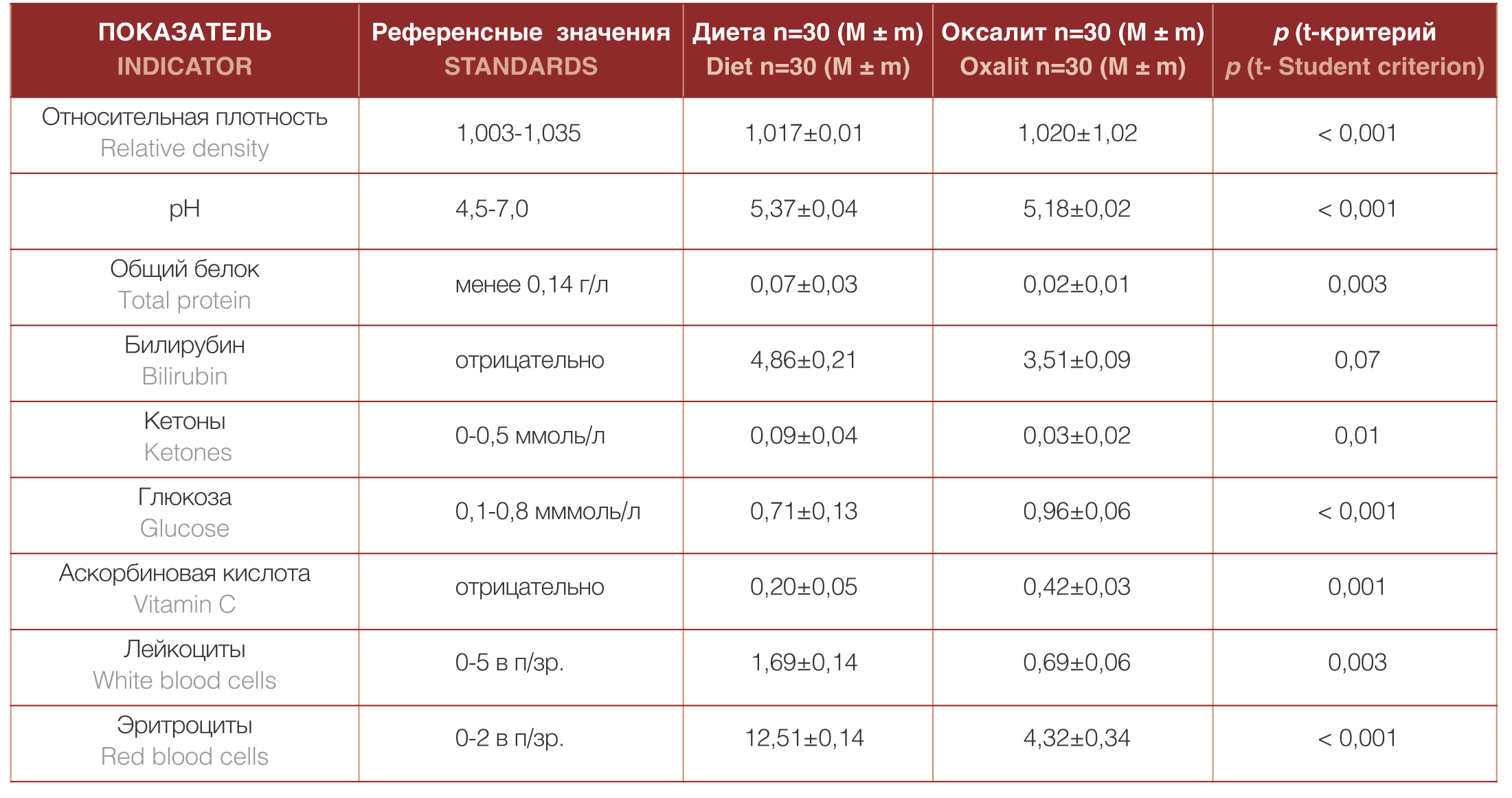
Примечание: n – число наблюдений в группах, M – среднее арифметическое, m – стандартная ошибка среднего, p – статистический показатель достоверности различия, *Анализы (полный справочник под редакцией Ингерлейб М.Б., 2012 год)
Note: n is the number of observations in groups, M is the arithmetic mean, m is the standard error of the mean, p is a statistical indicator of the significance of the difference, * Analyzes (full reference edited by Ingerleib MB, 2012)
Побочных действий БАД «Оксалит» не отмечено. Все больные отметили хорошую переносимость препарата.
ВЫВОДЫ
Результаты проведенного исследования показали, что применение биологически активного комплекса «Оксалит» у пациентов с МКБ не оказывает отрицательного действия на функциональное состояние печени и почек и не оказывает мочегонного действия. Препарат оказывает значительное положительное влияние на обмен литогенного вещества –оксалатов: при его применении снижается уровень содержания оксалатов в суточной моче в 2,4 раза (р<0,05) Необходимо отметить, что на фоне приема БАД выявлено увеличение на 54%, уровня экскреции с мочой магния. На фоне приема препарата было отмечено уменьшение степени гематурии меньше в 3 раза относительно группы контроля.
На фоне приема препарата незначительно, в пределах нормы повышается относительная плотность мочи. Кроме того, по результатам исследования выявлено незначительное подкисление мочи, а также увеличение экскреции с мочой глюкозы и кетонов.
Не выявлено статистически достоверных изменений в почечной суточной экскреции других литогенных веществ: кальция, мочевой кислоты, натрия, неорганических фосфатов, а также низкомолекулярного ингибитора камнеобразования – цитратов. Также не обнаружено влияния изучаемой БАД на содержание в суточной моче мочевины, хлора, билирубина.
Литогенез при кальций-оксалатном уролитиазе отличается наличием большого количества патологических взаимосвязей. Не всегда гипероксалурия при МКБ связана с особенностями питания, учитывая наличие эндогенно и экзогенно продуцируемого оксалата. Биологически активный комплекс «Оксалит» снижает уровень экскреции оксалатов в моче как у пациентов с алиментарной, так и у пациентов с идиопатической гипероксалурией. Вероятно, биологически активный комплекс «Оксалит» оказывает комплексное действие на процесс метаболизма оксалатов в организме человека.
Обнаруженные эффекты препарата «Оксалит» позволяют говорить о возможности его применения при противорецидивном лечении больных кальций-оксалатным уролитиазом при сочетании его с употреблением большого объема жидкости (до 2,5 л/сут. и более при отсутствии противопоказаний со стороны других органов и систем) и сбалансированным употреблением кальция: не более 1000-1200 мг в сутки.
ЛИТЕРАТУРА
- Мартов А.Г., Харчилава Р.Р., Акопян Г.Н., Гаджиев Н.К., Мазуренко Д.А., Малхасян В.А. Клинические рекомендации – мочекаменная болезнь 2019 г. М., Российское общество урологов. 73с. URL: https://www.ooorou.ru/public/uploads/ROU/Files/%D0%9A% D0%A0%D0%9C%D0%9A%D0%91%2008.2019.pdf. [Martov A.G., Kharchilava R.R., Akopyan G.N., Gadzhiyev N.K., Mazurenko D.A., Malkhasyan V.A. Clinical guidelines – urolithiasis. 2019 M., Russian Society of Urology. 73 p. URL: https://www.ooorou.ru/public/uploads/ROU/ Files/%D0%9A%D0%A0%D0%9C%D0%9A%D0%91%2008.2019.pdf. nephrolithic potential of resveratrol via inhibition of ROS, MCP-1, (In Russian)]
- Всемирная организация здравоохранения. Неинфекционные заболевания. URL: https://www.who.int/topics/chronic_diseases/ru/ [World Health Organization. Noncommunicable diseases. URL: https://www.who.int/topics/chronic_diseases/ru/ (In Russian)]
- Bird VY, Khan SR. How do stones form? Is unification of theories on stone formation possible? Arch Esp Urol 2017;70(1):12-27
- Wojcikowski K., Stevenson L., Leach D, Wohlmuth H, Gobe G. Antioxidant capacity of 55 medicinal herbs traditionally used to treat the urinary system: a comparison using a sequential threesolvent extraction process. J Altern Complement Med 2007;13(1):103–109.doi: 10.1089/acm.2006.6122
- Яненко Э.К., Константинова О.В., Поляков Н.В., Елагин В.О. Опыт применения пролита септо в комплексном лечении больных мочекаменной болезнью. Урология 2012;(4):5-7. [Yanenko E.K., Konstantinova O.V., Polyakov N.V., Elagin V.O. Experience of use of prolit septo in the complex treatment of patients with urolithiasis. Urologia=Urology 2012;(4):5-7. (In Russian)
- Hong SH, Lee HJ, Sohn EJ, Ko HS, Shim BS, Ahn KS, et al. AntiFiles/%D0%9A%D0%A0%D0%9C%D0%9A%D0%91%2008.2019.pdf. nephrolithic potential of resveratrol via inhibition of ROS, MCP-1, hyaluronan and osteopontin in vitro and in vivo. Pharmacol Rep 2013;65(4):970–979
- Barros ME, Lima R, Mercuri LP, Matos JR, Schor N, Boim MA Effect of extract of Phyllanthus niruri on crystal deposition in experimental urolithiasis. Urol Res 2006;34(6):351-7. doi: 10.1007/s00240-006-0065-1
- Pucci ND, Marchini GS, Mazzucchi E, Reis ST, Srougi M, Evazian D, Nahas WC Effect of phyllanthus niruri on metabolic parameters of patients with kidney stone: a perspective for disease prevention. Int Braz J Urol 2018;44(4):758-764. doi: 10.1590/S1677-5538. IBJU.2017.0521
- JL Nishiura, AH Campos, MA Boim, IP Heilberg, N Schor. Phyllanthus niruri normalizes elevated urinary calcium levels in calcium stone forming (CSF) patients. Urol Res 2004;32(5):362–366. doi: 10.1007/s00240-004-0432-8
- Robertson WG. Do "inhibitors of crystallisation" play any role in the prevention of kidney stones? A critique. Urolithiasis 2017;45(1):43-56. doi: 10.1007/s00240-016-0953-y.
- Freitas AM, Schor N, Boim MA. The effect of Phyllanthus niruri on urinary inhibitors of calcium oxalate crystallization and other factors associated with renal stone formation. BJU Int 2002 Jun;89(9):829-34. doi: 10.1046/j.1464-410x.2002.02794.x
- Micali S, Sighinolfi MC, Celia A, De Stefani S, Grande M, Cicero AF, Bianchi G. Can Phyllanthus niruri affect the efficacy of extracorporeal shock wave lithotripsy for renal stones? A randomized, prospective, long-term study. J Urol 2006 Sep;176(3):1020-2. doi: 10.1016/j.juro.2006.04.010
- Боев И.А. Антимикробная активность морских бурых водорослей. Наука и инновации XXI века. Материалы III Всероссийской конференции молодых ученых. 2016 Издательство: Сургутский государственный университет (Сургут); С. 105-107. [Boyev I.A. Antimicrobial activity of marine brown algae. 21-st Century Science and Innovation. Materialy III Vserossiyskoy konferentsii molodykh uchenykh. 2016 Izdatel'stvo: Surgutskiy gosudarstvennyy universitet (Surgut); P. 105-107.(In Russian)]
- Cushnie TP, Lamb AJ. Recent advances in understanding the antibacterial properties of flavonoids Int J Antimicrob 2011;38(2):99-107. doi: 10.1016/j.ijantimicag.2011.02.014.
- Coothan KV, Anthony J, Sreenivasan PP, Palaninathan V. Physicochemical alterations of urine in experimental hyperoxaluria: a biochemical approach with fucoidan. J Pharm Pharmacol 2007;59(3):419-27. doi: 10.1211/jpp.59.3.0012
- Mi J, Duan J, Zhang J, Lu J, Wang H, Wang Z. Evaluation of antiurolithic effect and the possible mechanisms of Desmodium styracifolium and Pyrrosiae petiolosa in rats. Urol Res 2012;40(2):151-61. doi: 10.1007/s00240-011-0401-y.







