ВВЕДЕНИЕ
Брахитерапия при раке предстательной железы (РПЖ) выполняется более чем в 20 клиниках РФ с применением в основном зарубежных микроисточников (МИ). До 2015 года основное количество МИ с йодом-125 закупалось за рубежом. Позднее МИ стала выпускать компания ЗАО «НаноБрахиТех», г. Дубна. Однако высокая стоимость реализуемых в России микроисточников не позволяет увеличивать количество проводимых операций брахитерапии и, тем более, широко тиражировать данную методику в России.
В данной статье отражены основные этапы развития производства, клинических испытаний МИ, разработанных АО «ГНЦ РФ – ФЭИ» (IPРE SEED), оценка их эффективности и безопасности применения для медицинского персонала путем получения данных о локальных дозах облучения, а также сравнение отечественных МИ с зарубежными аналогами.
МАТЕРИАЛЫ И МЕТОДЫ
Микроисточник «IPPE SEED», разработанный в АО «ГНЦ РФ – ФЭИ», представляет собой покрытый тонким слоем радиоактивного йода-125 серебряный стержень, герметично запаянный в титановую капсулу (рис. 1).
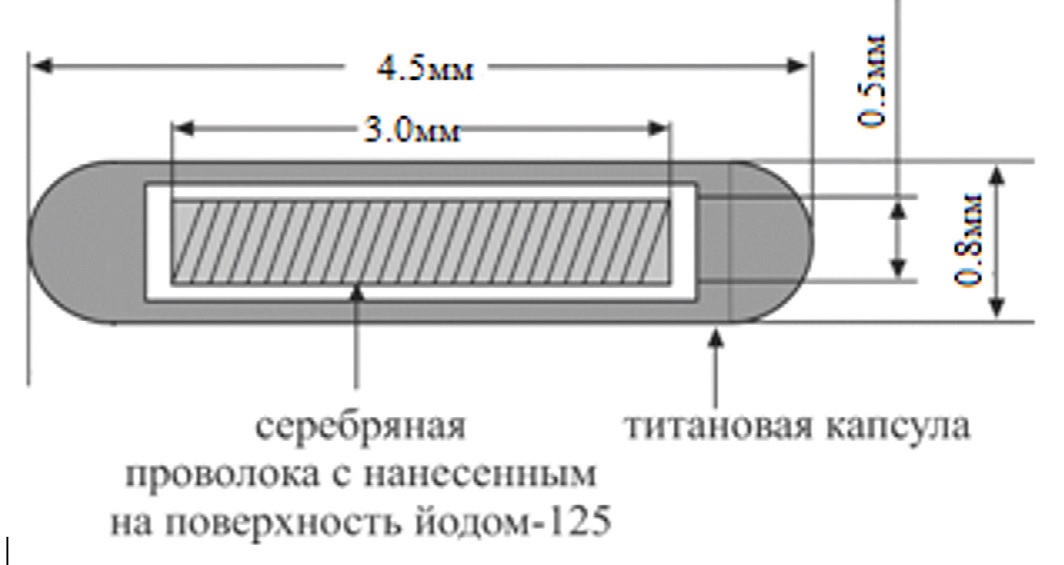
Рис. 1. Микроисточник «IPPE SEED»
Fig. 1. Microsource «IPPE SEED»
Разработчиками были учтены достоинства известных иностранных МИ. Было проведено сравнение свойств и характеристик МИ «IPPE SEED» и «OncoSeed 6711» фирмы ONCURA. Конструктивные характеристики МИ представлены в таблице 1 [1].
Таблица 1. Конструктивные характеристики микроисточников
Table 1. Design characteristics of microsources
| Параметры Parameters |
Тип микроисточников Microsource type |
|
|---|---|---|
| IPPE SEED | OncoSeed 6711 | |
| Длина, мм Length, mm |
4,50 | 0,41±0,12 |
| Диаметр, мм Diameter, mm |
0,8 | 0,76±0,16 |
| Длина активной части, мм Active part length, mm |
3,00 | 0,62±0,23 |
| Толщина стенки, мм Wall thickness, mm |
0,05 | 0,68±0,39 |
| Материал основы активной части Base material of the active part |
Серебряная проволока Silver wire |
Серебряная проволока Silver wire |
| Диаметр основы активной части, мм Active part base diameter, mm |
0,5 | 0,5 |
| Химическое соединение, нанесенный на основу активной части Chemical compound applied to the base of the active part |
AgI | AgI и AgBr |
| Толщина слоя активного химического соединения, мкм Active chemical compound layer thickness, microns |
8∙10-3 | 1,75 |
I-125 претерпевает электронный захват с периодом полураспада 59,43 суток и средней энергией фотонного излучения равной 28,33 кэВ [2].
Излучаемые при распаде электроны внутренней конверсии и Ожэ-электроны полностью поглощаются в материале герметичной капсулы источника. Слой половинного ослабления фотонного излучения в мягких тканях организма – около 2 см [2]. Для изготовления корпуса МИ используется титановая трубка Ø 0,8×0,05 мм. Вкладыши изготовлены из серебряной проволоки Ø 0,5 мм марки Ср 999,9 ГОСТ 6836. Герметизация корпуса МИ осуществляется титановыми шариками и сварными швами, образующимися при оплавлении кромок. Толщина слоя нанесенной активности микроисточника составляет 8,0×10-3 мкм или 80 Ǻ слоя материала AgI, соответствующего значению нанесенной активности в 1 мКи [3].
На рисунке 2 представлены линии уровня мощности поглощенной дозы (изодозы) в воде от одиночного микроисточника. Результаты нормированы на нанесенную активность, равную 1 мКи [4].
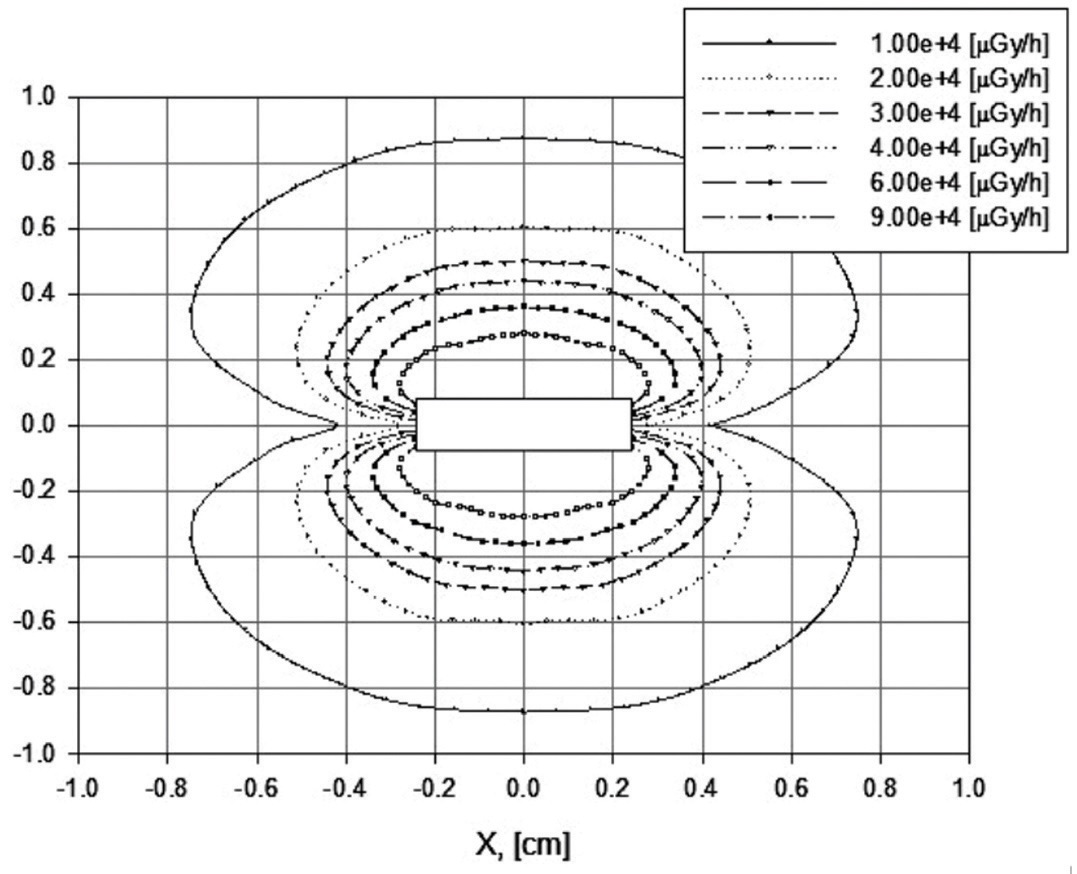
Рис. 2. Изолинии мощности поглощенной дозы в воде от микроисточника
Fig. 2. Isolines of the absorbed dose rate in water from a microsource
На базе Физико-энергетического института имени А.И. Лейпунского создано опытно-промышленное производство МИ, мощностью до 50 тыс. изделий в год [5]. Для учета, контроля и движения МИ по технологическим участкам и формирования сопроводительной документации на поставки МИ потребителям используется электронная база данных, которая позволяет прослеживать информацию по произведенным в АО «ГНЦ РФ – ФЭИ» микроисточникам (данные о сырье; даты изготовления, сварки, герметизации, стерилизации, сортировки, упаковки; номера паспортов; даты отправки заказчикам; информацию по отбракованным МИ и т.д.), а также информацию о потенциальных потребителях МИ (рис. 3).
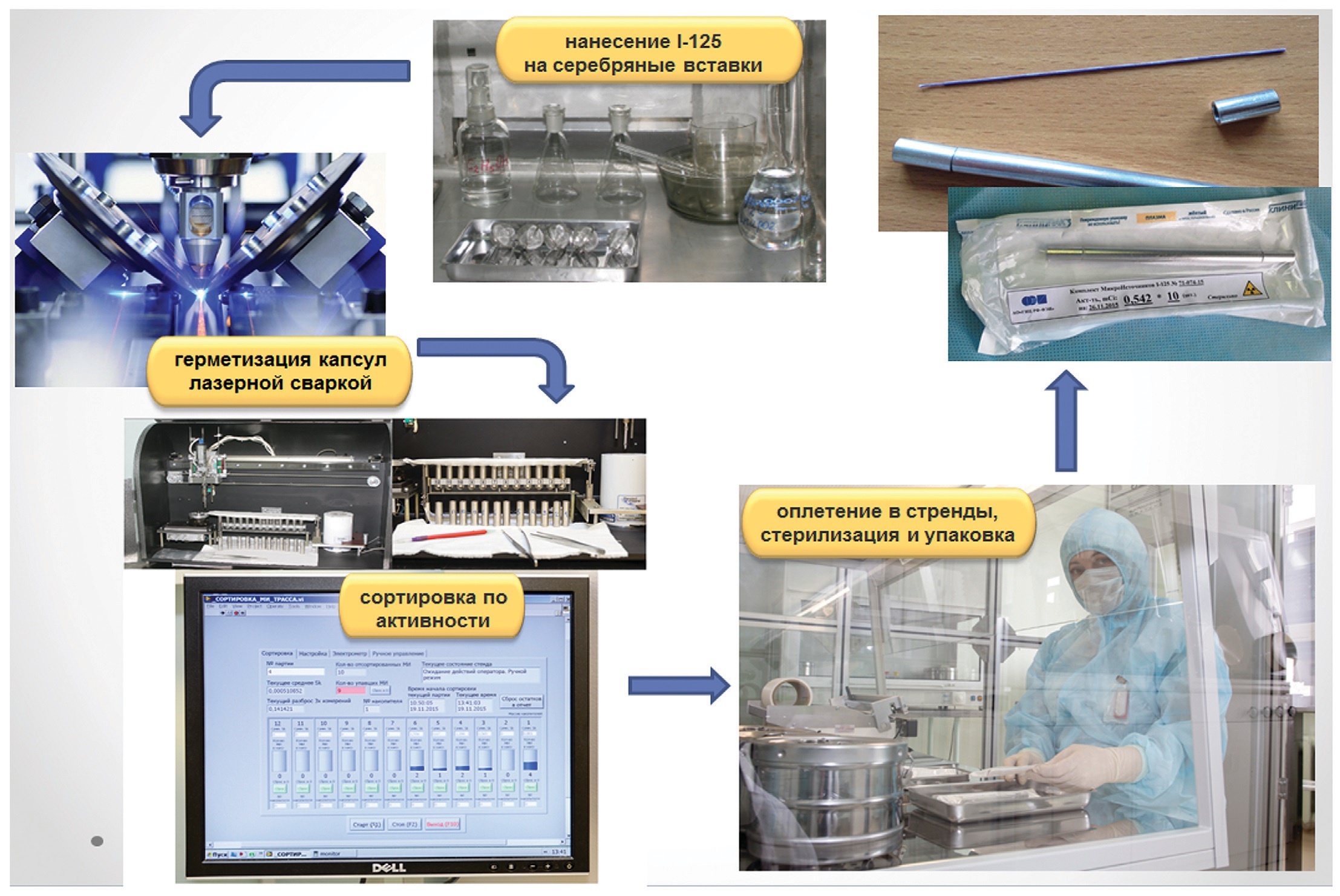
Рис. 3. Технологическая схема процесса производства микроисточников ФЭИ
Fig. 3. Technological scheme of the production process of IPPE SEED microsources
В целях оценки безопасности микроисточников «IPPE SEED» для медицинского персонала при проведении брахитерапии осуществлен локальный дозиметрический контроль во время операции [6]. Для этого были применены термолюминесцентные дозиметры на основе кристаллов оксида алюминия. Дозиметры размещались на всех пальцах обеих рук персонала, а также на очковой оправе – вблизи внешних углов левого и правого глаза и напротив переносицы оперирующего персонала. Сборки дозиметров закрепляются так, чтобы не создавать помех работе оператора (рис. 4) [2].

Рис. 4. Размещение сборок дозиметров для измерений локальных доз облучения пальцев и глаз оператора
Fig. 4. Placement of assemblies of dosimeters for measuring local doses of radiation to the fingers and eyes of the operator
В связи с отсутствием российского аналога программы планирования операций по брахитерапии физические характеристики микроисточников производства АО «ГНЦ РФ — ФЭИ» (IPPE SEED) были внесены в соответствии с информацией, полученной от производителя, в базу данных программного обеспечения (VarySeed и PSID), что позволило в дальнейшем использовать ее при планировании операций с отечественными микроисточниками.
РЕЗУЛЬТАТЫ
В 2015 году силами трех филиалов ФГБУ «НМИЦ радиологии» Минздрава России в рамках клинических испытаний 36 пациентам была проведена брахитерапия источниками I-125 производства АО «ГНЦ РФ — ФЭИ». Параллельно с клиническими испытаниями был выполнен дозиметрический контроль с целью оценки безопасности МИ «IPPE SEED». Полученные в ходе испытаний результаты продемонстрировали полную безопасность отечественных источников для медперсонала, проводящего брахитерапию.
Пациенты были рандомизированы по степени онкологического риска прогрессии РПЖ. Группу низкого онкологического риска (благоприятный прогноз по классификации D’Amico) составили 30 (83,3%) пациентов, умеренного риска – 6 (16,7%) больных [7]. Возраст пациентов колебался от 54 до 79 лет (средний возраст 64,6 года), уровень простатспецифического антигена (ПСА) – от 2,3 до 18 нг/мл, в среднем 8 нг/мл, объем предстательной железы до брахитерапии колебался от 15 до 60 см3 (средний 35 см3). Максимальная скорость потока мочи, оцениваемая по результатам урофлоуметрии, проводимой до начала исследования, варьировала от 10 до 31 мл/с, составив в среднем 15,8 мл/с (табл. 2).
Таблица 2. Исходные данные пациентов
Table 2. Initial data of patients
| № п/п |
ФИО пациента Full name of the patient |
Возраст на момент проведения исследования,годы Age at the time of the study, years |
Диагноз по TNM Diagnosis by TNM |
Начальный уровень ПСА Initial PSA level |
Объем предстательной железы, см3 Prostate volume, cm3 | Баллы по Глисону Gleason score |
Тазовая лимфаденэктомия Pelvic lym-phadenectomy |
Qmax |
|---|---|---|---|---|---|---|---|---|
| 1. | СИИ | 79 | Т1сN0M0 | 9,7 | 20 | 6 | Нет | 15 |
| 2. | ЕАА | 66 | Т1сN0M0 | 6 | 30 | 6 | Нет | 17 |
| 3. | НАС | 64 | T2aN0M0 | 8,2 | 45 | 6 | Нет | 31 |
| 4. | МНС | 77 | Т1сN0M0 | 8,6 | 36 | 6 | Нет | 24 |
| 5. | ЧВА | 62 | Т2aN0M0 | 4,6 | 46 | 6 | Нет | 16 |
| 6. | КВН | 62 | Т1сN0M0 | 7,6 | 30 | 6 | Нет | 22 |
| 7. | ГНН | 57 | Т1сN0M0 | 6,8 | 45 | 6 | Нет | 21 |
| 8. | МАИ | 57 | Т2сN0M0 | 18 | 20 | 7 | Да | 15 |
| 9. | ГВМ | 57 | Т2аN0M0 | 8 | 34 | 7 | Да | 17,3 |
| 10. | ЛГИ | 80 | Т1сN0M0 | 8,6 | 34 | 6 | Нет | 12 |
| 11. | КВВ | 62 | Т2аN0M0 | 6,4 | 30 | 7 | Да | 12,2 |
| 12. | РВН | 76 | Т1сN0M0 | 6,9 | 28 | 6 | Нет | 26 |
| 13. | КМА | 60 | Т2аN0М0 | 9,2 | 25 | 6 | Нет | 16 |
| 14. | КВП | 66 | Т1сN0M0 | 8,1 | 28 | 6 | Нет | 17,2 |
| 15. | ВЕА | 61 | T2aN0M0 | 7,1 | 36 | 6 | Нет | 16 |
| 16. | БЕМ | 57 | Т1сN0M0 | 6,4 | 27 | 6 | Нет | 16 |
| 17. | МНФ | 65 | T2bN0M0 | 3,8 | 42 | 6 | Нет | 18 |
| 18. | СВМ | 69 | T2bN0M0 | 14 | 60 | 6 | Да | 14 |
| 19. | МВВ | 75 | T2bN0M0 | 2,7 | 15 | 6 | Нет | 13 |
| 20. | КВВ | 62 | T2aN0M0 | 6,7 | 48 | 7 | Да | 24 |
| 21. | ПВА | 54 | T2aN0M0 | 4,2 | 45 | 7 | Да | 15 |
| 22. | УМБ | 61 | T2aN0M0 | 3,5 | 35 | 7 | Нет | 18 |
| 23. | ВСМ | 61 | Т2вN0М0 | 6 | 30 | 6 | Нет | 10 |
| 24. | ЕОМ | 67 | Т2вN0М0 | 6,4 | 29 | 6 | Нет | 12 |
| 25. | КЮВ | 55 | Т2аN0М0 | 15 | 37 | 6 | Нет | 17,1 |
| 26. | НСК | 69 | T2aN0M0 | 6 | 38 | 6 | Нет | 21,6 |
| 27. | ТВФ | 74 | Т2вN0М0 | 11,4 | 50 | 6 | Нет | 10,4 |
| 28. | ЧШЩ | 66 | Т2аN0М0 | 6,1 | 37 | 6 | Нет | 10,4 |
| 29. | ААА | 54 | Т2аN0М0 | 8,7 | 40 | 6 | Нет | 12 |
| 30. | АБВ | 68 | Т2аN0М0 | 7 | 41 | 6 | Нет | 12 |
| 31. | БИА | 54 | Т2аN0М0 | 7 | 25 | 6 | Нет | 10 |
| 32. | СИА | 73 | Т2аN0М0 | 9,4 | 29 | 6 | Нет | 10,9 |
| 33. | СТУ | 68 | Т2N0M0 | 9,2 | 44 | 6 | Нет | 16 |
| 34. | ХЦЧ | 79 | Т2N0M0 | 9,8 | 43 | 6 | Нет | 12 |
| 35. | ТГВ | 67 | Т2вN0М0 | 15 | 50 | 6 | Нет | 10 |
| 36. | КЛН | 61 | Т2аN0М0 | 6,6 | 33 | 6 | Нет | 10,7 |
| Среднее | 64,4 | 8 | 35 | 6,16 | 15,8 | |||
Все пациенты перед включением в исследование подписывали информированное согласие. Больные были проинформированы о методике проведения брахитерапии, возможных побочных реакциях и мерах их предупреждения.
Пациентам в группе благоприятного прогноза брахитерапию проводили в монорежиме. Суммарная очаговая доза (СОД) облучения составила 145 Гр. При имплантации были использованы источники I-125 двух активностей – 0,55 и 0,35 мКи. В зависимости от объема предстательной железы применялось от 40 до 80 микроисточников (в среднем 57). Время имплантации в среднем составило 85 минут. Длительность пребывания пациента в стационаре не превышала 2 суток.
В группе промежуточного прогноза низкомощностная брахитерапия была проведена в комбинации с лапароскопической тазовой лимфаденэктомией, которую выполняли за 4–5 недель до имплантации микроисточников.
По результатам контрольного обследования через 6 месяцев после проведенной брахитерапии уровень ПСА у всех пациентов снизился в среднем на 87% от исходного.
Отмеченные в ходе исследования побочные реакции проявлялись в основном в явлениях дизурии 1-й степени по классификации RTOG/EORTC. Только у 1 (2,7%) из 36 пациентов через месяц после брахитерапии развилась острая задержка мочи, потребовавшая катетеризации мочевого пузыря. В последствии восстановить самостоятельный акт мочеиспускания у этого пациента удалось консервативными методами. Проявлений гастроинтестинальной токсичности среди пролеченных пациентов зарегистрировано не было.
Наблюдение за пациентами было продолжено с целью получения отдаленных результатов лечения [8].
На срок наблюдения 60 месяцев (5 лет) безрецидивная выживаемость по уровню ПСА составила 94,4%. У 2 пациентов был диагностирован рецидив заболевания. Средний уровень ПСА через 5 лет после проведенной брахитерапии составил 0,3 нг/мл (от 0,8 до 0,01 нг/мл). Общая 5-летняя выживаемость составила 91,6%. Это связано со смертью 3 пациентов старше 80 лет от сопутствующих заболеваний без рецидива РПЖ. Основными проявлениями поздней лучевой токсичности были лучевой цистит и уретрит 1-2 степени по RTOG/EORTC у 4 пациентов, а также явления лучевого ректита 2 степени у 1 пациента (табл. 3).
Таблица 3. Результаты 5-летнего наблюдения за пациентами, принявшими участие в испытаниях российских микроисточников I-125
Table 3. Results of 5-year follow-up of patients who took part in the trials of Russian microsources I-125
| Исследуемый параметр The investigated parameter |
Значение параметра Parameter value |
|---|---|
| Количество пациентов Number of patients |
36 |
| Биохимическая безрецидивная 5-летняя выживаемость Biochemical disease-free survival for 60 months (5 years) |
94,4% (34 пациента) |
| Общая 5-летняя выживаемость Overall survival at 60 months (5 years) |
91,6% (33 пациента) |
| Лучевой цистит, уретрит I II ct. (RNOG) Radiation cystitis, urethritis, stage I II. |
11,1% (4 пациента) |
| Лучевой ректит II ct. (RNOG) Radiation rectitis, stasge II. II ct. (RTOG) |
2,7% (1 пациент) |
Параллельно клиническим испытаниям был проведен дозиметрический контроль с целью оценки безопасности российских МИ I-125. Полученные в результате измерений локальные дозы облучения онколога-радиолога при проведении брахитерапии представлены в таблице 4.
Таблица 4. Результаты измерений локальных доз облучения онколога-радиолога при проведении операции
Table 4. Results of measurements of local radiation doses of an oncologist-radiologist during an operation
| Локализация дозиметров Localization of dosimeters |
Накопленная доза, мГр (указанные погрешности - 1 SD) Accumulated dose, mGy (indicated errors - 1 SD) |
Накопленная доза, нормированная на время работы хирурга-онколога-радиолога и суммарную активность источников 125I, [мГр/(мин*МБк)]*10-6(указанные погрешности - 1 SD) Accumulated dose, normalized to the operating time of the radiological surgeon and the total activity of 125I sources, [mGy / (min* MBq)]* 10-6 (specified errors - 1 SD) |
|---|---|---|
| Большой палец правой руки Right thumb |
0,13±0,014 | 1,6±0,18 |
| Указательный палец правой руки Right index finger |
0,25±0,026 | 3,1±0,33 |
| Средний палец правой руки Right middle finger |
0,33±0,033 | 4,2±0,41 |
| Безымянный палец правой руки Ring finger of the right hand |
0,19±0,021 | 2,4±0,26 |
| Мизинец правой руки Right little finger |
0,15±0,016 | 1,8±0,19 |
| Большой палец левой руки Left thumb |
0,37±0,038 | 4,7±0,48 |
| Указательный палец левой руки Left index finger |
0,52±0,051 | 6,5±0,64 |
| Средний палец левой руки Left middle finger |
0,48±0,049 | 6,1±0,62 |
| Безымянный палец левой руки Ring finger of the left hand |
0,34±0,038 | 4,3±0,48 |
| Мизинец левой руки Left little finger |
0,26±0,029 | 3,2±0,36 |
| Правый глаз Right eye |
0,32±0,032 | 4,0±0,40 |
| Переносица Nasal bridge |
0,10±0,010 | 1,2±0,12 |
| Левый глаз Left eye |
0,10±0,011 | 1,2±0,13 |
Длительность работы онколога-радиолога во время подготовки источников и операции – 0,983 ч, суммарная активность источников – 1426 МБк. В таблице 4 приведены результаты исходных измерений.
Результаты измерений локальных доз облучения медицинского физика при подготовке к операции представлены в таблице 5.
Таблица 5. Результаты измерений локальных доз облучения медицинского физика при подготовке к операции
Table 5. Results of measurements of local radiation doses of a medical physicist in preparation for surgery
| Локализация дозиметров Localization of dosimeters |
Накопленная доза, мГр (указанные погрешности - 1 SD) Accumulated dose, mGy (indicated errors - 1 SD) |
|---|---|
| Большой палец правой руки Right thumb |
0,067±0,0083 |
| Указательный палец правой руки Right index finger |
0,19±0,016 |
| Средний палец правой руки Right middle finger |
0,062±0,009 |
| Безымянный палец правой руки Ring finger of the right hand |
0,038±0,0030 |
| Мизинец правой руки Right little finger |
0,043±0,0085 |
| Большой палец левой руки Left thumb |
0,090±0,0098 |
| Указательный палец левой руки Left index finger |
0,47±0,09 |
| Средний палец левой руки Left middle finger |
0,20±0,019 |
| Безымянный палец левой руки Ring finger of the left hand |
0,12±0,013 |
| Мизинец левой руки Left little finger |
0,071±0,009 |
Из полученных данных следует, что даже максимальные величины измеренных локальных поглощенных доз не представляют радиационной опасности при использовании для брахитерапии МИ «IPPE SEED», так как, согласно НРБ-99/2009, годовые пределы дозы для населения составляют 50 мЗв в год в кистях, стопах и коже и 15 мЗв в год – для глаз. Для персонала (группы А и Б) эти пределы еще выше: в 2,5 и 10 раз соответственно [9].
В таблицах 6 и 7 приведены результаты измерений локальных доз облучения пальцев обеих рук и глаз онколога-радиолога и медицинского физика при работе с импортными микроисточниками соответственно.
Таблица 6. Результаты измерений локальных доз облучения онколога-радиолога при проведении операции с импортными микроисточниками
Table 6. Results of measurements of local radiation doses of an oncologist-radiologist during surgery with imported microsources
| Локализация дозиметров Localization of dosimeters |
Накопленная доза, мГр (указанные погрешности - 1 SD) Accumulated dose, mGy (indicated errors - 1 SD) |
Накопленная доза, нормированная на время работы хирурга-онколога-радиолога и суммарную активность источников [мГр/(мин*МБк)]*10-6(указанные погрешности - 1 SD) Accumulated dose, normalized to the operating time of the radiological surgeon and the total activity of 125I sources, [mGy / (min* MBq)]* 10-6 (specified errors - 1 SD) |
|---|---|---|
| Большой палец правой руки Right thumb |
0,15±0,014 | 1,8±0,17 |
| Указательный палец правой руки Right index finger |
0,25±0,026 | 3,0±0,32 |
| Средний палец правой руки Right middle finger |
0,27±0,035 | 3,2±0,42 |
| Безымянный палец правой руки Ring finger of the right hand |
0,16±0,022 | 1,9±0,27 |
| Мизинец правой руки Right little finger |
0,15±0,016 | 1,8±0,18 |
| Большой палец левой руки Left thumb |
0,43±0,041 | 5,1±0,52 |
| Указательный палец левой руки Left index finger |
0,45±0,055 | 5,4±0,71 |
| Средний палец левой руки Left middle finger |
0,46±0,051 | 5,5±0,62 |
| Безымянный палец левой руки Ring finger of the left hand |
0,37±0,040 | 4,4±0,49 |
| Мизинец левой руки Left little finger |
0,25±0,030 | 2,3±0,29 |
| Правый глаз Right eye |
0,31±0,034 | 3,7±0,42 |
| Переносица Nasal bridge |
0,090±0,011 | 1,1±0,14 |
| Левый глаз Left eye |
0,092±0,0090 | 1,1±0,12 |
Таблица 7. Результаты измерений локальных доз облучения медицинского физика при подготовке к операции с импортными микроисточниками
Table 7. Results of measurements of local radiation doses of a medical physicist in preparation for an operation with imported microsources
| Локализация дозиметров Localization of dosimeters |
Накопленная доза, мГр (указанные погрешности - 1 SD) Accumulated dose, mGy (indicated errors - 1 SD) |
|---|---|
| Большой палец правой руки Right thumb |
0,068±0,0079 |
| Указательный палец правой руки Right index finger |
0,15±0,018 |
| Средний палец правой руки Right middle finger |
0,067±0,008 |
| Безымянный палец правой руки Ring finger of the right hand |
0,047±0,0035 |
| Мизинец правой руки Right little finger |
0,052±0,0093 |
| Большой палец левой руки Left thumb |
0,13±0,012 |
| Указательный палец левой руки Left index finger |
0,35±0,07 |
| Средний палец левой руки Left middle finger |
0,17±0,020 |
| Безымянный палец левой руки Ring finger of the left hand |
0,11±0,014 |
| Мизинец левой руки Left little finger |
0,090±0,011 |
ОБСУЖДЕНИЕ
Клинические испытания российских МИ продемонстрировали их безопасность для пациентов и медицинского персонала, что было доказано проведением дозиметрического контроля во время самой процедуры, а также при обследовании пациентов после проведения брахитерапии. Проведенный локальный дозиметрический контроль показал, что локальные дозы облучения медицинского персонала при применении в тех же условиях микроисточников «IPPE SEED» не отличаются от импортных микроисточников в пределах погрешностей измерений [2].
Эффективность отечественных МИ I-125 при проведении низкомощностной брахитерапии демонстрируется снижением уровня ПСА от исходного на 87% в срок наблюдения 6 месяцев. Безрецидивная биохимическая 5- летняя выживаемость составила 94,4%. Важным является отсутствие значимых лучевых реакций как в ранний, так и в поздний послеоперационный период. Следует отметить, что данные обследований, проведенные пациентам после низкомощностной брахитерапии МИ «IPPE SEED», доказывают их клиническую эффективность, безопасность и соответствие отечественных микроисточников I-125 международным стандартам. Низкая стоимость микроисточников производства АО «ГНЦ РФ – ФЭИ» относительно зарубежных аналогов позволяет увеличить число ежегодно проводимых операций, а также дает перспективы открытия новых подразделений, проводящих операции внутритканевой лучевой терапии.
ВЫВОДЫ
Микроисточники, разработанные АО «ГНЦ РФ – ФЭИ», успешно прошли клинические испытания, в течение которых доказана безопасность их применения для медицинского персонала. Проведенное исследование также продемонстрировало высокие показатели безрецидивной выживаемости и невысокий уровень побочных реакций у пролеченных пациентов.
ЛИТЕРАТУРА
1. Tanaka K., Kamo K., Tateoka K., Asanuma O., Sato K., Takeda H., Sakata K., Takada J. A comparison of the dose distributions between the brachytherapy 125I source models, STM1251 and Oncoseed 6711, in a geometry lacking radiation equilibrium scatter conditions. J Radiat Res 2015;56(2):366-71. https://doi.org/10.1093/jrr/rru088.
2. Степаненко В.Ф., Бирюков В.А., Карякин О.Б., Каприн А.Д., Галкин В.Н., Иванов С.А. и др. Локальные поглощенные дозы облучения медицинского персонала при брахитерапии рака предстательной железы микроисточниками125I российского производства. Радиация и риск (Бюллетень Национального радиационно-эпидемиологического регистра) 2017;26(1):44-59. [Stepanenko V.F., Biryukov V.A., Karjakin O.B., Kaprin A.D., Galkin V.N., Ivanov S.A., et al. Local absorbed doses of irradiation of medical personnel at brachytherapy of prostate cancer using 125I microsources of Russian production. Radiatsiya i risk (Byulleten' Natsional'nogo radiatsionno-epidemiologicheskogo registra) = The Bulletin «Radiation and Risk» 2017;26(1):44-59. https://doi.org/10.21870/0131-3878-2017-26-1-44-59. (In Russian)].
3. Нерозин Н.А., Пышко А.П., Шаповалов В.В. Расчетные исследования пространственного распределения мощности поглощенной дозы в опухоли и окружающих ее тканях для различных микроисточников. Исследования и практика в медицине 2015;2(4):41-49. [Nerozin N.A., Pyshko A.P., Shapovalov V.V. Calculation studies of spatial distribution of the absorbed dose rate for various seeds. Issledovaniya i praktika v meditsine = Research and Practical Medicine Journal 2015;2(4):41-49. (In Russian)].
4. Оборин А.В., Трофимчук С.Г., Виллевальде А.Ю., ЯковенкоА.А. Измерение мощности кермы в воздухе от микроисточников медицинского назначения на основе радионуклида 125I. Медицинская физика 2016;3(71):40-48. [Oborin A.V., Trofimchuk S.G., Villevalde A.Y., Yakovenko A.A. Air kerma rate measurement for i-125 medical microsources. Meditsinskaya Fizika = Medical Physics 2016;3(71):40-48. (In Russian)].
5. Подсобляев Д.А., Нерозин Н.А., Шаповалов В.В., Яковщиц Ю.А., Болонкин А.С., Дунин А.В., Говердовский А.А. Электрохимическое осаждение 125I на серебряные подложки микроисточников. Biomedical Photonics 2015;4(4):17-20. [Podsoblyaev D.A., Nerozin N.A., Shapovalov V.V., Yakovschits Yu.A., Bolonkin A.S., Dunin A.V., Goverdovskiy A.A. Electrochemical plating of i125 on silver matrix for microsources. Biomedical Photonics 2015;4(4):17-20. (In Russian)].
6. Nath R., Anderson L.L., Luxton G., Weaver K.A., Williamson J.F., Meigooni A.S. Dosimetry of interstitial brachytherapy sources: Recommendations of the AAPM Radiation Therapy Committee Task Group No. 43. Med Phys 1995;22(2):209-34. https://doi.org/10.1118/1.597458.
7. European Assosiation of Urology. Guidelines 2016.
8. Каприн А.Д., Галкин В.Н., Иванов С.А., Карякин О.Б., Бирюков В.А., Обухов А.А. и др. Низкомощностная контактная лучевая терапия (брахитерапия) рака предстательной железы отечественными микроисточниками I-125 в монорежиме и в комбинации с тазовой лимфаденэктомией. Урология 2017(1):38-42. [Kaprin A.D., Galkin V.N., Ivanov S.A., Karyakin O.B., Biryukov V.A., Obukhov A.A. et al. Low dose-rate contact radiation therapy (brachytherapy) for prostate cancer using domestic i-125 seeds as a monotherapy and combined with pelvic lymphadenectomy. Urologiya = Urologiia 2017(1):38-42. https://dx.doi.org/10.18565/urol.2017.1.38-42. (In Russian)].
9. Нормы радиационной безопасности (НРБ-99/2009). СанПин 2.6.1.252309. М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора 2009; 100 с. Radiation safety standards (NRB-99/2009). SanPin 2.6.1.252309. Moscow: Federal Center for Hygiene and Epidemiology of Rospotrebnadzor 2009; 100 p. (In Russian)].







