ВВЕДЕНИЕ
Мочекаменная болезнь (МКБ) является одним из наиболее распространенных заболеваний органов мочеполовой системы. В мире МКБ диагностируется у 2-20% населения, при этом у 30-50% пациентов в течение ближайших 5 лет после лечения развивается рецидив данного заболевания [1]. Во всех регионах Российской Федерации отмечается стойкая тенденция к росту заболеваемости МКБ [2].
Увеличение числа пациентов с МКБ сопровождается повышением социально-экономического бремени для системы здравоохранения и требует поиска оптимальной лечебной тактики для достижения лучшего результата при минимизации затрат на лечение пациентов с данной патологией [3, 4].
МКБ – заболевание, в генезе которого играют роль различные этиологические факторы. Патогенетические механизмы, способствующие образованию конкрементов, разнообразны [5, 6]. В настоящее время доказана генетическая предрасположенность к формированию конкрементов в мочевыводящих путях, выявлена связь ожирения и уролитиаза, выяснена роль инфекций мочевыводящих путей в развитии МКБ [7-9]. Особое место в генезе МКБ отводят метаболическому синдрому, являющемуся катализатором обширного ряда патологических состояний, таких как сахарный диабет, сердечно-сосудистые и онкологические заболевания и т.д. Некоторые из этих заболеваний могут как способствовать формированию мочевых конкрементов сами по себе, так и ограничивать возможность применения методов лечения пациентов [10].
Учитывая разнообразие этиопатогенеза МКБ и наличие у пациентов с камнями мочевыводящих путей клинически значимой сопутствующей патологии, существенно повышающей операционноанестезиологический риск, необходим персонализированный подход к выбору оптимальной тактики лечения МКБ в каждом конкретном клиническом случае.
Цель исследования – анализ опыта лечения пациентов с МКБ и сопутствующими заболеваниями, оценка возможности персонализированного подхода к выбору метода лечения уролитиаза.
МАТЕРИАЛЫ И МЕТОДЫ
Проведен ретроспективный анализ результатов лечения 208 пациентов, 124 (59,6%) мужчин и 84 (40,4%) женщин, в возрасте от 19 до 84 лет (средний возраст – 53,5±14,6 года), которым в период с 2021 по 2023 гг. в отделениях урологии Национального медицинского исследовательского центра хирургии им. А.В. Вишневского и городской клинической больницы им. А.К. Ерамишанцева Департамента здравоохранения г. Москвы выполнены различные оперативные вмешательства по поводу МКБ.
Предоперационное обследование пациентов включало сбор жалоб, анамнеза заболевания и жизни, физикальные методы, общеклинические анализы крови и мочи, биохимический анализ крови, посев мочи, ультразвуковое исследование почек и мочевого пузыря, а также компьютерную томографию (КТ) органов брюшной полости и забрюшинного пространства с контрастным усилением (при наличии противопоказаний к введению йодсодержащего рентгенконтрастного препарата проводилось нативное исследование), электрокардиографию, рентгенографию органов грудной полости, консультацию профильных специалистов в зависимости от характера сопутствующей патологии пациента.
Полученные клинические данные заносились в специально разработанную базу данных. Для их анализа использовались методы описательной статистики.
РЕЗУЛЬТАТЫ
Демографические данные пациентов, включенных в исследование, представлены в таблице 1. Более половины (n=127, 61,0%) пациентов были трудоспособного возраста (рис. 1).
Распределение пациентов по возрасту представлено на рисунках 1А и 1Б.
Сопутствующие заболевания имели место у 34 (16,3%) пациентов, у половины (7,7%) – отмечены множественные сопутствующие заболевания. Коморбидный фон пациентов представлен в таблице 2. Наиболее часто встречались гиперлипидемия – в 108 (52%) случаях и гипертоническая болезнь – у 52 (25%) пациентов. Сахарный диабет верифицирован у 15 (7%), подагра – у 3 (1,4%), гипотиреоз – у 2 (0,9%) пациентов. Медиана индекса коморбидности Чарлсон (ИКЧ) для выборки составила 4,7 (0-9). У 84 (40,4%) пациентов в анамнезе имели место инфекционно-воспалительные заболевания мочевыделительной системы (пиелонефрит, цистит), 91 (43,7%) больных ранее перенесли операции на органах мочеполовой системы (литотрипсия, литоэкстракция, аденомэктомия, простатэктомия, стентирование мочеточника, нефростомия). В 7 случаях выявлены уродинамически значимые заболевания: 4 (1,9%) случая доброкачественной гиперплазии предстательной железы (ДГПЖ), 2 (0,9%) – крупная миома матки, 1 (0,05%) – стриктура мочеточника (табл. 2).
Таблица 1. Демографические данные пациентов
Table 1. Demographic data of patients
| Показатели Features |
Всего (n=208) Total (n=208) |
Мужчины (n = 124) Мen (n = 124) |
Женщины (n = 84) Women (n = 84) |
|---|---|---|---|
| Средний возраст, годы (M±σ) Mean age, years (M±σ) |
53,5±14,6 | 53,6±14,2 | 55,0±16,2 |
| Предшествующие оперативные вмешательства по поводу МКБ, n Previous surgeries for urolithiasis, n |
91 | 45 | 46 |

Рис. 1. Распределение пациентов по возрасту в соответствии с классификацией ВОЗ: A – всей группы, Б – отдельно мужчин и женщин
Fig. 1. Distribution of patients by age in accordance with the WHO classification: A – for the whole group, Б – for men and women separately
Медиана количества выявленных конкрементов составила 3 (1-12). У 10 (4,8%) конкременты почек были множественными. В 97 (46,6%) случаев процесс был правосторонним, в 102 (49,0%) – левосторонним, у 9 (4,3%) пациентов камни выявлены в обеих почках. В 92 (44,2%) случаях верифицированы конкременты мочеточников. Средний размер конкрементов составил 11,2 (3-68) мм. Среднее значение плотности конкрементов, по данным КТ, составило 861,2±382,4 HU. В 4 (1,9%) случаях показатели плотности (500-900 HU) и кислотности мочи (≤5,5) у пациентов с коралловидными конкрементами (К4) позволили первым этапом провести литолитическую терапию цитратными смесями длительностью 3 месяца с достижением целевых значений кислотности (6,8-7,1). После уменьшения размеров конкремента на фоне цитратной терапии трем больным выполнены перкутанная нефролитотрипсия (ПНЛТ) и одному пациенту проведено ретроградное интраренальное хирургическое вмешательство (РИРХ).
Таблица 2. Коморбидный фон пациентов
Table 2. Patients’ comorbitity
| Заболевания и состояния Diseases and conditions |
n | % |
|---|---|---|
| Системные заболевания Systemic diseases |
||
| Гиперлипидемия Hyperlipidemia |
108 | 52 |
| Гипертоническая болезнь Arterial hypertension |
52 | 25 |
| Сахарный диабет Diabetes mellitus |
15 | 7 |
| Подагра Gout |
3 | 1,4 |
| Гипотиреоз Hypothireosis |
2 | 0,9 |
| Уродинамически значимые заболевания Urodynamic significant diseases |
||
| Инфекционно-воспалительные заболевания мочевыделительной системы UTI |
84 | 40,4 |
| Доброкачественная гиперплазия предстательной железы Benign prostate hyperplasia |
4 | 1,9 |
| Крупные миомы матки Large uterine fibroids |
2 | 0,9 |
| Стриктура мочеточника Ureteral stricture |
1 | 0,05 |
В 42 (20,2%) случаях удалось провести инфракрасную спектрометрию извлеченных конкрементов. Камни с однородным и близким к однородному составом (не менее 90%) встречались относительно редко – в 9 (21,4%) наблюдениях. Частота встречаемости камней с преобладанием кальций-оксалата составила 54,8% (23 случая), фосфатов – 23,8% (10), мочевой кислоты – 21,4% (9), что соответствует современным эпидемиологическим данным (рис. 2).
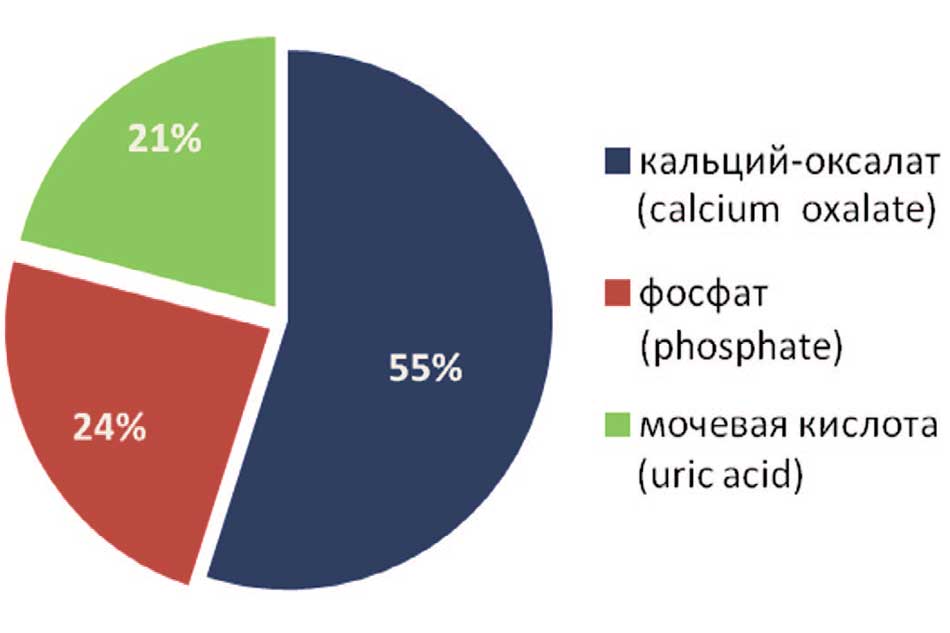
Рис. 2. Распределение пациентов в соответствии с преобладающим компонентом в составе конкремента
Fig. 2. Distribution of the patients according to the predominant component in the concretion
Выбор тактики лечения
При определении объема операции мы руководствовались актуальными клиническими рекомендациями: РИРХ, 58 (27,9%) случаев, выполняли по поводу конкрементов почек размерами до 15 мм в наибольшем измерении, ПНЛТ (n=36; 17,3%) – при конкрементах почек размерами более 15 мм, контактные уретеролитотрипсии (КУЛТ) (n=119; 57,2%) – при конкрементах мочеточников любых размеров. Исключение составили 2 (0,9%) случая полиморбидных пациентов с конкрементами, превышавшими 15 мм в наибольшем измерении, которым выполнили РИРХ как менее травматичную операцию, отличающуюся меньшим риском клинически значимого кровотечения.
В 3 (1,4%) случаях, в связи с низкой плотностью камня, выполнена дистанционная ударно-волновая литотрипсия (ДУВЛТ), в 2 (0,9%) случаях в силу расположения и размеров конкремента оказалась технически возможной литоэкстракция, у 2 (0,9%) пациентов отмечено самостоятельное отхождение конкремента на фоне литолитической терапии. В 2 (0,9%) наблюдениях, учитывая множественное поражение с локализацией конкрементов как в почке, так и в мочеточнике, последовательно выполнены КУЛТ и РИРХ (табл. 3).
Всем пациентам после ПНЛТ были установлены нефростомические дренажи. Решение о необходимости установки мочеточникового стента после КЛТ принималось интраоперационно, в зависимости от размера конкрементов, наличия резидуальных конкрементов, состояния слизистой оболочки мочеточника в зоне локализации конкремента и наличия предстентирования.
Выбор хирургической тактики
Все литотрипсии были выполнены с использованием отечественной тулиевой лазерной установки FiberLase U2. Средняя продолжительность ПНЛТ составила 124,1±30,5 мин, КУЛТ – 37,6±15 мин, РИРХ – 61,8±28,0 мин. Кровопотеря при всех операциях была клинически незначима.
Выбор хирургической тактики определялся индивидуально с учетом локализации, размеров и плотности конкремента, а также состояния мочевыводящих путей и степени компенсации сопутствующей патологии пациента.
Таблица 3. Виды оперативных вмешательств
Table 3. Types of surgeries
| Вид оперативного вмешательства Type of surgery |
n (%) |
|---|---|
| Контактная уретеролитотрипсия (КУЛТ) Ureteroscopy with lihtotripsy (USL) |
119 (57,2%) |
| Ретроградное интраренальное хирургическое вмешательство (РИРХ) Retrograde intrarenal surgery (RIRS) |
58 (27,9%) |
| Перкутанная нефролитотрипсия (ПНЛТ) Percutaneous nephrolithotripsy (PCNL) |
36 (17,3%) |
| Дистанционная ударно-волновая литотрипсия (ДУВЛТ) External shock wave lithotripsy (ESWL) |
3 (1,4%) |
| Литоэкстракция Lithoextraction |
2 (0,9%) |
| Последовательно выполнены КУЛТ и РИРХ USL with consequent RIRS |
2 (0,9%) |
| Литолитическая терапия Litholysis |
2 (0,9%) |
Далее нами представлено три клинических наблюдения, которые демонстрируют персонализированный подход к лечению пациентов с МКБ.
Клиническое наблюдение №1
Пациентка С. 70 лет обратилась с жалобами на периодическую боль в поясничной области справа. При обследовании обнаружен коралловидный камень правой почки (К3) размерами 41х15 мм, плотностью 410693 HU (рис. 3), pH мочи – 5. Кроме того у пациентки диагностирован флотирующий тромб глубокой вены голени, что потребовало немедленного назначения гепаринотерапии. В связи с этим выполнение планового оперативного вмешательства по поводу коралловидного камня было противопоказано. Учитывая характеристики конкремента, принято решение о назначении пациентке литолитической терапии. При контрольном обследовании через 2 месяца отмечено уменьшение размеров конкремента до 14 мм (рис. 4).

Рис. 3. Пациентка С. КТ почек от 21.06.2022: до начала лечения
Fig. 3. Patient C. CT scan of the kidneys, 21.06.2022: before the start of treatment
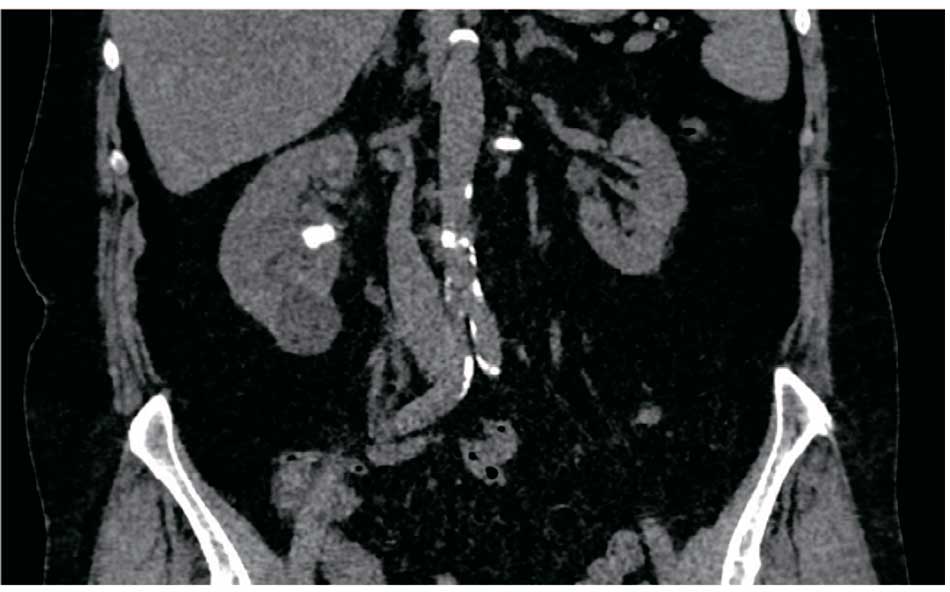
Рис. 4. Пациентка С. КТ почек от 28.08.2022: состояние после 2 месяцев применения цитратных смесей
Fig. 4. Patient C. CT scan of the kidneys, 28.08.2022: the condition after 2 months of using citrate mixtures
Учитывая результаты литолитической терапии, данные лабораторно-инструментальных исследований, а также высокий риск кровотечения, обусловленный приемом антиагрегантов, пациентке было выполнено менее травматичное хирургическое вмешательство – РИРХ справа с последующим дренированием верхних мочевых путей (ВМП) внутренним мочеточниковым стентом. Конкремент был полностью разрушен, а его фрагменты удалены из мочевыводящих путей (рис. 5).

Рис. 5. Пациентка C. КТ почек от 08.11.2022: состояние после РИРХ справа с дренированием верхних мочевых путей катетером-стентом
Fig. 5. Patient C. CT scan of the kidneys, 08.11.2022: post-RIRS condition on the right with drainage of the upper urinary tract with a ureteral stent
Клиническое наблюдение № 2
Пациентка И. 68 лет. Диагноз: Коралловидные камни обеих почек. Госпитализирована с жалобами на периодическое повышение температуры тела до фебрильных цифр. По данным КТ от 04.08.2021 г.: в чашечках и лоханке правой почки коралловидный камень (К2) размером 31х34 мм, плотностью 380 HU. В чашечках и лоханке правой почки коралловидный камень (К3) размером 32х28 мм, плотностью 450 HU. Двусторонняя пиелокаликоэктазия (рис. 6).
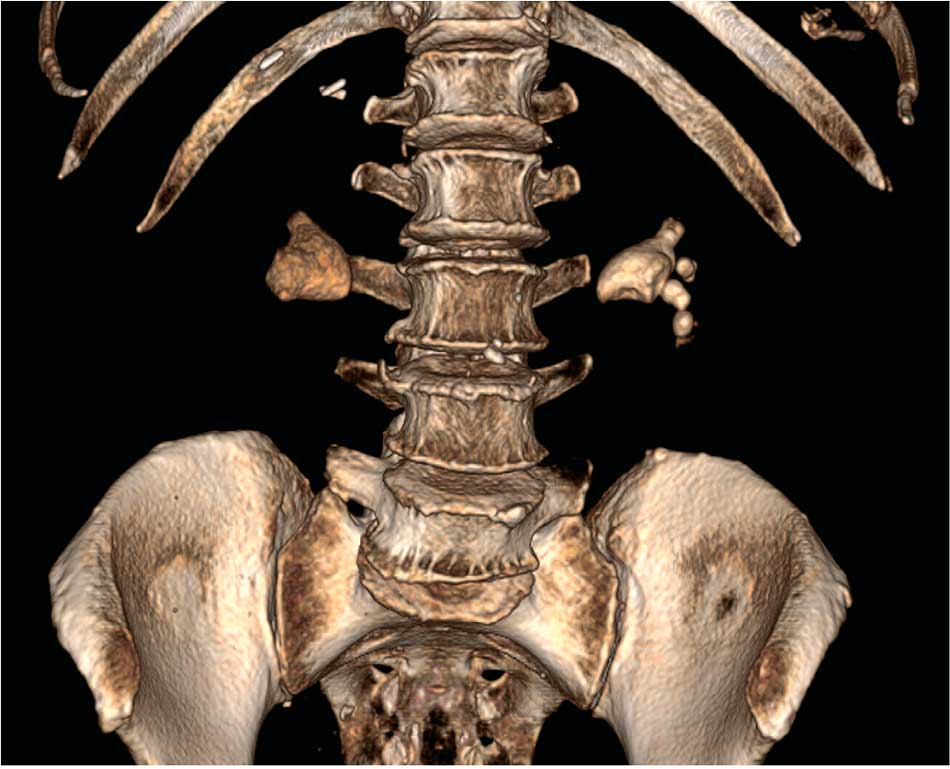
Рис. 6. Пациентка И. КТ почек от 04.08.2021,3D-модель, фронтальная проекция: до операции
Fig. 6. Patient I. CT scan of the kidneys, 08.04.2021,3D-model, frontal projection: before surgery
Учитывая наличие лихорадки и двусторонней пиелоэктазии, первым этапом лечения пациентке выполнена двусторонняя нефростомия. Через 2 недели антибактериальной терапии, назначенной с учетом результатов посева мочи, полученной при пункции чашечно-лоханочной системы почек при установке нефростом, выполнены ПНЛТ справа и стентирование левого мочеточника. В послеоперационном периоде нефростомические дренажи с обеих сторон были удалены (рис. 7).

Рис. 7. Пациентка И. КТ почек: состояние после ПНЛТ справа и стентирования левого мочеточника
Fig. 7. Patient I. CT scan of the kidneys: the condition after PСNL on the right and stenting of the left ureter
Через 3 недели пациентке была выполнена ПНЛТ слева с последующей РИРХ для удаления труднодоступных конкрементов чашечек левой почки, в результате чего все конкременты были удалены (рис. 8).

Рис. 8. Пациентка И. КТ почек. Снимок после оперативного вмешательства с противоположной стороны
Fig. 8. Patient I. Kidney CT frontal image. A picture after surgery from the opposite side
Клиническое наблюдение № 3
Пациент Н. 49 лет. В 2014 году перенес инфаркт миокарда, в том же году диагностирован бессимптомный конкремент левой почки до 15 мм диаметром. В январе 2021 года появились внезапные тянущие боли в левой поясничной области. При контрольном КТ в феврале 2021 года был обнаружен коралловидный камень левой почки (К2) размерами до 30 мм в наибольшем измерении, плотностью 1570 HU (рис. 9).

Рис. 9. Пациент Н. КТ почек: состояние до лечения
Fig. 9. Patient N. Kidney CT scan: condition before treatment
При подготовке к оперативному вмешательству по поводу коралловидного камня у пациента диагностирована кардиомиопатия, в связи с чем во многих центрах в проведении операции по поводу МКБ пациенту было отказано.
В январе 2022 года госпитализирован в НМИЦ хирургии. По данным коронарографии от 19.01.22, у пациента правый тип кровоснабжения миокарда, коронарные артерии без ангиографически значимых стенозов. Эхокардиография от 20.01.22: увеличены размеры левого желудочка. Толщина миокарда левого желудочка в норме. Верхушка сердца закруглена, расширена, несколько дискинетична. Акинезия переднего и переднеперегородочного сегментов левого желудочка во всех отделах. Ударный объем 67 мл, снижение фракции выброса практически вдвое – до 35 %, минутный объем сердца 3,6 л/ мин. Митральная регургитация 1 степени (гемодинамически незначимая), трикуспидальная регургитация 1-1,5 степени (гемодинамически незначимая). Сбросов крови нет. Сократительная функция левого желудочка резко снижена. Признаки атеросклероза восходящего отдела аорты. В полости перикарда жидкости не выявлено. Результаты Тредмил-теста от 21.01.2022 г.: максимальная частота сердечных сокращений 146/ мин достигнута, ST-T на изолинии, нарушения ритма сердца не регистрировались. Тест отрицательный, высокая степень толерантности к физической нагрузке.

Рис. 10. Пациент Н. КТ почек от 31.03.2023. Снимок после оперативного вмешательства
Fig. 10. Patient N. Kidney CT, 03.31.2023. A snapshot after surgery
В результате проведенного обследования установлен следующий диагноз: Мочекаменная болезнь. Коралловидный камень левой почки. Хронический пиелонефрит вне обострения. Ишемическая болезнь сердца. Постинфарктный (2014 год) кардиосклероз. Стресс-индуцированная кардиомиопатия неуточненная. Хроническая сердечная недостаточность (ХСН) I ст., II функциональный класс по NYHA. Гипертоническая болезнь 3 стадии, II степени, риск сердечно-сосудистых осложнений 4. Клиническая ситуация обсуждена на консилиуме врачей с участием анестезиолога, кардиолога и уролога. Абсолютных противопоказаний к операции не было выявлено. Принято решение о выполнении наименее травматичного оперативного вмешательства по поводу коралловидного камня, и 21.01.2022 пациенту выполнена РИРХ слева с последующим дренированием ВМП слева внутренним мочеточниковым стентом. Послеоперационный период протекал без осложнений.
Спустя 2 месяца после операции, 31.03.2023, перед удалением внутреннего мочеточникового стента пациенту выполнена контрольная КТ, при которой выявлен единичный резидуальный конкремент в средней трети левого мочеточника (рис. 10), в связи с чем 03.04.2023 выполнена КУЛТ.
ОБСУЖДЕНИЕ
В основу настоящей статьи положен анализ опыта лечения пациентов с МКБ в двух учреждениях – городской клинической больнице, оказывающей экстренную медицинскую помощь, и федеральном научноисследовательском центре, специализирующемся на плановом хирургическом лечении, что позволяет оценить различные клинические подходы к ведению этой категории пациентов.
Причины образования камней в мочевыводящих путях разнообразны. В настоящее время ряд специалистов склоняются к мнению, что не существует единой причины возникновения МКБ, а есть ряд факторов и состояний, которые способствуют формированию конкрементов. По результатам менделевской рандомизации на двух выборках, проведенной M. Liu с соавт. в 2023, из 44 факторов риска подтверждено статистически значимое влияние на развитие МКБ раннего начала курения, малоподвижного образа жизни, высокого содержания натрия в моче, соотношения натрия и калия в моче, соотношения натрия и креатинина в моче, содержания кальция в сыворотке, 25-гидрокси-витамина D, скорости клубочковой фильтрации (СКФ), индекса массы тела, окружности талии, уровня инсулина натощак, гликированного гемоглобина, сахарного диабета 2 типа и гипертонической болезни [11].
Как можно предположить из вышеуказанного, МКБ патогенетически ассоциирована с метаболическим синдромом и высокой коморбидностью. В частности, неоднократно высказывались предположения о взаимосвязи МКБ и высокого риска сердечно-сосудистых осложнений [12-16].
В ретроспективном обсервационном когортном исследовании C.J. Liu с соавт. в 2022 оценена взаимосвязь МКБ и атеросклеротического стеноза сонных артерий. Воспаление и оксидативный стресс способствуют образованию кристаллов и их адгезии к клеткам почечных канальцев, что приводит к росту камней в почках. Эти же патологические процессы также достоверно способствуют прогрессированию атеросклеротических заболеваний коронарных и сонных артерий. Учитывая, что воспаление играет ключевую роль как в возникновении камней в почках, так и в стенозе сонных артерий, многие показатели воспаления, включая соотношение нейтрофилов и лимфоцитов и соотношение моноцитов и лимфоцитов, могут быть использованы в качестве биомаркеров этих процессов. Индекс системного воспалительного ответа, который объединяет различные воспалительные клетки (нейтрофилы, моноциты и лимфоциты), предложен авторами в качестве более точного воспалительного биомаркера, позволяющего прогнозировать течение атеросклеротической болезни и МКБ [17].
В мета-анализе J. Saenz-Medina с соавт. в 2022 отмечено, что у пациентов с нефролитиазом чаще наблюдаются сердечно-сосудистые заболевания с относительным риском, оцениваемым от 1,20 до 1,24, а также более высокие показатели риска сосудистых заболеваний в целом, острого инфаркта миокарда и ишемического инсульта, в частности. Анализ подгрупп не дал достоверных результатов относительно влияния пола и возраста. Авторы предположили, что в основе этой взаимосвязи лежит, преимущественно, эндотелиальная дисфункция. Анализ состава мочи пациентов с МКБ также выявил более высокую экспрессию белков, связанных с сердечно-сосудистыми заболеваниями. Экспериментальные модели гипероксалурии выявили повышение маркеров эндотелиальной дисфункции в сыворотке крови [18]. По этой причине у пациентов с МКБ могут встречаться сопутствующие заболевания, которые повышают операционно-анестезиологический риск. Такие пациенты требуют персонализированного и мультидисциплинарного подхода.
В настоящее время не существует единого алгоритма выбора лечебной тактики у коморбидных пациентов. В связи с необходимостью учета большого количества факторов при выборе хирургических подходов к лечению коморбидных пациентов с МКБ и сопутствующими заболеваниями, разработка такового остается сложной задачей. Использование искусственного интеллекта для решения данной задачи представляется нам одним из наиболее перспективных путей улучшения результатов лечения пациентов с МКБ за счет персонализированного подхода к выбору хирургической тактики [19-25].
ЗАКЛЮЧЕНИЕ
Выбор лечебной тактики у больных МКБ с отягощенным коморбидным фоном, который ограничивает возможности хирургического лечения уролитиаза, остается непростой задачей. Для ее решения требуется мультидисциплинарный подход, а также последовательное или одновременное использование различных хирургических методик для удаления конкрементов из мочевыводящих путей.
Нами продемонстрировано три клинических наблюдения успешного лечения уролитиаза у пациентов с отягощенным коморбидным фоном. В каждом случае лечебная тактика определялась индивидуально, в связи с тем, что в настоящее время отсутствует алгоритм выбора методики лечения таких пациентов из-за необходимости учета большого количества факторов.
ЛИТЕРАТУРА
- Kachkoul R, Touimi GB, El Mouhri G, El Habbani R, Mohim M, Lahrichi A. Urolithiasis: history, epidemiology, aetiologic factors and management. Malays J Pathol 2023;45(3):333-52.
- Аполихин О.И., Сивков А.В., Солнцева Т.В., Комарова В.А. Эпидемиология мочекаменной болезни в различных регионах Российской Федерации. Бюллетень медицинских интернет-конференций 2011;1(3):167-76. [Apolikhin O.I., Sivkov A.V., Solntseva T.V., Komarova V.A. Epidemiology of urolithiasis in various regions of the Russian Federation. Biulleten meditsinskikh internet-konferentsii = Bulletin of Medical Internet Conferences 2011;1(3):167-76. (In Russian)].
- Протощак В.В., Паронников М.В., Орлов Д.Н., Киселев А.О. Медико-экономическое обоснование применения современных методов лечения мочекаменной болезни. Экспериментальная и клиническая урология 2019;(3):12-8. [Protoshchak V.V., Barannikov M.V., Orlov D.N., Kiselev A.O. Medical and economic justification of the use of modern methods of treatment of urolithiasis. Eksperimentalnaia i klinicheskaia urologiia = Experimental and Clinical Urology 2019;(3):12-18. (In Russian)]. https://doi.org/10.29188/2222-8543-2019-11-3-12-18.
- Desai M, Sun Y, Buchholz N, Fuller A, Matsuda T, Matlaga B, et al. Treatment selection for urolithiasis: percutaneous nephrolithomy, ureteroscopy, shock wave lithotripsy, and active monitoring. World J Urol 2017;35(9):1395-9. https://doi.org/10.1007/s00345-017-2030-8.
- Галкина Н.Г., Калинина Е.А., Галкин А.В. Мочекаменная болезнь: современные представления об этиологии (обзор). Саратовский научно-медицинский журнал 2020;16(3):773-9. [Galkina N.G., Kalinina E.A., Galkin A.V. Urolithiasis: modern concepts of etiology (review). Saratovskii nauchno-meditsinskii zhurnal = Saratov Journal of Medical Science 2020;16(3):773-9. (In Russian)]
- Wagner CA. Etiopathogenic factors of urolithiasis. Arch Esp Urol 2021;74(1):16-23.
- Mohammadi A, Shabestari AN, Baghdadabad LZ, Khatami F, Reis LO, Pishkuhi MA, et al. Genetic polymorphisms and kidney stones around the globe: a systematic review and meta-analysis. Front Genet 2022;13:913908. https://doi.org/10.3389/fgene.2022.913908.
- Carbone A, Al Salhi Y, Tasca A, Palleschi G, Fuschi A, De Nunzio C, et al. Obesity and kidney stone disease: a systematic review. Minerva Urol Nefrol 2018;70(4):393-400. https://doi.org/10.23736/S0393-2249.18.03113-2.
- Bauza JL, Pieras EC, Grases F, Tubau V, Guimerà J, Sabaté XA, et al. Urinary tract infection's etiopathogenic role in nephrolithiasis formation. Med Hypotheses 2018;118:34-35. https://doi.org/10.1016/j.mehy.2018.06.002.
- Cicerello E, Ciaccia M, Cova GD, Mangano MS. The new patterns of nephrolithiasis: what has been changing in the last millennium? Arch Ital Urol Androl 2021;93(2):195-9. https://doi.org/10.4081/aiua.2021.2.195.
- Liu M, Wu J, Gao M, Li Y, Xia W, Zhang Y, et al. Lifestyle factors, serum parameters, metabolic comorbidities, and the risk of kidney stones: a Mendelian randomization study. Front Endocrinol 2023;14:1240171. https://doi.org/10.3389/fendo.2023.1240171.
- Kim SY, Bang WJ, Min C, Choi HG. Association of nephrolithiasis with the risk of cardiovascular diseases: a longitudinal follow-up study using a national health screening cohort. BMJ Open 2020;10(11):e040034. https://doi.org/10.1136/bmjopen-2020-040034.
- Arafa A, Eshak ES, Iso H, Shirai K, Muraki I, Sawada N, et al. Urinary stones and risk of coronary heart disease and stroke: the Japan Public Health Center-Based Prospective Study. J Atheroscler Thromb 2020;27(11):1208-15. https://doi.org/10.5551/jat.54775.
- Yuan M, Zhou HY, Hu F, Liu SY, Rao W, Wu LF, et al. Association between kidney stones and risk of developing stroke: a meta-analysis. Neurol Sci 2021;42(11):4521-9. https://doi.org/10.1007/s10072-021-05113-5.
- Huang L, Hu J, Xue C, Ding J, Guo Z, Yu B. Vascular calcification on the risk of kidney stone: a meta-analysis. Ren Fail 2023;45(1):2183727. https://doi.org/10.1080/0886022X.2023.2183727.
- Bnaya A, Kafha IZ, Barhoum H, Shavit L. Vascular calcification in kidney stone formers: the impact of age and stone composition. Urolithiasis 2024;52(1):97. https://doi.org/10.1007/s00240-024-01597-w.
- Liu CJ, Jan HC, Huang HS. Risks of carotid artery stenosis and atherosclerotic cardiovascular disease in patients with calcium kidney stone: assessment of systemic inflammatory biomarkers. J Pers Med 2022;12(10):1697. https://doi.org/10.3390/jpm12101697.
- Saenz-Medina J, Muñoz M, Rodriguez C, Sanchez A, Contreras C, Carballido-Rodríguez J, Prieto D. Endothelial Dysfunction: An Intermediate Clinical Feature between Urolithiasis and Cardiovascular Diseases. Int J Mol Sci 2022;23(2):912. https://doi.org/10.3390/ijms23020912.
- Пранович А.А., Исмаилов А.К., Карельская Н.А., Костин А.А., Кармазановский Г.Г., Грицкевич А.А. Искусственный интеллект в диагностике и лечении мочекаменной болезни. Российский журнал телемедицины и электронного здравоохранения 2022;8(1):42-57. [Pranovich A.A., Ismailov A.K., Karelskaya N.A., Kostin A.A., Karmazanovsky G.G., Gritskevich A.A. Artificial intelligence in the diagnosis and treatment of urolithiasis. Rossiiskii zhurnal telemeditsiny i elektronnogo zdravookhraneniia = Russian Journal of Telemedicine and E-Health 2022;8(1):42-57. (In Russian)]. https://doi.org/10.29188/2712-9217-2022-8-1-42-57.
- Cil G, Dogan K. The efficacy of artificial intelligence in urology: a detailed analysis of kidney stone-related queries. World J Urol 2024;42(1):158. https://doi.org/10.1007/s00345-024-04847-z.
- Musheyev D, Pan A, Kabarriti AE, Loeb S, Borin JF. Quality of information about kidney stones from artificial intelligence chatbots. J Endourol 2024;38(10):1056-61. https://doi.org/10.1089/end.2023.0484.
- Panthier F, Melchionna A, Crawford-Smith H, Phillipou Y, Choong S, Arumuham V, et al. Can artificial intelligence accurately detect urinary stones? A systematic review. J Endourol 2024;38(8):725-40. https://doi.org/10.1089/end.2023.0717.
- Yang B, Veneziano D, Somani BK. Artificial intelligence in the diagnosis, treatment and prevention of urinary stones. Curr Opin Urol 2020;30(6):782-7. https://doi.org/10.1097/MOU.0000000000000820.
- Nedbal C, Bres-Niewada E, Dybowski B, Somani BK. The impact of artificial intelligence in revolutionizing all aspects of urological care: a glimpse in the future. Cent European J Urol 2024;77(1):12-4. https://doi.org/10.5173/ceju.2023.255.
- Hashemi Gheinani A, Kim J, You S, Adam RM. Bioinformatics in urology – molecular characterization of pathophysiology and response to treatment. Nat Rev Urol 2024;21(4):214-42. https://doi.org/10.1038/s41585-023-00805-3.







