Одной из основных задач в лечении детей с врожденными обструктивными заболеваниями мочеточника, диагностированными пренатально, является восстановление уродинамики верхних мочевыводящих путей (ВМП). Применение у детей с тяжелыми формами ретенционных изменений чашечно-лоханочной системы почки хирургических и эндоскопических методов лечения, направленных на увеличение диаметра функциональных сегментов мочеточника, оказывают положительное влияние на восстановление уродинамики ВМП. Однако по данным ряда авторов при рентгеноурологическом обследовании детей с пренатально диагностированными врожденными обструктивным заболеваниями мочеточника в 81% случаев ретенционные изменения чашечно-лоханочной системы почки соответствуют 1-ой или 2-ой степени тяжести, что является показанием к консервативной терапии [1, 2]. До настоящего времени консервативное лечение этих состояний было симптоматическое и основное внимание уделялось динамике размеров чашечно-лоханочной системы без возможностей медикаментозно воздействовать на патоуродинамические и дисметаболические процессы [3, 4].
МАТЕРИАЛЫ И МЕТОДЫ
В группу исследования вошли 48 пациентов старше 6 лет поступивших в Центр «Оперативной андрологии и эндоскопической урологии» Детской городской клинической больницы № 9 им. Г.Н. Сперанского с направляющим диагнозом гидронефроз и обструктивный мегауретер.
Для оценки функционального состояния почки, тяжести ретенционных изменений чашечно-лоханочной системы и состояния уродинамики верхних мочевыводящих путей всем детям были проведены следующие исследования:
1. Стандартные методы исследования:
- лабораторные исследования крови и мочи;
- ультразвуковое исследование почек;
- внутривенная урография на 6, 12, 18 и 30 минуте после микции;
- микционная цистография.
2. Специальные методы исследования:
- диуретическая ультразвуковая пиелография с компьютерной интерпретацией результатов обследования;
- качественно-количественная оценка протеинового профиля мочи методом автоматизированного электрофореза в полиакриламидном геле.
На основании рентгеноурологического обследования нарушений функции почек не было диагностировано ни у одного больного, а ретенционные изменения чашечнолоханочной системы соответствовали 1-ой или 2-ой степени.
Для оценки состояния уродинамики ВМП всем детям проведена диуретическая ультразвуковая пиелография по разработанной в клинике методике: после самостоятельного мочеиспускания определяли исходные размеры лоханки, затем внутримышечно вводили лазикс в дозе 0,5 мг/кг и проводили мониторинг поперечных размеров лоханки на каждой 5-й минуте исследования в течение 60 минут. Оценка результатов диуретической ультразвуковой пиелографии была проведена по авторской методике [5]. Установленные закономерности изменения объемных показателей, характеризующих фазы наполнения и опорожнения лоханки, определяли отсутствие зависимости состояния уродинамики ВМП от исходного объема (размера) лоханки [6]. Основными критериями оценки состояния уродинамики ВМП были разработанные уродинамические коэффициенты, характеризующие резервуарную функцию лоханки (КL), проходимость пиелоуретерального сегмента (КPUS) и эффективность опорожнения лоханки на высоте повышенного потока мочи (Ко), позволяющие установить вариант и определить тяжесть нарушения уродинамики ВМП.
Коэффициент опорожнения лоханки на высоте повышенного потока мочи (Ко), характеризующий уродинамику на уровне лоханки и мочеточника, рассчитывался по формуле: Ко = (Vnmax-Vо10) / (Vnmax – Vi), где Vnmax – максимальный объем наполнения лоханки, Vо10 – объем лоханки на 10 минуте ее опорожнения и Vi – исходный объем лоханки.
Коэффициент адаптации лоханки к повышенному потоку мочи (КL), отражающий резервуарную функцию лоханки, рассчитывался по формуле: КL = (Vi х 1,63) / (Vn10 – Vi), где Vi – исходный объем лоханки, 1,63 – коэффициент прогнозируемого объема наполнения лоханки на 10-й минуте исследования в зависимости от ее исходного объема и Vn10 – объем наполнения лоханки на 10-й минуте исследования.
Коэффициент адаптации пиелоуретерального сегмента (ПУС) к возросшему объему наполнения лоханки (КPUS), отражающий транзиторную функцию мочеточника, рассчитывался по формуле: КPUS=(Viх1,63) /(Vn10 – Vi), где Vi – исходный объем лоханки, 1,63 – коэффициент прогнозируемого объема опорожнения лоханки на 10 минуте ее опорожнения и Vо10 – объем лоханки на 10 минуте ее опорожнения.
Электрофорез белков мочи относится к информативным лабораторным методам диагностики ранних стадий нарушений функционального состояния почечной паренхимы [7, 8]. Имеются публикации, в которых электрофорез белков мочи рассматривается как прогностический тест изменений ренальной функции у детей с пузырно-мочеточниковым рефлюксом и гидронефрозом [9-13].
Для определения скрытых нарушений функционального состояния нефронов, у детей с нарушениями уродинамики верхних мочевых путей, которые невозможно верифицировать другими методами диагностики, всем пациентам выполнена качественно-количественная оценка протеинового профиля мочи методом автоматизированного электрофореза в полиакриламидном геле. Тип протеинурии определял индекс белковых фракций (ИБФ), который рассчитывался, как отношение суммы значений среднеи высокомолекулярных протеинов к значениям низкомолекулярных преальбуминов. Значения показателей ИБФ< 0,5 определяли канальцевый тип протеинурии, >1,5 клубочковой, а интервал значения 0,5-1,5 указывали на смешанный тип. По преобладанию в уропротеинограмме преальбуминовых или постальбуминовых белковых фракций (Σlpf – leading protein fractions), оценивали степень дисфункции нефронов минимальную (Σlpf < 10 мг/л), умеренную (Σlpf 10–20 мг/л) и выраженную (Σlpf > 20 мг/л). Кроме этого были определены патологический (П-белок) и общий белок (О-белок) мочи.
Статистический анализ результатов проведен с использованием пакета программ Microso Excel 2003 и Statistica 6,0. Значения показателей, имеющих нормальное распределение, представлены как М ± σ (М – среднее, σ – стандартное отклонение), при ненормальном распределении – Me ± IQR (Me – медиана, IQR – межквартильный размах). Сравнение количественных показателей в разных группах осуществляли при помощи Т-критерия Вилкоксона, при нормальном распределении Т-критерий Стьюдента. ДИ-95%÷ДИ+95%, где ДИ – доверительный интервал. Различия показателей считалось достоверным при p< 0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В группе обследованных детей у 5 пациентов (10,4%) значения коэффициента эффективности опорожнения лоханки (Ко) были равны или были больше 1, что свидетельствовало об отсутствии нарушений уродинамики ВМП. У остальных детей значения уродинамических коэффициентов характеризовали различные варианты нарушений уродинамики ВМП. Средние значения уродинамических коэффициентов были не информативны, поэтому оценка степени тяжести нарушений уродинамики ВМП была проведена по градации значений уродинамических коэффициентов: НОРМА=≥0,96; 1 СТЕПЕНЬ=0,95-0,75; 2 СТЕПЕНЬ=0,740,50; 3 СТЕПЕНЬ= 0,49-0,25 и 4 СТЕПЕНЬ=0,24-0,04. На основании этого в большинстве случаев установлены 3-ая (39,5%) и 4-ая (37,2%) степени тяжести нарушения уродинамики ВМП. Все пациенты были распределены по вариантам нарушения уродинамики.
В большинстве случаев (52,1%) имелся дезадаптационный вариант, который характеризовался снижением коэффициента эффективности опорожнения лоханки (Ко) при нормативных показателях коэффициентов адаптации лоханки (КL) и пиело-уретерального сегмента (КPUS).
Обструктивный вариант, установленный в 29,2%, случаев был обусловлен низкими значениями коэффициента адаптации ПУС (КPUS) при нормативных значениях коэффициента адаптации лоханки (КL).
Снижение коэффициентов адаптации лоханки (КL) и пиело-уретерального сегмента (КPUS), отмеченные у остальных 8,3% детей, определяли обструктивно-гипертензионный вариант нарушений уродинамики обусловленный обструкцией мочеточника в сочетании с внутрилоханочной гипертензией.
Средние значения коэффициента эффективности опорожнения лоханки (КO)=0,18±0,11(0,12÷0,24) определяли у детей с обструктивным вариантом 4-ую степень тяжести нарушения уродинамики ВМП. У пациентов с обструктивно-гипертензионном вариантом тяжесть нарушений уродинамики ВМП соответствовала 3-ей степени при значениях (КO)=0,36±0,20(0,16÷0,56).
В превалирующем дезадаптационном варианте значения коэффициента (КO)=0,56±0,33 (0,43÷0,68) характеризовали 2-ую степень нарушения уродинамики ВМП.
Внутрилоханочная гипертензия 3-ей степени отмечалась у детей с обструктивно-гипертензионным вариантом, при значениях коэффициента адаптации лоханки (КL)= 0,44±0,33(0,12÷0,77). У детей с другими вариантами значения данного коэффициента были (КL)≥1,0, что характеризовало адекватную реакцию лоханки на повышенный поток мочи.
Нарушения проходимости ПУС 3-ей степени диагностировано у детей с обструктивным вариантом (КPUS)=0,37±0,20(0,26÷0,47) и 2-ой степени у пациентов с обструктивногипертензионным вариантом, где значения коэффициента адаптации ПУС были выше (КPUS)=0,61±0,42 (0,19÷1,02). Предположительно нарушения проходимости ПУС могли быть обусловлены снижением его эластичности.
Анализ состояния протеинового профиля мочи в группе детей с обструктивным вариантом нарушения уродинамики ВМП показал преобладание смешенного типа протеинурии (71,4%), в остальных случаях диагностирован канальцевый и клубочковый тип протеинурии при средних значениях ИБФ-0,86± 0,49(0,08÷1,52). Выраженность протеинурии у 57,1% детей с обструктивным вариантом была умеренной. Минимальная протеинурия отмечалась у 28,6% детей и выраженная в 14,3% случаях при средних показателях ЛПФ-11,20±7,41(2,54÷30,34), П-белка-15,86;5,95 (10,60÷16,55) и О-белка-52,29±19,82 (24,0÷92,0).
У детей с обструктивно-гипертензионным вариантом нарушения уродинамики ВМП в равной степени определялся смешенный и канальцевый тип протеинурии (50%/50%) при средних значениях показателей ИБФ 0,61±0,46(0,08÷1,09). В большинстве случаев отмечались минимальные степени протеинурии, а в остальных умеренная и выраженная степени протеинурии при значениях показателей: ЛПФ-11,08± 8,44 (3,67÷20,83), П-белка-16,27± 11,64 (6,08÷29,54) и О-белка -47,25± 30,47(27,0÷92,0).
При анализе протеинового профиля мочи у 20 детей с дезадаптационным вариантом нарушения уродинамики ВМП установлена минимальная степень протеинурии при средних показателях: ЛПФ-8,61;7,46 (5,76÷13,22), П-белка 13,66;5,76 (10,13÷15,89) и О-белка-46;15(40,0÷ 55,0). В данной группе детей с дезадаптационным вариантом преобладал смешенный тип протеинурии (70%) при средних значениях ИБФ0,72±0,40(0,13÷1,52).
Во второй группе с дезадаптационным вариантом нарушения уродинамики ВМП определялась умеренная и выраженная степени протеинурии (81,8% и 18,2% соответственно) при средних показателях: ЛПФ-15,19;6,99(10,05÷17,49), П-белка-29,16;14,37(15,83÷30,20) и О-белка-62,28±19,70(27,0÷88,0). Канальцевый и смешанный тип протеинурии в данной группе детей был распределен поровну при средних значениях ИБФ-0,52±0,30(0,13÷0,22).
Таким образом, нарушения уродинамики ВМП 4-ой степени в большинстве случаев было отмечено у детей с обструктивным вариантом в сочетании с протеинурией умеренной выраженности. В группе детей обструктивно-гипертензионным вариантом преобладала 3-ая степень нарушения уродинамики, а выраженность протеинурии была минимальная. При дезадаптационном варианте степени нарушения уродинамики колебались от 1 до 4ой степени тяжести с превалированием, так же как и в предыдущем варианте 3-ей степени и минимальной выраженности протеинурии. При всех вариантах нарушения уродинамики ВМП лидирующим был смешанный тип протеинурии.
На основании оценки результатов внутривенной урографии, диуретической ультразвуковой пиелографии и протеинового профиля белков мочи всем пациентам была показана консервативная терапия.
В последние годы в клинической практике широкое применение при лечении мочекаменной болезни получил фитопрепарат Роватинекс содержащий 6 типов терпенов (Анетол, Борнеол, Камфен, Пинен, Фенхон, Цинеол). Кроме литокинетического и антилитогенного эффектов терпены обладают спазмолитическим (Борнеол, Камфен, Пинен, Фенхон), диуретическим (Анетол) и противовоспалительным действием (Анетол, Борнеол, Камфен, Пинен, Фенхон, Цинеол), а также усиливают почечный кровоток (Анетол, Борнеол, Камфен) [14-18].
Впервые у детей Роватинекс был применен, при «программируемом» стентировании детей с обструктивным мегауретером и гидронефрозом с целью предотвращения инкрустации мочеточникового стента, что позволило увеличить длительность дренирования ВМП до 6 и более месяцев [19].
На основании установленных механизмов действия терпенов и их безопасности для оценки возможности медикаментозно воздействовать на патоуродинамические и дисметаболические процессы фитопрепарат Роватинекс был назначен обследованным пациентам в дозировке от 1 до 2 капсул в день в зависимости от возраста в течение 1 месяца [20].
Контрольная диуретическая ультразвуковая пиелография проведена 43 пациентам через 1-2 месяца после приема Роватинекса.
Анализ значений уродинамических коэффициентов у детей с обструктивным вариантом после приема Роватинекса показал улучшение уродинамики ВМП в среднем на 23% при исходных показателях (КO)=0,18±0,11 по сравнению с контрольными (КO)=0,41±0,23. Тем самым степень тяжести нарушения уродинамики ВМП снизилась с 4-ой до 3-ей. Улучшение уродинамики ВМП была обусловлена повышением проходимости ПУС при его исходных значениях (KPUS)=0,37±0,20 и контрольных (KPUS)=1,05±0,96 (таб.1). Изменения уродинамических коэффициентов обусловили трансформацию обструктивного варианта в более благоприятный дезадаптационный вариант у 42,9% пациентов.
Таблица 1. Динамика средних значений уродинамических коэффициентов нарушений уродинамики ВМП до и после приема Роватинекса
| Варианты | Уродинамические коэффициенты | |||||
|---|---|---|---|---|---|---|
| КO | КL | KPUS | ||||
| До | После | До | После | До | После | |
| Обструктивный вариант (29,2%) |
0,18±0,11 (0,12÷0,24) |
0,41±0,23 (0,26÷0,56) |
2,06±0,94 (1,55÷2,57) |
2,29±1,85 (1,09÷3,50) |
0,37±0,20 (0,26÷0,47) |
1,05±0,96 (0,42÷1,67) |
| Обструктивногипертензионный вариант (8,3%) | 0,36±0,20 (0,16÷0,56) |
0,61±0,54 (0,13÷1,35) |
0,44±0,33 (0,12÷0,77) |
1,75±1,74 (0,66÷4,16) |
0,61±0,42 (0,19÷1,02) |
1,04±0,27 (0,67÷1,41) |
| Дезадаптационный вариант (52,1%) |
0,56±0,33 (0,43÷0,68) |
0,55±0,40 (0,36÷0,73) |
4,20±6,03 (1,92÷6,47) |
2,74±3,00 (1,36÷4,13) |
3,17±3,41 (1,89÷4,46) |
1,51±1,17 (0,97÷2,05 |
Примечание: КO-коэффициент эффективности опорожнения лоханки; КL-коэффициент адаптации лоханки; KPUS-коэффициент адаптации мочеточника; значения представлены как среднее (М) ± стандартное отклонения (m); доверительный интервал (ДИ-95%÷ДИ+95%); достоверность различий показателей между группами p<0,05.
При контрольной оценке протеинового профиля мочи после приема Роватинекса выраженность протеинурии у всех детей с обструктивным вариантом уменьшилась до минимальной. Средние показатели лидирующих протеиновых фракций (ЛПФ) до лечения составляли 11,20± 7,41(2,54÷30,34) и 5,91±1,69 (2,22÷8,33) после фитотерапии. Кроме этого было отмечено снижение других показателей состава белковых фракции: П-белок до 15,86;5,95 (10,60÷16,55), после 9,34±2,92 (3,18÷14,53) и О-белок до 52,29±19,82 (24,0÷92,0) после 39,64±12,77 (18,0÷56,0). Тип протеинурии не изменился при исходных показателях индекса белковых фракций ИБФ 0,86±0,49 (0,08÷1,52) и контрольных 1,08±0,73 (0,14÷2,31). Динамика средних показателей протеинового профиля белков мочи в зависимости от варианта нарушений уродинамики ВМП до и после приема Роватинекса представлена в таблице 2.
Таблица 2. Динамика средних значений показателей протеинового профиля в зависимости от варианты нарушений уродинамики ВМП до и после приема Роватинекса
| Варианты | Показатели | ||||
|---|---|---|---|---|---|
| Период | ИБФ | ЛПФ | П-белок | О-белок | |
| Обструктивный вариант (29,2%) | До | 0,86±0,49 (0,08÷1,52) |
11,20±7,41 (2,54÷30,34) |
15,86;5,95 (10,6÷16,55) |
52,29±19,82 (24,0÷92,0) |
| После | 1,08±0,73 (0,14÷2,31) |
5,91±1,69 (2,22÷8,33) |
9,34±2,92 (3,18÷14,53) |
39,64±12,77 (18,0÷56,0) |
|
| Обструктивногипертензионный вариант (8,3%) |
До | 0,61±0,46 (0,08÷1,09) |
11,08±8,44 (3,67÷20,83) |
16,27±11,64 (6,08÷29,54) |
47,25±30,47 (27,0÷92,0) |
| После | 0,37±0,23 (0,14÷0,60) |
12,6±11,18 (4,39÷25,33) |
17,36±20,31 (2,36÷40,48) |
46,94±28,12 (6,82÷116,0) |
|
| Дезадаптационный вариант (52,1%) | До | 0,72±0,40 (0,13÷1,52) |
8,61;7,46 (5,76÷13,22) |
13,66;5,76 (10,13÷15,9) |
46;15 (40,0÷55,0) |
| После | 0,53±0,71 (0,29÷1,0) |
8,05;7,0 (4,96÷11,96) |
11,05;9,76 (7,88÷17,65) |
41;27 (34,0÷67,0) |
|
Примечание: (ИБФ)-индекс белковых фракций; (ЛПФ)-лидирующие протеиновые фракций; (П-белок)-патобелок; (О-белок)-общий белок; Значения показателей представлены как среднее (М) ± стандартное отклонения (m); доверительный интервал (ДИ-95%÷ДИ+95%); достоверность различий показателей между группами p>0,05.
У детей с обструктивно-гипертензионном вариантом также отмечено улучшение уродинамики ВМП в среднем на 25% при исходных показателях (КO)=0,36±0,20 и контрольных (КO)=0,61±0,54. Степень тяжести нарушения уродинамики ВМП снизилась с 3-ей до 2-ой степени. Положительная динамика в этой группе детей кроме повышения коэффициента адаптации пиело-уретерального сегмента (KPUS средние значения до 0,61±0,42, после 1,04±0,27) была обусловлена снижением внутрилоханочной гипертензии при исходных значениях коэффициента адаптации лоханки (КL)=0,44±0,33 и контрольных (КL)=1,75±1,74. В 75% случаев изменения уродинамических коэффициентов обусловили трансформацию обструктивно-гипертензионного варианта в дезадаптационный вариант.
Выраженность протеинурии у детей с обструктивно-гипертензионным вариантом до приема Роватинекса колебалась от минимальной до выраженной. После фитотерапии отмечено преобладание минимальной и отсутствие выраженной протеинурии при контрольных значениях: ЛПФ до 11,08±8,44 (3,67÷20,83), после 12,6±11,18 (4,39÷25,33); П-белка до 16,27±11,64 (6,08÷29,54), после 17,36±20,31 (2,36÷40,48) и О-белка до 47,25±30,47 (27,0÷92,0), после 46,94± 28,12 (6,82÷116,0). Контрольные индексы белковых фракций составляли 0,37±0,23 (0,14÷0,60) и свидетельствовали об увеличении канальцевого типа протеинурии при исходных значениях ИБФ=0,61±0,46 (0,08÷1,09).
В группе детей с дезадаптационном вариантом коэффициенты эффективности опорожнения лоханки оставались на том же уровне при исходных значениях (КO)=0,56±0,33 и контрольных (КO)=0,55±0,40. Вместе с тем у 16,1% детей отмечено полное восстановление уродинамики ВМП. Трансформация дезадаптационного варианта в обструктивный и обструктивно-гипертензионный варианты отмечено у 9,7% пациентов.
Выраженность патологического профиля белков мочи при дезадаптационном варианте, который исходно сопровождался в 64,5% случаев минимальной степенью протеинурии, после приема Роватинекса оставалась на том же уровне (64,5%) при средних значениях: ЛПФ до 8,61;7,46 (5,76÷13,22), после 8,05;7,0 (4,96÷11,96); П-белка до 13,66;5,76 (10,13÷15,89), после 11,05;9,76 (7,88÷17,65) и О-белка мочи до 46;15 (40,0÷55,0), после 41;27 (34,0÷67,0). Процентное перераспределение установлено между умеренной и выраженной степенями тяжести за счет увеличения выраженной протеинурии (до 6,5%, после 16,1%). Кроме этого положительная динамика отмечена в изменении преобладающего до приема Роватинекса смешенного типа протеинурии на канальцевый при значениях ИБФ до лечения 0,72±0,40 (0,13÷1,52), после 0,53±0,71 (0,29÷1,0).
На основании результатов статистической обработки показателей уродинамических коэффициентов характеризующих состояние уродинамики ВМП до и после применения Роватинекса у детей с ретенционными изменениями чашечно-лоханочной системы 1-ой и 2 степени, установлено его положительное влияние на все уродинамические фазы наполнения и опорожнения лоханки за счет повышения проходимости пиело-уретерального сегмента и резервуарной функции лоханки.
При контрольной диуретической ультразвуковой пиелографии у 6 детей с дезадаптационном вариантом констатировано полное восстановление уродинамики ВМП. У остальных детей сравнительный анализ степеней нарушений уродинамики ВМП до и после применения Роватинекса показал увеличение процентного соотношения легких степеней (рис. 1). Кроме этого после приема Роватинекса отмечена трансформация тяжелых обструктивных вариантов в более благоприятный дезадаптационный вариант (рис. 2).
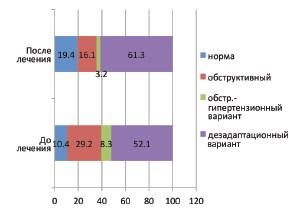
Рис. 1. Динамика процентных соотношений степеней тяжести нарушений уродинамики ВМП до и после приема Роватинекса
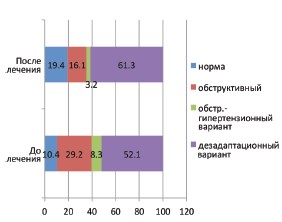
Рис. 2. Динамика процентных соотношений вариантов нарушений уродинамики ВМП до и после приема Роватинекса
Динамика протеинового профиля белков мочи не зависимо от варианта нарушения уродинамики ВМП после применения Роватинекса характеризовалась сменой смешанного типа протеинурии на более мягкий канальцевый тип у 42,1% детей (рис. 3). Такая же положительная динамика отмечена при сравнительном анализе выраженности протеинурии, которая в 78,9% была минимизирована (рис. 4).
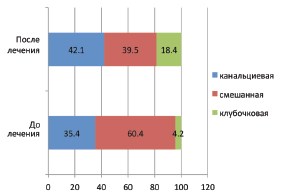
Рис. 3. Динамика процентных соотношений типов протеинурии до и после приема Роватинекса
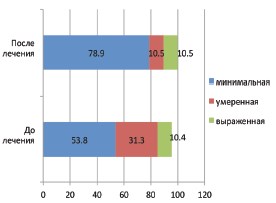
Рис. 4. Динамика процентных соотношений выраженности протеинурии до и после приема Роватинекса
ЗАКЛЮЧЕНИЕ
Установленные закономерности динамики показателей уродинамических коэффициентов и протеинового профиля белков мочи после фитотерапии у детей с ретенционными изменениями чашечно-лоханочной системы 1-ой и 2 степени являются основанием для утверждения необходимости пролонгировать длительность приема Роватинекса до 2-3 месяцев, в группе детей с дезадаптационным вариантом для повышения эффективности консервативной терапии, а у детей с тяжелыми обструктивными вариантами с целью более эффективной подготовки к последующим эндоскопическому или хирургическому вмешательствам.
ЛИТЕРАТУРА
1. Alberti C. Congenital ureteropelvic junction obstruction: physiopathology, de-coupling of tout court pelvic dilatation-obstruction semantic connection, bi-omarkers to predict renal damage evolution. // Eur Rev Med Pharmacol Sci. 2012. Vol. 16, N 2. Р. 213-219.
2. Hashim H, Woodhouse CR. Ureteropelvic Junction Obstruction. // Eur Urol Suppl. 2012. Vol. 11, N 2. P. 25-32. 3. Ахмедов Ю.М., Шарков С.М. , Мавлянов Ф.Ш. Врожден-ный гидронефроз у детей (обзор литературы). // Медицинский научный и учебно-методический журнал. 2005. N 29. С. 57-91.
4. Врублевский С.Г. Диагностика и тактика лечения детей с расширением чашечно-лоханочной системы. // Вопросы практической педиатрии. 2008. Т. 3, N 3. С. 35-39.
5. Бабанин И.Л., Казанская И.В., Ростовская В.В. Способ диагностики нарушений уродинамики расширенной лоханки у детей с гидронефрозом. // Патент на изобретение № 2423918. 2010.
6. Бабанин И.Л., Казанская И.В., Ростовская В.В. Ультразвуковые критерии оценки функционального состояния лоханки и проходимости пиело-уретерального сегмента у детей с гидронефрозом. //Детская хирургия. 2010. N 2. С. 15-20.
7. Воронцов А.Л., Нестеровская А.Ю., Потапова Л.А. Использование мето-да электрофореза белков нативной мочи в дифференциальной диагности-ке нефропатий. // Нефрология и диализ. 2005. T. 7, N 3. С. 12-16.
8. Габбасова Н.В. Белковый профиль мочи при нефропатиях у детей: Авто-реф. дисс. ... докт. мед. наук. М., 2009. 38 с.
9. Кириллов В.И., Богданова Н.А. Нарушения уродинамики как патогене-тический фактор хронических заболеваний почек у детей. // Российский вестник перинатологии и педиатрии. 2007. Т. 52, N 4. С. 42-49.
10. Beckers G, Mann H, Melzer H, Bemelmans B, Jakse G, Rohrmann D.. Urinary sodium dodecyl sulfate electrophoresis with silver staining: a noninvasive diagnostic tool for obstructive uropathy in children. // J Urol. 2008. Vol. 179, N 2. Р. 703-707.
11. Матюшина К.М., Ростовская В.В., Казанская И.В., Бабанин И.Л., Ворон-цов А.Л. Значение белкового состава мочи в функциональной оценке по-чек у детей первых лет жизни с гидронефрозом. // Детская хирургия. 2011. N 6. С. 29-36.
12. Матюшина К.М., Бабанин И.Л., Ростовская В.В., Расулов Н.С. Влияние индивидуальных особенностей уродинамики верхних мочевых путей на формирование различий в функционировании нефронов при гидронефро-зе у детей. // Материалы X Российского конгресса «Современные техно-логии в педиатрии и детской хирургии», Москва, 18-20 октября 2011 г. – Российский вестник детской хирургии, анестезиологии и реаниматологии (Приложение). 2011. – С. 59-60.
13. Ростовская В.В., Матюшина К.М., Казанская И.В., Бабанин И.Л., Расулов Н.С., Воронцов А.Л. Диагностика нарушений тубулярных функций поч-ки при гидронефрозе у детей первых лет жизни. //Детская хирургия. 2012. N 4. С. 6-12.
14. Romics I, Siller G, Kohnen R, Mavrogenis S, Varga J, Holman E. A special terpene combination (Rowatinex) improves stone clearance after extracorporeal shockwave lithotripsy in urolithiasis patients: a results of a placebo-controlled randomized trial. // Urol Int. 2010. Vol.86, N 1. P102-109.
15. Азизов А.П. Применение Роватинекса в лечении хронического пиелоне-фрита, осложненного нефролитиазом. // Фарматека. 2011. N 20. С. 88-90.
16. Сивков А.В., Черепанова Е.В., Шадеркина В.А. Применение фитопрепа-ратов на основе терпенов при мочекаменной болезни. // Эксперименталь-ная и клиническая урология. 2011. N 1. С.69-72.
17. Максимов В.А., Яровой С.К., Александров Н.С., Максудов Р.Р. Место фитотерапии в лечении мочекаменной болезни. // Урология. 2012. N 3. С.58-61.
18. Яровой С.К. Место фитопрепаратов на основе терпенов в комплексной терапии и метафилактике мочекаменной болезни. // Медицинская пано-рама. 2015. N 7. С.53-54.
19. Гуденко Ю.А., Казанская И.В., Лобжанидзе З.Б. Применение препарата Роватинекс в детской урологии. // Экспериментальная и клиническая урология. 2013. N 3. С.61-65.
20. Казанская И.В., Бабанин И.Л., Матюшина К.М. Роль фитотерапии «рова-тинексом» в прогнозировании динамики ретенционных изменений верх-них мочевых путей. // Репродуктивное здоровье детей и подростков. 2015. N 2. Тезисы IV съезда детских урологов-андрологов,4-5 апреля 2015 г., Москва, Зеленоград. С.







