Стриктура мочеточника – это уменьшение просвета мочеточника различного генеза, характеризующееся явлениями функциональной обструкции верхних мочевыводящих путей (ВМП). На сегодняшний день, большинство авторов оценивают эффективность эндоскопического рассечения сужений мочеточников на уровне 78-89% [1,2]. Основными преимуществами эндоуретеротомии являются меньшая инвазивность, более низкие летальность и длительность госпитализации, более быстрое восстановление пациента по сравнению с открытыми или эндовидеохирургическими пластиками мочеточника [3-6].
Стриктуры мочеточников на начальном этапе формирования морфологических изменений стенки мочеточника часто протекают бессимптомно, что может приводить к несвоевременной диагностике изменений со стороны ВМП. Будучи не выявленным, сужение мочеточника в большинстве случаев приводит к развитию ипсилатеральной гидронефротической трансформации, истончению паренхимы и снижению почечной функции [7]. У многих пациентов, страдающих данной патологией, одним из этапов лечения является установка нефростомического дренажа для восстановления пассаж мочи и снятия избыточного гидростатическое давление.
Некоторым пациентам (около 30%) производят эндоуретеротомию с функционирующим нефростомическим дренажем [8]. В тоже время обязательным финальным этапом эндоскопического рассечения сужения мочеточника является установка мочеточникового стента, который не только выполняет роль каркаса для регенерации тканей мочеточника, но и дренирует ВМП. Таким образом, в послеоперационном периоде встает вопрос выбора метода дренирования ВМП (стент или нефростомический дренаж?) и его длительности.
До сих пор не определена оптимальная длительность нахождения стента в мочеточнике после эндоуретеротомии. С одной стороны, стент должен выполнять роль «каркаса», на котором происходит заживление тканей мочеточника – т.е. желательным является его длительное нахождение в органе. В исследовании Р.В. Салюкова рекомендованным является срок стентирования мочеточника после его реканализации не менее 8 недель, в то время как в более современных работах А.Г. Мартова и соавт. рутинная длительность стентирования мочеточника составляет 4-6 недель [9-11]. С другой стороны, стент является инородным телом, поддерживающим воспалительный процесс. По мнению некоторых исследователей – полное восстановление тканей мочеточника длится 7 недель.
Однако было выявлено, что как только достигается полная регенерацию эпителия, мочеточниковый стент перестает играть роль «помощника» и запускает каскад воспалительного ответа организма, приводящий к усиленному делению фибробластов [12].
Сниженный пассаж мочи через зону хирургического вмешательства может способствовать неправильной эпителизации места инцизии и приводить к усиленному росту фибробластов. Так, M.E. Jabbour выявил, что у пациентов со сниженной функций ипсилатериальной почки, у которых результаты эндоуретеротомии были не удовлетворительны, наблюдается снижение уровней TGF-β – цитокина, стимулирующего пролиферацию мезенхимальных клеток, регенерацию гладкой мускулатуры и заживление ран [13].
Однако не только сниженная функция ипсилатеральной почки может приводит к снижению пассажа мочи через зону инцизии стриктуры. Нефростомический дренаж, особенно установленный через нижнюю группу чашечек, снижает отток мочи по ВМП в мочевой пузырь. До настоящего времени не существует исследований, посвященных срокам перекрытия и удаления уже имеющегося нефростомического дренажа после выполнения эндоуретеротомии.
На данный момент в России и за рубежом не существует клинических рекомендаций, регламентирующих вид и длительность послеоперационного дренирования почки после выполненной эндоуретеротомии.
МАТЕРИАЛЫ И МЕТОДЫ
Целью данной работы явилось изучение влияния метода и длительности дренирование ВМП после эндоуретеротомии с применением различного вида энергии. В основу исследования положен проспективный анализ эндоскопического лечения 148 пациентов с непротяженными доброкачественными стриктурами мочеточника в период с 2007 по 2016 гг. в СПб ГБУЗ Клиническая больница Святителя Луки. 67 женщин (45,3%) и 81 мужчины (54,7%) были включены в исследование, медиана возраста больных составила 48 (34;60) лет.
У всех пациентов по данным инструментальных обследований (ультразвуковое исследование почек, внутривенная урография или КТ органов забрюшинного пространства с внутривенным контрастированием) отмечалось наличие гидронефроза различной степени, согласно классификации постнатального гидронефроза Society of Fetal Ultrasound (2010).
Результаты предоперационного обследования пациентов представлены по группам и отражены в таблице 1.
Таблица 1. Результаты предоперационного обследования
| Показатели | Группа «1» | Группа «2» | Группа «3» | Группа «4» |
|---|---|---|---|---|
| Возраст, лет Ме (Q25;Q75) | 53 (40;60) | 45 (33;55) | 53 (40;62) | 37 (39;57) |
| Пол, отношение муж/жен | 35/34 | 23/16 | 13/8 | 10/9 |
| Анамнез | ||||
| Наличие МКБ, чел. (%) | 55 (79,7) | 27 (69,2) | 15 (71,4) | 8 (42,1) |
| Длительность МКБ, лет Ме (Q25;Q75) | 5 (2;8) | 6 (0;9) | 6 (0;10) | 0 (0;7) |
| Наличие пиелонефрита, чел. (%) | 25 (36,2) | 14 (36,9) | 13 (61,9) | 10 (52,6) |
| Длительность пиелонефрита, лет Ме (Q25;Q75) | 0 (0;6) | 0 (0;7) | 2 (0;5) | 1 (0;4) |
| Самостоятельное отхождение камней, чел. | 26 (37,7) | 16 (41,0) | 7 (33,3) | 3 (15,8) |
| Камень, чел. (%) | 47 (68,1) | 16 (41,0) | 8 (38,1) | 2 (10,5) |
| Эндоскопические вмешательства, чел. (%) | 27 (39,1) | 12 (30,8) | 11 (52,4) | 9 (47,4) |
| Протяженность стриктуры, мм. Ме (Q25;Q75) | 10 (6;14) | 11 (6;14) | 11 (7;14) | 13 (7;19) |
| Локализация стриктуры, кол-во пациентов (%) | ||||
| Левый/правый мочеточник | 39/30 | 18/21 | 10/11 | 10/9 |
| Пиело-уретеральный сегмен | 9 (13,0) | 12 (30,8) | 1 (4,8) | 4 (21,1) |
| Верхняя треть мочеточника | 12 (17,4) | 7 (17,9) | 4 (19,0) | 2 (10,5) |
| Средняя треть мочеточника | 4 (5,8) | 5 (12,8) | 4 (19,0) | 2 (10,5) |
| Нижняя треть мочеточника | 44 (63,8) | 15 (38,5) | 12 (57,1) | 11 (57,9) |
| Этиология стриктуры, кол-во пациентов (%) | ||||
| Врожденная | 8 (11,6) | 12 (30,8) | - | 4 (21,1) |
| Воспалительная | 30 (43,5) | 12 (30,8) | 7 (33,3) | 3 (14,3) |
| Ятрогенная | 28 (40,6) | 14 (35,9) | 13 (61,9) | 9 (47,4) |
| Лучевая | 2 (2,9) | 1 (2,6) | м | 1 (5,3) |
| Идиопатическая | 1 (1,4) | - | - | 2 (10,5) |
| Сопутствующие заболевания, кол-во пациентов (%) | ||||
| Сердечно-сосудистые заболевания | 30 (43,5) | 15 (38,5) | 13 (61,9) | 6 (31,6) |
| Сахарный диабет | 23 (33,3) | 7 (17,9) | 11 (52,4) | 3 (14,3) |
| Наличие келоидных рубцов | 13 (18,8) | 11 (28,2) | 5 (23,8) | 7 (36,8) |
| Гидронефроз до операции, кол-во пациентов (%) | ||||
| 1 степень | 25 (36,2) | 14 (35,9) | 6 (28,6) | 2 (10,5) |
| 2 степень | 37 (53,6) | 19 (48,7) | 10 (47,6) | 15 (78,9) |
| 3 степень | 7 (10,1) | 6 (15,4) | 5 (23,8) | 2 (10,5) |
Обращает на себя внимание тот факт, что наиболее часто возникновение сужения мочеточника было связано с хроническими воспалительными заболеваниями ВМП (35,1%) и врачебными воздействиями (43,2%).
Пациентам, поступившие в стационар с клинической картиной выраженного воспалительного процесса в верхних мочевыводящих путях (14 человек), предварительно производилось восстановление адекватного пассажа мочи путем выполнения ипсилатеральной перкутанной нефростомии. Последующие вмешательства выполнялись после купирования воспалительного процесса, но не ранее, чем через 21 день после нефростомии.
Пациенты, не имевшие на момент выполнения оперативного вмешательства нефростомического дренажа, были включены в группу "A". У 40 пациентов (27,0%) на момент выполнения эндоскопического рассечения стриктуры мочеточника имелся ипсилатеральный нефростомический дренаж с медианой срока нахождения 3 (2;8) месяца. Данные пациенты были включены в группу "Б".
Группы «А» и «Б» не имели достоверных различий в возрастном и гендерном составе, особенностях анамнеза пациентов (заболевания мочекаменной болезнью, хроническим пиелонефритом), протяженности, локализации и этиологии стриктур мочеточников, степени гидронефротической трансформации почки.
В завершении оперативного вмешательства всем пациентам устанавливался мочеточниковый стент. Было установлено 58 (39,1%) эндопиелотомических стентов и 90 (60,8%) JJ-стентов. Размер и вид стента выбирались интраоперационно в зависимости от анатомических особенностей пациента, локализации зоны хирургического интереса и наличия расходного материала на момент выполнения процедуры.
Группы «А» и «Б» имели по 2 подгруппы в зависимости от вида использованного мочеточникового стента. Дизайн исследования представлен на рисунке 1.
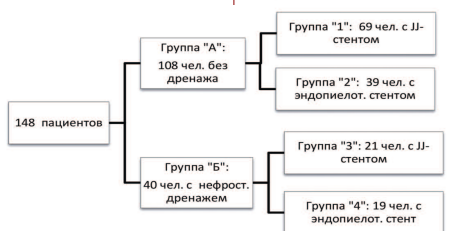
Рис.1. Дизайн исследования
Все пациенты были прооперированы: производилось эндоскопическое рассечение суженного участка мочеточника с использованием различных методов – эндоскопического ножа/ножниц, электроножа, лазерного волокна (табл. 2).
Таблица 2. Методики оперативного вмешательства в группах
| Группа «1» | Группа «2» | Группа «3» | Группа «4» | |
|---|---|---|---|---|
| Вид эндоуретеротомии, кол-во пациентов (%) | ||||
| «Холодный нож» | 30 (43,5) | 12 (30,8) | 12 (57,1) | 3 (14,3) |
| Лазерная | 21 (30,4) | 11 (28,2) | 1 (4,8) | 10 (52,6) |
| Электрическая | 18 (36,1) | 27 (41,0) | 8 (38,1) | 6 (31,6) |
РЕЗУЛЬТАТЫ
Сроки удаления мочеточникового стента определялись индивидуально и зависели от интраоперационной картины, сопутствующих заболеваний и, иногда, возможностей пациента
Эффективность эндоуретеротомии оценивались не ранее, чем через 4 недели после удалениямочеточникового стента. Результаты разделяли по двухуровневой системе: «удовлетворительный» или «неудовлетворительный». «Удовлетворительным» считался результат, когда на момент опроса пациент не предъявлял жалоб, типичных для заболеваний ВМП и почек со стороны операции, и отсутствовали данные о рецидиве стриктуры по результатам УЗИ и внутривенной урографии: определялась полная проходимость мочеточника для контрастного вещества, значительное сокращение полостей почки и мочеточника, отсутствие отрицательных изменений со стороны паренхимы почки.
Неудовлетворительныи результат признавался при возникновении стриктуры мочеточника в течение всего периода наблюдения.
Ближайшие и отдаленные результаты оперативного лечения отражены в таблице 3.
Таблица 3. Ближайшие и отдаленные результаты оперативного лечения
| Группа «1» | Группа «2» | Группа «3» | Группа «4» | |
|---|---|---|---|---|
| Период наблюдения, мес. Ме (Q25;Q75) | 18 (12;26) | 18 (10;22) | 16 (10;18) | 18 (10;23) |
| Период стентирования, нед. Ме (Q25;Q75) | 6 (6;8) | 7 (6;8) | 8 (7;8) | 7 (6;8) |
| Гидронефроз через 3 дня после операции, кол-во пациентов (%) | ||||
| 0 степень | 26 (37,7) | 14 (35,9) | 5 (23,8) | 5 (26,3) |
| 1 степень | 29 (42,0) | 19 (48,7) | 11 (52,4) | 7 (36,8) |
| 2 степень | 14 (20,3 | 6 (15,4) | 5 (23,8) | 6 (31,6) |
| 3 степень | - | - | - | 1 (5,3) |
| Гидронефроз перед удалением стента, кол-во пациентов (%) | ||||
| 0 степень | 47 (68,1) | 30 (76,9) | 14 (66,7) | 9 (47,4) |
| 1 степень | 18 (26,1) | 8 (20,5) | 7 (33,3) | 8 (42,1) |
| 2 степень | 4 (5,8) | 1 (2,6) | 2 (10,5) | |
| Нефростома перекрыта через, дней Ме (Q25;Q75) | n/a | n/a | 5(3;6) | 4(1;5) |
| Рецидив, кол-во чел. (%) | 14 (20,3) | 7 (17,9) | 9 (42,9) | 7 (36,8) |
Общая эффективность эндоскопических методов коррекции непротяженных стриктур мочеточников составила 75%. У пациентов, не имевших нефростомического дренажа, рецидив стриктуры мочеточника произошел в 21 случае (19,4%).Утех пациентов, кто перенес оперативное вмешательство с ранее установленным нефростомическимдренажом, эффективность лечения была ниже: рецидив произошел у 16 человек, что составило 40% от всех пациентов групп «3» и «4».
Отдаленный результат эндоскопического лечения непротяженных стриктур мочеточников достоверно не отличался у пациентов в различных группах (р>0,05). Однако, выявлена статистическая тенденция (р=0,09) к развитию рецидива у тех пациентов, кто имел нефростомический дренаж и кому был впоследствии установлен JJстент.
73 (49,3%) пациента помимо стриктуры имели конкремент мочеточника. У 17 (23,8%) из них в отдаленном периоде развился рецидив сужения мочеточника, что оказалось меньше, чем в группе пациентов, не имевших конкремента мочеточника (26,6%), однако различия не было статистически достоверным (р>0,05). Таким образом, очевидно, что наличие конкремента мочеточника не является фактором, способствующим развитию рецидива сужения мочеточника в различных группах больных.
У пациентов с безрецидивным течением послеоперационного периода длительность стентирования мочеточника составила 6,9±1,5 недель, в то время как у пациентов, имеющих рецидив заболевания, стент находился 7,0±1,1 недель (р>0,05).
Срок перекрытия нефростомического дренажа достоверно отличался у пациентов, перенесших рецидив сужения мочеточника и с безрецидивным характером течения послеоперационного периода. Зависимость эффективности эндоуретеротомии от сроков пережатия нефростомического дренажа приведена на рисунке 2, из которого видно, что средний срок пережатия нефростомического дренажа составил 6 суток у пациентов, с рецидивом стриктуры мочеточника в отдаленном периоде, что оказалось достоверно больше, чем у пациентов с эффективной эндоуретеротомией (р<0,05)
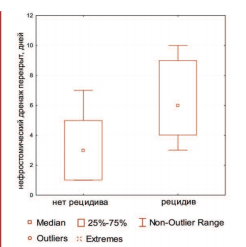
Рис.2. Зависимость эффективности эндоуретеротомии от сроков пережатия нефростомического дренажа
Проведен анализ причин повторного стриктурообразования во всех случаях. Факторы, имеющие достоверное отличие у пациентов с различной эффективностью уретеротомии, приведены в таблице 4, к ним относятся: наличие нефростомического дренажа, пережатие нефростомического дренажа позднее 3-х дней, гидронефроз 3-й степени на 3 сутки и 2-й степени перед удалением стента.
Таблица 4. Анализ факторов, влияющих на развитие рецидива стриктуры мочеточника
| Прогностический фактор | ОР рецидива | P |
|---|---|---|
| Наличие нефростомического дренажа | 2,8 | <0,05 |
| Пережатие нефростомического дренажа после 3-х дней | 4,4 | <0,05 |
| Гидронефроз на 3-ие сутки: 3 ст. против 0 ст. | 6,5 | <0,05 |
| Гидронефроз перед удалением стента: 2 ст. против 0 ст. | 44,0 | <0,05 |
* ОР – относительный риск
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ И ВЫВОДЫ
По нашим данным общая эффективность эндоуретеротомии составила 75%, что в целом соотносится с диапазоном значений эффективности методики, полученным в работах зарубежных коллег [2,4,12,14,15,16].
По результатам нашей работы, вид и размер мочеточникового стента не оказывает значимого влияния на результат эндоуретеротомии. Аналогичные данные были получены в нескольких проспективных экспериментальных исследованиях, выполненных на минипигах [17]. S. Razdan и соавторы с успехом используют одномоментную установке двух JJ-стентов, что позволяет улучшить шансы на успешное лечение даже пациентов «группы высокого риска рецидива» [12].
По нашим данным длительность стентирования мочеточника не может быть признана фактором, оказывающим влияние на результаты эндоуретеротомии. Диапазон длительности стентирования мочеточника составил 6-8 недель. Но даже в таких пределах мы не обнаружили статистически значимых различий в результатах лечения. Именно срок 6 недель рекомендуют большинство зарубежных коллег [17]. Однако некоторые авторы, основываясь на результатах экспериментальных работ на животных, утверждают, что достаточный срок для успешного восстановления мочеточника после эндоуретеротомии составляет от 1 до 3 недель [18,19].
В нашем исследовании были выявлены статистически значимые различия в эффективности эндоуретеротомии в зависимости наличия или отсутствия у пациента перед операцией ранее установленного нефростомического дренажа. Так пациенты, перенесшие чрезкожное дренирование полостной системы до операции, имели достоверно более плохие результаты конечного лечения. В российской и зарубежной литературе отсутствуют данные о влиянии нефростомического дренажа на результаты эндоуретеротомии.
Безусловно, полученные нами данным требуют проверки на большей выборке пациентов, и при подтверждении результатов исследования можно будет сделать вывод о нецелесообразности установки нефростомического дренажа в случае невыраженного гидронефроза, в рамках часто негласно принятой «подготовки к оперативному лечению».
Кроме того, в нашей работе было выявлено, что «раннее» (в течение 3х суток после эндоуретеротомии) перекрытие нефростомического дренажа оказывает протективное воздействие и улучшает результаты эндоуретеротомии (ОР=4,4, р<0,05). Подобные зависимости еще не были описаны в литературе и требуют дальнейшего изучения. Отмеченная зависимость связана с имеющимися данными о негативном влиянии сниженния почечной функции на результаты эндоуретеротомии [20-22]. Вероятно, нормальный пассаж мочи через зону рассечения мочеточника необходим для правильного формирования эпителия и сдерживания роста фибробластов.
ЗАКЛЮЧЕНИЕ
Эндоскопическая коррекция непротяженных стриктур мочеточников достаточно эффективна при меньшей инвазивности и затратности по сравнения с открытой и лапароскопической реконструкциями мочеточника.
В работе показано, что вид внутрипросветного стента и длительность стентирования мочеточника не оказывают влияния на вероятность развития рецидива стриктуры. Однако наличие нефростомического дренажа признано фактором неблагоприятного прогноза в оценке отдаленных результатов эндоуретеротомии. Кроме того, выявлено что перекрытие имеющегося нефростомического дренажа в течение первых трех суток после операционного вмешательства повышает эффективностью эндоуретеротомии в отдаленной перспективе. Необходим дальнейший научный поиск факторов, которые могут оказывать влияние на успех эндоуретеротомии, что в последствие приведет к повышению эффективности методики в целом.
ЛИТЕРАТУРА
1. Goldfischer ER, Gerber GS.. Endoscopic Management of Ureteral Strictures. e Journal of Urology. 1997; 157 (3): 770–75. doi:10.1016/S0022-5347(01)65037-7.
2. Corcoran AT, Smaldone MC, Ricchiuti DD, Averch TD. Management of Benign Ureteral Strictures in the Endoscopic Era. J Endourol. 2009; 23 (11): 1909–12. doi:10.1089/end.2008.0453.
3. Richter F, Irwin RJ, Watson RA, Lang EK. Endourologic Management of Benign Ureteral Strictures with and without Compromised Vascular Supply. Urology 2000; 55 (5): 652–56. doi:10.1016/S0090-4295(00)00484-2.
4. Meretyk S, Albala DM, Clayman RV, Denstedt JD, Kavoussi LR. Endoureterotomy for Treatment of Ureteral Strictures. J Urol. 1992; 147 (6): 1502–6. doi.org/10.1016/s0022-5347(17)37608-5
5. Fasihuddin Q, Abel F, Hasan AT, Shimali M. Effectiveness of Endoscopic and Open Surgical Management in Benign Ureteral Strictures. J Pakistan Med Associ. 2001; 51 (10): 351–53
6.Kachrilas S, BourdoumisA,Karaolides T, Nikitopoulou S, Papadopoulos G, Buchholz N et al.Current Status of Minimally Invasive Endoscopic Management of Ureteric Strictures.era Adv in Urology 2013; 5 (6). SAGE Publications: 354–65. doi:10.1177/1756287213505671.
7. Wein AJ , Kavoussi LR, Partin AW, Peters CA. Campbell-Walsh Urology. 11 ed. Elsevier Health Sciences. 2016.
8. Anastasescu R, Merrot T, Chaumoître K, Panuel M, Alessandrini P. Antegrade Percutaneous Balloon Dilation of Ureteral Strictures aer Failed Pelviureteric or Ureterovesical Reimplantation in Children. Urology 2011; 77(6): 1444–49. doi:10.1016/j.urology.2010.10.052.
9. Салюков Р.В. Рентгеноэндоскопическая Диагностика И Лечение Облитераций Мочеточников И Лоханочно-Мочеточникового Сегмента. Автореф. канд. мед. наук. Москва, 2002. URL: https://dlib.rsl.ru/viewer/01000346232#? page=1 Ссылка активна на 28.03.2018
10. МартовА.Г.,КорниенкоС.И. Малоинвазивный способ лечения стриктур верхних мочевых путей. Кубанский Научный Медицинский Вестник. 2010; 8: 126–33.
11.МартовА.Г.,ЕргаковД.В.,АндроновА.С.,ДутовС.В.Малоинвазивное Лечение Стриктур Верхних Мочевых Путей. Хирургия. Журнал Им. Н.И. Пирогова. 2014;12: 46–55.
12. Razdan S, Silberstein IK, Bagley DH. Ureteroscopic Endoureterotomy. BJU Inter. 2005;95: 94–101. doi:10.1111/j.1464-410X.2005.05207.x.
13. Jabbour ME, Goldfischer ER, Anderson AE, Smith AD, and Kushner L. Endopyelotomy Failure Is Associated with Reduced Transforming Growth Factor-Beta. J Urol. 1998; 160 (6): 1991–94. doi:10.1097/00005392-199812010-00012
14.Hibi H, Ohori T, Taki T, Yamada Y, Honda N. Long-Term Results of Endoureterotomy Using a Holmium Laser. International J Urol. 2007; 14 (9): 872–74. doi:10.1111/j.1442-2042.2007.01835.x.
15.Lane BR., Singh D, Meraney A, Streem SB. Novel Endourologic Applications for Holmium Laser. Urology. 2005; 65 (5): 991–93. doi:10.1016/j.urology.2005.01.050.
16. Lojanapiwat B, Soonthonpun S, Wudhikarn S. Endoscopic Treatment of Benign Ureteral Strictures. Asian J Surgery 2002; 25 (2): 130–33. doi:10.1016/S1015-9584(09)60160-3.
17. Shah O, Marien T. Ureteral and Ureteroenteric Strictures. In Ureteroscopy. Totowa (NJ): Humana Press; 2013.
18. Kerbl K, Chandhoke PS, Figenshau RS, Stone AM, Clayman RV. Effect of Stent Duration on Ureteral Healing Following Endoureterotomy in an Animal Model. J Urol. 1993; 150 (4): 1302–5. doi: 10.1016/s0022-5347(17)35765-8
19. Soria F, Sánchez FM, Sun F, Ezquerra J, Durán E, Usón J. Comparative Study of Ureteral Stents Following Endoureterotomy in the Porcine Model: 3 vs 6 Weeks and 7F vs 14F. CardioVascul Interven Radiol. 2003; 28 (6): 773–78. doi:10.1007/s00270-004-0266-3.
20. Gnessin E, Yossepowitch O, Holland R, Livne PM, Lifshitz DA. Holmium Laser Endoureterotomy for Benign Ureteral Stricture: A Single Center Experience. J Urol. 2009; 182 (6): 2775–79. doi:10.1016/j.juro.2009.08.051.
21. Erdogru T, Kutlu O, Koksal T, Danisman A, Usta MF, Kukul E, Baykara M. Endoscopic Treatment of Ureteric Strictures: Acucise, Cold-Knife Endoureterotomy and Wall Stents as a Salvage Approach. Urologia Internat. 2005; 74 (2): 140–46. doi:10.1159/000083285.
22. Lane BR, Desai MM, Hegarty NJ, Streem SB. Long-Term Efficacy of Holmium Laser Endoureterotomy for Benign Ureteral Strictures. Urology 2006; 67 (5): 894–97. doi:10.1016/j.urology.2005.11.012.







