Несмотря на эффективность медикаментозной терапии доброкачественной гиперплазии предстательной железы (ДГПЖ), в ряде случаев, ее симптоматический эффект оказывается недостаточным. В связи с этим поиск новых методов коррекции симптомов нарушения функции нижних мочевых путей (СНМП) при ДГПЖ остается актуальным. На наш взгляд «идеальная терапия» СНМП при ДГПЖ должна вызывать: атрофию (редукцию объема) предстательной железы, уменьшать симптомы и инфравезикалную обструкцию. Принимая во внимание механизм действия ботулинического токсина типа А (БТА) и патофизиологию нарушений мочеиспускания при ДГПЖ, имеются основания предположить, что интрапростатические инъекции ботулотоксина окажутся эффективными.
В литературе нами найдено лишь 7 исследований [4-10], посвященных интрапростатическим инъекциям БТА при ДГПЖ. Причем только исследование Maria et al. [10] является двойным слепым плацебо-контролируемым. Число пациентов в большинстве исследований не превышало 30 человек. Оценивались объем предстательной железы, скорость мочеиспускания и число баллов по шкале IPSS до начала лечения и в различные периоды после процедуры.
Мы располагаем опытом 5-месячного наблюдения пациента после интрапростатического введением БТА (Лантокс) по поводу СНМП обусловленных ДГПЖ.
Жалобы. Пациент Х., 62 лет, обратился с жалобами на ноктурию до 3-х раз, учащенное мочеиспускание (до 10 раз) днем, чувство неполного опорожнения мочевого пузыря.
Анамнез. Считает себя больным более 10 лет. Получал терапию альфа-адреноблокаторами и растительными экстрактами с умеренным эффектом. Сопутствующие заболевания отрицает.
Осмотр. При осмотре и пальпации область почек и мочевого пузыря не измена. Предстательная железа при осмотре per rectum увеличена в размерах, безболезненна, без уплотнений, срединная борозда сглажена.
Инструментальные и лабораторные исследования. Клинические анализы мочи, крови и биохимический анализ крови без отклонений. Пациент имел умеренную степень СНМП. В ходе исследования оценивались: симптомы по шкале IPSS; параметры мочеиспускания методом урофлоуметрии; объем простаты ультразвуковым методом; сексуальная функция с помощью опросника МИЭФ и шкалы количественной оценки мужской копулятивной функции (КОМКФ).
Таблица 1. Динамика основных клинических показателей до и в различные сроки после введения БТА
Показатели |
До лечения |
1 месяц после лечения |
2 месяца после лечения |
5 месяцев после лечения |
IPSS (баллы) |
13 |
8 |
7 |
8 |
QOL (баллы) |
3 |
2 |
2 |
2 |
Q (мл/сек.) max * / ' |
14 |
21,7 |
19 |
22 |
V прост (см3) |
68 |
41 |
39 |
34 |
МИЭФ |
38 |
35 |
37 |
37 |
КОМКФ |
26 |
30 |
31 |
27 |
Лечение. В условиях дневного стационара пациенту под аппликационной анестезией под ультразвуковым контролем трансректально в предстательную железу было введено 200 ЕД Лантокса (2 инъекции в каждую долю по 50 ЕД соответственно). Препарат разведен в 8 мл стерильного физиологического раствора. Для проведения процедуры использовался ультразвуковой аппарат с трансректальным датчиком и насадкой для проведения биопсии и игла для эндоскопических вмешательств Ch 5 (рисунок 1).
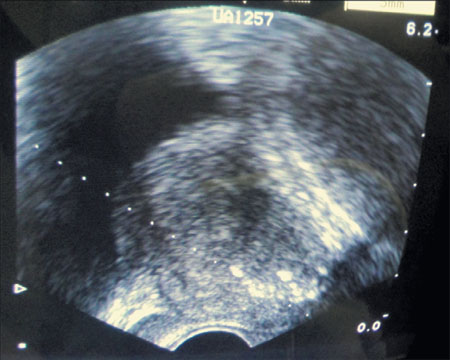
Рисунок 1. Трансректальная УЗ навигация интрапростатического введения препарата Лантокс пациенту Х.
Процедура наведения иглы под контролем ТРУЗИ идентична таковой при биопсии простаты.
Результаты. Динамика основных клинических показателей до и в различные сроки после введения БТА представлена в таблице 1.
При анализе результатов через 5 месяцев отмечено клинически значимое уменьшение симптомов по шкале IPSS c 13 до 8 баллов, клинически значимое увеличение максимальной объемной скорости мочеиспускания (Qmax) с 14 до 22 мл/сек., а также достоверное уменьшение объема предстательной железы с 68 см3 до 34 см3. По данным опросников, клинически значимого изменения показателей половой функции у пациента не зарегистрировано.
Таким образом, через 5 месяцев после интрапростатического введения БТА пациенту с СНМП и ДГПЖ достигнуто:
- уменьшение симптомов по шкале IPSS;
- увеличение объемной скорости мочеиспускания;
- атрофия (уменьшение объема) предстательной железы.
Заключение. Полученный результат позволяет сделать вывод о возможности ботулинотерапии СНМП при ДГПЖ. В настоящее время мы наблюдаем еще 5 больных на разных сроках после интрапростатического введения БТА (Лантокс). После получения статистически значимых данных можно будет сделать более достоверные выводы о перспективности данного метода коррекции симтомов при ДГПЖ.
Ключевые слова: ботулинический токсин типа А, доброкачественная гиперплазия предстательной железы, симптомы нижних мочевых путей.
ЛИТЕРАТУРА
- Каприн А.Д., Иванов С.А., Клименко А.А. Уроантисептическая терапия в лечении лучевого цистита у женщин. Российский научный центр рентгенрадиологии МЗ РФ. 2005.
- Галил-Оглы Г.А., Каприн А.Д., Титова В.А., Паклина О.В., Чазова Н.Л., Клименко А.А. Функциональные и морофологические изменения нижних мочевых путей в процессе лучевой терапии на органы малого таза. М. 2004.
- Chuang Y.C., Kim D.K., Chiang P.H., Chancellor M.B. Bladder botulinum toxin A injection can benefit patients with radiation and chemical cystitis. BJU Int. 2008 Sep; 102 (6): 704-6.
- Chuang Y.C., Tu C.H., Huang C.C. et al. Intraprostatic injection of botulinum toxin type-A relieves bladder outlet obstruction in human and induces prostate apoptosis in dogs. BMC Urology 2006; 6:12.
- Kuo H.C. Prostate botulinum A toxin injection an alternative treatment for benign prostatic obstruction in poor surgical candidates. Urology 2005; 65: 670-4.
- Park D.S., Cho T.W., Lee Y.K., LeeY.T., Hong Y.K., Jang W.K. Evaluation of short-term clinical effects and presumptive mechanism of botulinum toxin type A as a treatment modality of benign prostatic hyperplasia. Yons Med J 2006; 47: 706-14.
- Larson T.R., Scottsdalle A.Z., Huidobro C. et al. Intraprostatic injection of botulinum toxin in the treatment of symptomatic LUTS, including sequential MRIs for accurate changes in size of the prostate. J Urol 2005; 173 (suppl): 376.
- Guercini F., Giannantoni A., Bard R.L. et al. Intraprostatic botulin toxin injection in patients with severe benign prostatic hyperplasia: a multicenter feasibility study. J Urol 2005; 173 (suppl): 376-7.
- Silva J., Silva C., Saraiva L. et al. Intraprostatic botulinum toxin type A injection in patients unfit for surgery presenting with refractory urinary retention and benign prostatic enlargement. Effect on prostate volume and micturition resumption. Eur Urol 2008; 53: 153.
- Maria G., Brisinda G., Civello I.M., Bentivoglio A.R., Sganga G., Albanese A. Relief by botulinumtoxin of voiding dysfunction due to benign prostatic hyperplasia: Results of a randomized, placebo-controlled study. Urology 2003; 62:.259-64.






